ANTIGENO SINTETICO PARA LA DETECCION DE ANTICUERPOS INMUNOREACTIVOS CON EL VIRUS VIH.
Un método para determinar la presencia de anticuerpos de VIH en un fluido corporal,
incluyendo:
(a) contacto en condiciones que permitan la unión inmunoespecífica para formar una mezcla de reacción del fluido corporal con una composición que contenga por lo menos un polipéptido seleccionado del grupo consistente en las secuencias de aminoácidos:
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E07007809.
Solicitante: BIO-RAD LABORATORIES, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1000 ALFRED NOBEL DRIVE,HERCULES, CA 94547.
Inventor/es: COLE, CAROL-ANN, MONJI, NOBUO, COLEMAN,PATRICK,F, CHONG-DUG SU,PETER, GOSHORN,ALICE,KAMP.
Fecha de Publicación: .
Fecha Solicitud PCT: 31 de Julio de 1998.
Fecha Concesión Europea: 12 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07K14/16 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › VIH-1.
- G01N33/569K2
Clasificación PCT:
- C07K14/00 C07K […] › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K14/16 C07K 14/00 […] › VIH-1.
- C07K7/00 C07K […] › Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados.
- C12Q1/70 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen virus o bacteriófagos.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
Fragmento de la descripción:
Antígeno sintético para la detección de anticuerpos inmunoreactivos con el virus VIH.
Campo de la invención
Esta invención se refiere a polipéptidos sintéticos, polipéptidos recombinantes y secuencias de polinucleótidos recombinantes codificando las mismas, útiles para la detección de anticuerpos asociados al virus de inmunodeficiencia humana tipo 1 (VIH-1) y/o tipo 2 (VIH-2) (en lo sucesivo, "VIH" utilizado sin referencia al tipo significará cualquiera de ambos tipos), y se refiere en especial a polipéptidos sintéticos que imitan epítopos antigénicos de los productos de gen de la región de la polimerasa VIH.
Antecedentes de la invención
Se sabe que los virus de la inmunodeficiencia humana tipos 1 y 2 (VIH-1 y VIH-2) causan el síndrome de inmunodeficiencia humana adquirida (SIDA). Aparentemente, ambos virus presentan formas similares de transmisión. El VIH-1 y el VIH-2 fueron aislados al principio de la década de 1980 en pacientes africanos con SIDA. Desde entonces se han identificado casos en la mayoría de países del mundo. Como los virus VIH presentan una rápida deriva genética, están surgiendo cepas ampliamente divergentes. Por ello, se ha demostrado que la detección y el tratamiento de las cepas variantes resulta problemático y difícil.
Los individuos con anticuerpos reactivos al VIH-1 y/o VIH-2 se determinan mediante inmunoensayos del formato sándwich ELISA convencional. Estos ensayos comprenden un antígeno viral inmovilizado, que puede incluir lisado viral, proteínas de retrovirus o polipéptidos naturales o sintéticos, que entran en contacto con sangre o componentes séricos sospechosos de contener anticuerpos HTV. Si bien los tests comerciales existentes parecen haber reducido significativamente la transmisión de virus VIH en productos hematológicos, la configuración de cada test puede presentar algunos inconvenientes.
Los posibles inconvenientes de los tests de lisado viral incluyen: la necesidad de cultivar y manipular grandes cantidades de virus infecciosos vivos; la posibilidad de que los virus vivos puedan incorporarse a los materiales del test; la naturaleza variable del lisado viral resultante; y el importante número de resultados falsos positivos y falsos negativos, que requieren pruebas adicionales de confirmación. Estos inconvenientes pueden ir también asociados al uso de proteínas virales aisladas como antígenos.
El uso de polipéptidos sintéticos, (en lo sucesivo, "polipéptido sintético" y "polipéptido" significará cualquiera, todos o una combinación de lo siguiente: polipéptido sintético, polipéptido recombinante, o polipéptido) que puede ser manipulado para imitar inmunológicamente epítopos antigénicos de los virus VIH, puede evitar algunos de los inconvenientes antes mencionados. Un área de preocupación con el uso de polipéptidos sintéticos (menos de o igual a 60 residuos de longitud) en ensayos diagnósticos es la consideración de que la deriva antigénica viral podría hacer que no se detectaran sueros infectados con VIH-1 o VIH-2 utilizando esos ensayos, posiblemente debido a la limitada presentación de epítopos virales. Un método para evitar tal cosa es incluir polipéptidos de distintas regiones inmunodominantes del genoma viral. Por tanto, polipéptidos sintéticos que imiten inmunológicamente regiones inmunodominantes de los productos del gen pol de VIH-1 y VIH-2 son importantes adiciones a los ya descritos polipéptidos que imitan las proteínas env, gag y pol de VIH-1 y VIH-2. Las patentes de los Estados Unidos Nº 4.629.783 y 5.075.21 1 describen polipéptidos sintéticos que imitan determinantes antigénicos de VIH-1. La Patente Cosand de Estados Unidos 5.075.211 describe polipéptidos sintéticos que imitan inmunológicamente epítopos antigénicos de proteínas de VIH-1 de la región pol, incluyendo dos polipéptidos que son similares a los polipéptidos de esta invención. En ensayos de cribado de sangre, cuanto mayor es la inmunorreactividad de los antígenos utilizados en el método de ensayo, es menos probable que no se detecten anticuerpos de una nueva variante o subtipo de HTV-1 o VIH-2, presentes en la muestra de un paciente.
La Patente de Estados Unidos 5.306.466 describe un "retrovirus VIH-3" del que se creyó inicialmente que era algo aparte y distinto de VIH-1 y VIH-2. Posteriormente, los investigadores han establecido que el retrovirus VIH-3 es simplemente un subtipo especial del VIH-1, al que se denomina ahora subtipo O, o Grupo O (R. De Leys, et al., J. Virol.: 1207-1216 (1990); L.G Gürtler, et al. J. Virol.: 1581-1585 (1994)).
Comparando diversos aislados de VIH-1, los investigadores han demostrado que algunas regiones del genoma son altamente variables, mientras que otras se conservan razonablemente bien. Se han observado polimorfismos similares también en el VIH-2.
A pesar de las aparentes similitudes en el estado de la enfermedad y la transmisión de los virus VIH-1 y VIH-2, los tipos de virus se han diferenciado en base a su divergencia genética. En base a análisis genéticos, los aislados virales pueden ser agrupados de acuerdo con su homología genética con aislados previos. Hoy VIH-1 y VIH-2 conforman las dos principales ramas de árbol genético del VIH. Los estudios de hibridación de ADN sugieren que mientras existen algunas regiones de amplia homología entre VIH-1 y VIH-2, otras regiones parecen muy divergentes. (Clavel et al., Science 233:343 (1986)). De hecho, se ha comprobado que el VIH-2 tiene, en general, sólo una homología aproximada del 40% con el VIH-1, y los estudios han demostrado escasa reactividad inmunológica cruzada entre las glicoproteínas de la envoltura. La limitada reactividad serológica cruzada entre esos virus hace que los ensayos de cribado basados en antígenos de VIH-1 sean insuficientes para el cribado o diagnóstico de infección por VIH-2 en sueros humanos.
Resumen de la invención
La invención se define en las reivindicaciones que se anexan. Se han identificado secuencias de polipéptido denominadas ROD 124E1, ROD124C2X, RODC1X, RODC3X y ROD 124C5X, capaces de imitar regiones inmunodominantes de proteínas VIH-2, codificadas en la región polimerasa. Esos polipéptidos pueden usarse en varios ensayos específicos de unión para la detección de anticuerpos del virus VIH-2.
Breve descripción de las figuras
La Fig. 1 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pGEX/pol23.
La Fig. 2 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pGEX/pol7.
La Fig. 3 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pQE/pol23.
La Fig. 4 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pQE/pol7.
La Fig. 5 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pThioHis/pol23.
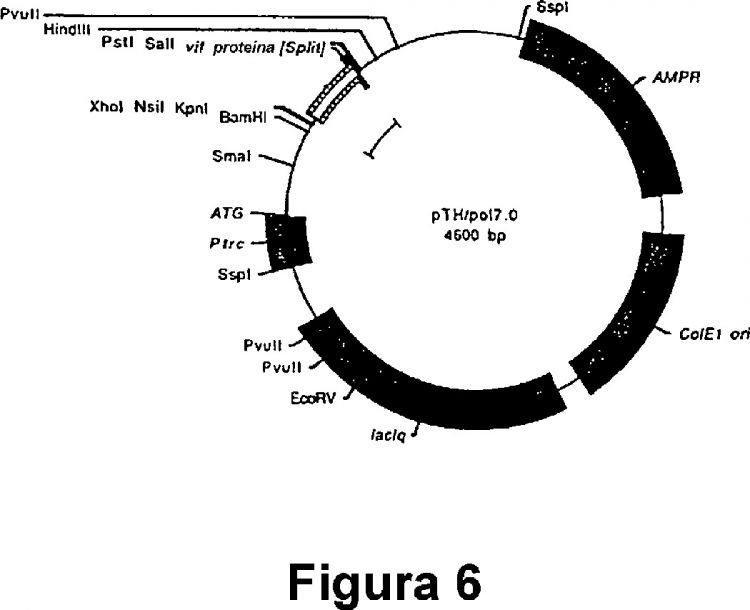
La Fig. 6 muestra un mapa de plásmidos de una de las estructuras recombinantes de la presente invención, más específicamente la de pThioHis/pol7.
Descripción detallada de las modalidades específicas
Se proporcionan nuevos polipéptidos que imitan inmunológicamente proteínas incluidas en los retrovirus VIH-2.
En general, el término "polipéptido" o "péptido" utilizado aquí significará una cadena de moléculas de aminoácidos con actividad biológica. Los términos no se refieren a un producto de una longitud específica.
Además, uno o más aminoácidos pueden añadirse a los extremos de un oligopéptido o polipéptido, para el acoplamiento a un soporte o portador.
Se prefiere en especial la cisteína para facilitar el acoplamiento covalente a otros polipéptidos o, por ejemplo, para formar dímeros por oxidación. Para formar polímeros, se prefiere tener por lo menos dos residuos de cisteína presentes en las moléculas que se están uniendo, de preferencia utilizando residuos de cisteína añadidos a las porciones terminales de los polipéptidos. También son útiles las combinaciones de cisteína con espaciadores de aminoácidos intervinientes. Por ejemplo, dos residuos de cisteína pueden ser separados por uno o más residuos de aminoácidos. Los residuos de glicina son especialmente útiles, y pueden emplearse de uno a tres residuos de glicina entre aminoácidos. También se ha comprobado que...
Reivindicaciones:
1. Un método para determinar la presencia de anticuerpos de VIH en un fluido corporal, incluyendo:

2. El método según la reivindicación 1 en el que el polipéptido se conjuga a una macromolécula portadora.
3. El método según la reivindicación 1 en el que el polipéptido es inmovilizado.
4. El método según la reivindicación 1 en el que se detecta la unión inmunoespecífica por inmunoprecipitación.
5. El método según la reivindicación 1 en el que la composición incluye por lo menos un polipéptido seleccionado de una proteína polimerasa de VIH-2 y una seleccionada de una proteína polimerasa de VIH-1.
6. El método según la reivindicación 1 en el que se detecta la unión inmunoespecífica entre el polipéptido o la proteína y el componente anticuerpo del fluido corporal por:
7. El método según la reivindicación 6 en la que el marcador incluye un enzima que es detectado por la adición del sustrato enzimático, un radiomarcador o un marcador fluorescente.
8. El método para determinar la presencia de anticuerpos de VIH-2 en un fluido corporal, incluyendo:

9. Una composición de polipéptidos, inmunorreactiva a anticuerpos de VIH, una de las siguientes secuencias de aminoácidos:

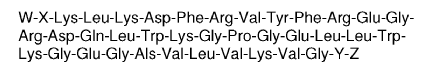
donde W es un H del grupo amino terminal NH2 del polipéptido, o uno o más aminoácidos adicionales ligados al grupo amino terminal NH2 del polipéptido, seleccionándose los aminoácidos adicionales para facilitar el acoplamiento del polipéptido a una proteína portadora o a un soporte; X está ausente, Cys-Gly-Gly; o Lys-Lys, Y está ausente, Cys- o uno o más aminoácidos se añaden para facilitar el acoplamiento; y Z es OH o NH2.
10. La composición de polipéptido según la reivindicación 9, donde el mencionado polipéptido tiene la fórmula (V) ROD 124 E1.
11. La composición de polipéptido según la reivindicación 9, donde el mencionado polipéptido tiene la fórmula (VII) ROD 124C2X.
12. La composición de polipéptido según la reivindicación 9, donde el mencionado polipéptido tiene la fórmula (VIII) ROD C1X.
13. La composición de polipéptido según la reivindicación 9, donde el mencionado polipéptido tiene la fórmula (IX) ROD C3X.
14. La composición del polipéptido de la reivindicación 9, donde el mencionado polipéptido tiene la fórmula (XI) ROD 124C65X.
15. Un kit de prueba para la determinación de la presencia de anticuerpos de VIH en un fluido corporal incluyendo un antígeno y reactivos auxiliares adecuados para su uso en la detección de la presencia de anticuerpos del antígeno en el mencionado fluido; donde el mencionado antígeno es el polipéptido de la reivindicación 9.
Patentes similares o relacionadas:
Uso de una proteína accesoria derivada del VIH para la reactivación del VIH latente, del 27 de Mayo de 2020, de Janssen Sciences Ireland Unlimited Company: Una proteína que consiste en los primeros 66 aminoácidos N-terminales (T66) de la proteína accesoria Tat derivada del virus de inmunodeficiencia humana […]
Sal de cloruro de Tat-NR2B9c, del 29 de Enero de 2020, de NoNO Inc: Una sal de cloruro de un péptido que es TAT-NR2B9c (SEQ ID NO:6) o difiere de TAT-NR2B9c en hasta 5 sustituciones, inserciones o deleciones de […]
Direccionamiento de factores de coagulación al TLT-1 en plaquetas activadas, del 23 de Octubre de 2019, de NOVO NORDISK HEALTH CARE AG: Una proteína procoagulante que comprende (i) al menos un factor de coagulación, que es un polipéptido de FVII o un polipéptido de FIX, unido covalentemente […]
Vector dual para la inhibición del virus de la inmunodeficiencia humana, del 16 de Octubre de 2019, de Calimmune Inc: Una célula hospedadora preparada transduciendo una célula hematopoyética con un vector de expresión lentiviral, comprendiendo el vector de expresión lentiviral una primera […]
Antígenos del virus de la inmunodeficiencia humana, vectores, composiciones y métodos de uso de los mismos, del 28 de Agosto de 2019, de Janssen Vaccines & Prevention B.V: Un ácido nucleico que codifica una proteína de la envoltura del VIH sintética que comprende la secuencia de aminoácidos de la SEQ ID NO: 8, o la SEQ ID […]
Procedimiento novedoso y composiciones, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Uno o más primeros polipéptidos inmunógenos para su uso en un procedimiento de generación de una respuesta inmunológica frente a Mycobacterium spp., en los […]
 Producción rápida de virus de título elevado, del 29 de Mayo de 2019, de ALEXION PHARMACEUTICALS, INC.: Procedimiento de producción de partículas virales, que comprende:
introducir de forma transitoria en una línea celular DF-1 una secuencia de nucleótidos […]
Producción rápida de virus de título elevado, del 29 de Mayo de 2019, de ALEXION PHARMACEUTICALS, INC.: Procedimiento de producción de partículas virales, que comprende:
introducir de forma transitoria en una línea celular DF-1 una secuencia de nucleótidos […]
Vectores y construcciones de liberación de antígenos de virus de la gripe, del 8 de Mayo de 2019, de ALTIMMUNE UK LIMITED: Una construcción de vector fluorocarbonado-antígeno de estructura CmFN--CyHx-(Sp)-R, donde m = 3 a 30, n <= 2m + 1, y = 0 a 15, x <= 2y, […]