Sales sólidas amorfas de Cobicistat (GS-9350).
Un sólido amorfo de una sal de un compuesto de fórmula (I):**Fórmula**
que no está revestido sobre una partícula de sílice,
en donde la sal es (i) una sal de citrato, tartrato, oxalato, fumarato, clorhidrato, lactato, fosfato, sulfato o malato, o (ii) una sal de xinafoato, tosilato, bromuro, dicloroacetato, naftalensulfato, alcanforsulfonato, nicotinato, hipurato, etanosulfonato, malonato, succinato, cetoglutarato, benzoato, besilato, edisilato, sacarinato, ascorbato o maleato.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2012/035871.
Solicitante: GILEAD SCIENCES, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 333 LAKESIDE DRIVE FOSTER CITY, CA 94404 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SUJINO,Keiko, KOZIARA,JOANNA M, LUONG,ANNE, YU,RICHARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/427 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › no condensados y conteniendo otros heterociclos.
- A61P31/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Antivirales.
- C07D277/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 277/00 Compuestos heterocíclicos que contienen ciclos de tiazol-1,3 o tiazol-1,3 hidrogenado. › Radicales sustituidos por átomos de nitrógeno.
PDF original: ES-2543923_T3.pdf
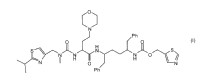
Fragmento de la descripción:
Sales sólidas amorfas de Cobicistat (GS-9350) Antecedentes de la invención
La solicitud de patente internacional con número de publicación WO 2008/010921 describe compuestos y composiciones farmacéuticas que mejoran la farmacocinética de un fármaco co-administrado inhibiendo la citocromo P450 monooxigenasa. Uno de dichos inhibidores es el compuesto de fórmula (I).
**(Ver fórmula)**Desafortunadamente, las propiedades de estado sólido del compuesto de fórmula (I) hacen que este sea difícil de manipular y procesar a gran escala. Por ejemplo, su baja temperatura de transición vitrea, su naturaleza higroscópica y su ausencia de cristalinidad, así como también su naturaleza que le impide fluir libremente, hacen que este sea particularmente difícil de procesar y formular (por ejemplo, como comprimido).
La solicitud de patente internacional con número de publicación WO 2009/135.179 analiza las dificultades asociadas con el procesado del compuesto (I) y describe la combinación del compuesto de fórmula (I) con las partículas sólidas portadoras con el fin de mejorar las propiedades físicas del material sólido resultante. Aunque el polvo resultante que fluye libremente tiene valores de carga elevados para el compuesto de fórmula (I), estabilidad física y química aceptables, propiedades de liberación rápida del fármaco y excelente aptitud de compresión, las partículas portadoras inertes contribuyen al peso y volumen total del sólido, de forma que se requiere significativamente más material en una formulación con el fin de lograr una dosis concreta del compuesto de fórmula (I). Por consiguiente, existe la necesidad de formas sólidas del compuesto de fórmula (I) que tengan las propiedades beneficiosas de los sólidos descritos en el documento WO 2009/135.179, pero que carezcan de las partículas portadoras que contribuyen al peso y volumen del sólido. El documento WO 2010/115.000 describe métodos e intermedios que son útiles para la preparación del compuesto de fórmula (la), definido a continuación.
Sumarlo de la Invención
La invención proporciona formas sólidas amorfas del compuesto de fórmula (I) que tienen muchas de las propiedades beneficiosas de los materiales analizados en la solicitud de patente internacional con número de publicación WO 2009/135.179, pero que carecen de las partículas portadoras sólidas.
Por consiguiente, en una realización, la invención proporciona un sólido amorfo de la invención que es un sólido amorfo de una sal de un compuesto de fórmula (I):
**(Ver fórmula)**que no está revestido sobre una partícula de sílice.
En otra realización de la invención se proporciona una composición farmacéutica que comprende un sólido amorfo de la invención. En otra realización, la invención proporciona un comprimido que comprende un sólido amorfo de la invención.
En otra realización, la invención proporciona una composición farmacéutica que comprende un sólido amorfo de la invención; fumarato de tenofovir y disoproxilo; emtricitabina y elvitegravir.
En otra realización, la invención proporciona sólidos amorfos y composiciones farmacéuticas para su uso en un método para inhibir la actividad de citocromo P-450 en un animal que comprende administrar un sólido amorfo de la invención o una composición farmacéutica de la invención al animal (por ejemplo, un mamífero tal como un ser humano).
En otra realización, la invención proporciona sólidos amorfos en combinación con una cantidad terapéuticamente eficaz de uno o más agentes terapéuticos seleccionados entre el grupo que consiste en compuestos inhibidores de VIH proteasa, inhibidores de transcriptasa inversa no nucleósido de VIH, inhibidores de transcriptasa inversa de nucleósido de VIH, inhibidores de transcriptasa inversa de nucleótido de VIH, inhibidores de VIH integrasa e inhibidores de CR5, para su uso en un método para el tratamiento de infección por VIH.
En otra realización, la invención proporciona un sólido amorfo de la invención para su uso en terapia médica.
En otra realización, la invención proporciona un sólido amorfo de la invención para su uso en el tratamiento profiláctico o terapéutico de una infección por VIH.
En otra realización, la invención proporciona un sólido amorfo de la invención para su uso en la inhibición de la actividad de citocromo P-450.
En otra realización, la invención proporciona un sólido amorfo de la invención para su uso en la preparación de un medicamento para el tratamiento de infección por VIH en un mamífero.
En otra realización, la invención proporciona un sólido amorfo de la invención para su uso en la preparación de un medicamento para inhibir la actividad de citocromo P-450 en un animal.
En otra realización, la invención proporciona un método como se describe en la reivindicación 13 que comprende: a) poner en contacto un compuesto de fórmula (I) con un ácido requerido en un primer disolvente, y b) añadir un segundo disolvente en condiciones que permitan la formación de una sal.
En otra realización, la invención proporciona un método como se describe en la reivindicación 14 que comprende, secado por pulverización de una solución que comprende un compuesto de fórmula (I) y un ácido requerido en condiciones que permitan la formación de una sal.
También se divulga un método que comprende añadir una solución de tolueno de un compuesto de fórmula (I):
**(Ver fórmula)**a heptanos para dar un sólido amorfo.
En otra realización, la invención proporciona un método para la preparación de una composición farmacéutica que comprende combinar el sólido amorfo de la invención y un excipiente farmacéuticamente aceptable para proporcionar la composición farmacéutica.
En otra realización, la invención proporciona un método para la preparación de una composición farmacéutica que comprende: combinar un sólido amorfo de la invención, fumarato de tenofovir y disoproxilo, emtricitabina, y elvitegravir, para proporcionar la composición farmacéutica.
También se divulga un material preparado por un método descrito en la presente memoria.
Descripción detaiiada de ia invención
Los expertos en la materia apreciarán que los compuestos de fórmula (I) pueden existir y se pueden aislar en formas racémicas y ópticamente activas. Algunos compuestos pueden exhibir polimorfismo. Debe entenderse que la presente invención engloba cualquier forma racémica, ópticamente activa, polimórfica o estereoisomérica, o sus mezclas, de un compuesto de fórmula (I), que posea propiedades útiles descritas en la presente memoria, conociéndose bien en la técnica cómo preparar formas ópticamente activas (por ejemplo, por resolución de la forma
racémica por técnicas de cristalización, por síntesis a partir de materiales de partida ópticamente activos, por síntesis quiral, o por separación cromatogràfica usando una fase estacionaria quiral).
Un "sólido amorfo", según se usa en la presente memoria, incluye materiales sólidos que no tienen un patrón tridimensional periódico. Por ejemplo, se pueden identificar sólidos amorfos que carecen de cristalinidad por análisis XRPD según se ¡lustra en la presente memoria. En una realización, un sólido amorfo es una forma manipulable que fluye libremente (por ejemplo, un polvo o sólido). En otra realización, los sólidos amorfos excluyen materiales vitreos, de caucho y de goma que incluyen los materiales de fórmula I preparados en la Solicitud de Patente Internacional con Número de Publicación WO 2008/010921.
En una realización, la invención proporciona composiciones farmacéuticas que comprenden el sólido amorfo de la invención que se puede administrar a un hospedador mamífero, tal como un paciente humano, en varias formas adaptadas a la vía de administración escogida (por ejemplo, por vía oral).
Las composiciones de la invención pueden incluir uno o más excipientes farmacéuticamente aceptables. Los excipientes incluyen, pero sin limitación, sustancias que pueden servir como vehículo o medio para un sólido amorfo de la invención (por ejemplo, un diluyente o un portador). Pueden incluirse en cápsulas de gelatina de cubierta dura o blanda, se pueden comprimir para dar lugar a comprimidos, o se pueden incorporar directamente al alimento de la dieta del paciente. Para administración terapéutica oral, se puede combinar el compuesto activo con uno o más excipientes y usarse en forma de comprimidos ¡ngeribles, comprimidos bucales, trociscos, cápsulas, elixires, suspensiones, jarabes, obleas y similares. Normalmente, dichas preparaciones y composiciones contendrán al menos un 0,1 % de compuesto activo.... [Seguir leyendo]
Reivindicaciones:
1. Un sólido amorfo de una sal de un compuesto de fórmula (I):
**(Ver fórmula)** **(Ver fórmula)**1.
**(Ver fórmula)**que no está revestido sobre una partícula de sílice, en donde la sal es (I) una sal de cltrato, tartrato, oxalato, fumarato, clorhidrato, lactato, fosfato, sulfato o malato, o (¡I) una sal de xlnafoato, tosllato, bromuro, dlcloroacetato, naftalensulfato, alcanforsulfonato, nlcotlnato, hlpurato, etanosulfonato, malonato, succlnato, cetoglutarato, benzoato, besllato, edlsllato, sacarlnato, ascorbato o maleato.
2. El sólido amorfo de la reivindicación 1 que tiene una temperatura de transición vitrea de al menos aproximadamente 40 -C, opclonalmente de al menos aproximadamente 50 -C.
3. El sólido amorfo de una cualquiera de las reivindicaciones 1-2, en el que el compuesto de fórmula (I) es un compuesto de fórmula (la):
4. Una composición farmacéutica que comprende un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1-3 y un excipiente farmacéuticamente aceptable.
5. Un comprimido que comprende un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1-3.
6. Una composición farmacéutica que comprende un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1 -3; fumarato de tenofovir y dlsoproxllo; emtrlcltablna y elvltegravlr.
7. Un sólido amorfo como se describe en cualquiera de las reivindicaciones 1-3, para su uso en un método para Inhibir la actividad de cltocromo P-450 en un animal.
8. Un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1-3 en combinación con una cantidad terapéuticamente eficaz de uno o más agentes terapéuticos seleccionados entre el grupo que consiste en compuestos Inhibidores proteasa de VIH, Inhibidores de transcrlptasa Inversa no nucleósldo de VIH, inhibidores de transcrlptasa Inversa de nucleósldo de VIH, Inhibidores de transcrlptasa Inversa de nucleótldo de VIH, Inhibidores ¡ntegrasa de VIH e Inhibidores de CCR5, para su uso en un método para el tratamiento de una Infección por VIH.
9. Un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1-3, para su uso en terapia médica.
10. Un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1-3, para su uso en el tratamiento profiláctico o terapéutico de una Infección por VIH.
11. Un sólido amorfo como se describe en una cualquiera de las reivindicaciones 1 -3, para su uso en la preparación de un medicamento para el tratamiento de Infección por VIH en un mamífero.
12. Un método para la preparación de un sólido amorfo de una sal de un compuesto de fórmula (I) de acuerdo con la reivindicación 1 que comprende: a) poner en contacto un compuesto de fórmula (I):
**(Ver fórmula)** **(Ver fórmula)**con un ácido requerido en un primer disolvente, y b) añadir un segundo disolvente en condiciones que permitan la formación de una sal.
5 13. Un método para la preparación de un sólido amorfo de una sal de un compuesto de fórmula (I) de acuerdo con la
reivindicación 1 que comprende secar por pulverización una solución que comprende un compuesto de fórmula (I):
**(Ver fórmula)**y un ácido requerido en condiciones que permitan la formación de una sal.
14. Un método para la preparación de una composición farmacéutica que comprende combinar el sólido amorfo que se describe en una cualquiera de las reivindicaciones 1-3 y un excipiente farmacéuticamente aceptable para proporcionar la composición farmacéutica.
15 15. Un método de preparación de una composición farmacéutica que comprende; combinar un sólido amorfo como
se describe en una cualquiera de las reivindicaciones 1-3, fumarato de tenofovir y disoproxilo, emtñcitabina y elvltegravlr para proporcionar la composición farmacéutica.
Patentes similares o relacionadas:
Composiciones y métodos anti-HCMV, del 22 de Julio de 2020, de Evrys Bio, LLC: Una composición que comprende un compuesto de la Fórmula I: **(Ver fórmula)** en donde: Ar es **(Ver fórmula)** en donde cada anillo cíclico de 5 o 6 miembros […]
Productos terapéuticos basados en la lantionina sintetasa 2 tipo C, del 15 de Julio de 2020, de LANDOS BIOPHARMA, INC: Un compuesto de la fórmula: **(Ver fórmula)** o una sal o éster farmacéuticamente aceptable de este, en donde: Q es piperazina-1,4-diilo; […]
Procedimientos de tratamiento del cáncer usando antagonistas de unión al eje de PD-1 e inhibidores de TIGIT, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo antagonista anti-PD-L1 o fragmento de unión a antígeno del mismo y un anticuerpo antagonista anti-TIGIT o fragmento de unión a antígeno del mismo para su uso […]
Macrocíclico y composición que comprende el mismo, del 8 de Julio de 2020, de Shenzhen TargetRx, Inc: Un compuesto macrocíclico sustituido, que es un compuesto macrocíclico representado por la fórmula (I), o una forma cristalina, una sal farmacéuticamente […]
Vectores de CMVH y CMVRh recombinantes que codifican un antígeno heterólogo aislado de un virus Paramyxoviridae y usos de los mismos, del 1 de Julio de 2020, de Oregon Health & Science University: Un vector de CMVRh o CMVH recombinante que comprende una secuencia de ácido nucleico que codifica un antígeno heterólogo, en el que el antígeno […]
Derivados de oxadiazepinona y su uso en el tratamiento de infecciones por hepatitis B, del 17 de Junio de 2020, de Novira Therapeutics Inc: Un compuesto de Fórmula IA: **(Ver fórmula)** O una sal farmacéuticamente aceptable del mismo, en el que A es N o C(H); R1 es H, alquilo […]
Extracto de Petasites y composición para tratar infecciones víricas, del 10 de Junio de 2020, de MAX-ZELLER SOHNE AG: Extracto de Petasites para usar en el tratamiento de una enfermedad vírica de un mamífero, preferentemente humana.
Compuestos de tiazolida para tratar infecciones virales, del 10 de Junio de 2020, de ROMARK LABORATORIES, L.C.: Composición farmacéutica que comprende al menos uno de nitazoxanida o tizoxanida o sal farmacéuticamente aceptable de los mismos para su […]