Composición que comprende albúmina para su utilización en el tratamiento de Esclerosis Lateral Amiotrófica (ELA) mediante recambio plasmático.
Composición que comprende albúmina para su utilización en el tratamiento de Esclerosis Lateral Amiotrófica (ELA) mediante recambio plasmático.
La presente invención se refiere a una composición que comprende albúmina, más específicamente albúmina al 5% (p/v), para su utilización en el tratamiento de la Esclerosis Lateral Amiotrófica mediante recambio plasmático.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201530074.
Solicitante: GRIFOLS WORLDWIDE OPERATIONS LIMITED.
Nacionalidad solicitante: Irlanda.
Dirección: Embassy House, Ballsbridge Dublin 4 IRLANDA.
Inventor/es: JORBA RIBES,JAVIER, PÁEZ REGADERA,Antonio Manuel.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/38 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Albúminas.
- A61P25/28 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
Fragmento de la descripción:
Composición que comprende albúmina para su utilización en el tratamiento de Esclerosis Lateral Amiotrófica (ELA) mediante recambio plasmático La presente invención se refiere a una composición que comprende albúmina, más específicamente albúmina al 5% (p/v) , para su utilización en el tratamiento de Esclerosis Lateral Amiotrófica mediante recambio plasmático.
La Esclerosis Lateral Amiotrófica (en adelante ELA) es un trastorno neuronal motor con una incidencia anual de aproximadamente 3 por cada 100.000 habitantes. La ELA es una enfermedad neurológica degenerativa crónica, progresiva y fatal, que afecta a las neuronas motoras encargadas de controlar el movimiento de los músculos voluntarios. En el 90% de los casos, la enfermedad ocurre de forma esporádica y su causa es desconocida. A pesar de haberse realizado extensos estudios sobre esta enfermedad, su patogénesis sigue siendo desconocida y no se ha encontrado un tratamiento eficaz.
Tal como se mencionó anteriormente, la ELA es habitualmente progresiva, con parálisis motora superior e inferior que conduce a la muerte en un promedio de tres años desde el comienzo de la misma. Por lo general, durante el curso de la enfermedad se crean problemas médicos difíciles y angustiosos, lo que ha estimulado el uso de una gran variedad de tratamientos tales como fármacos tóxicos, veneno de cobra inactivado y plasmaféresis, entre otros.
La plasmaféresis es un procedimiento médico común en el que se separa el plasma de la sangre total. Se ha utilizado para el tratamiento de pacientes que sufren de diferentes enfermedades crónicas. Una vez que el plasma es separado de las células sanguíneas, las células se pueden retornar al paciente junto con fluidos de reemplazo o sin los mismos. Cuando se tratan pacientes mediante plasmaféresis terapéutica, se coloca un catéter en una vena mayor, tal como por ejemplo en el brazo, y se coloca un segundo catéter en otra vena, por ejemplo, en el pie o en la mano. A continuación, la sangre sale del cuerpo del paciente a través del catéter y se envía a un separador, donde el plasma es separado de las células sanguíneas. La sangre sin plasma y, opcionalmente, junto con el fluido de reemplazo es retornada al paciente a través del segundo catéter. En lugar de dos catéteres periféricos, también se puede utilizar un catéter de doble vía, central o periférico.
P201 530074
Hasta la fecha, el tratamiento de ELA mediante plasmaféresis ha resultado ineficaz, según los reportes de la literatura científica y médica. Por ejemplo, Silani y otros (Silani, V., Scarlato, G., Valli, G. and Marconi, M. "Plasma Exchange Innefective in Amyotrophic Lateral Sclerosis" Arch. NeuroJ. (1980) Vol. 37: 511-513) informaron que un recambio plasmático con plasma congelado fresco y solución salina en cuatro pacientes con ELA no modificó el curso clínico de la enfermedad, en un estudio de seis meses de duración. Por otra parte, Monstad y otros (Monstad, l., Dale, l., Petlund, C.F. and Sjaastad, O. "Plasmapheresis in Motor Neuron Disease (MND) , a control study". 1979 (Resumen en Acta NeuroJ. Scand. 1978) informaron que un recambio plasmático en 7 pacientes que sufrían de Enfermedad Neuronal Motora (EMN) , entre las que se incluye la ELA, no resultó en diferencias significativas en el curso de la enfermedad entre los grupos de control y los tratados. No se menciona qué fluido de reemplazamiento fue utilizado durante el tratamiento de recambio plasmático.
Cabe señalar que el uso del recambio plasmático en el tratamiento de ELA está considerado como de categoría IV (la más baja) en las Directrices sobre el Uso de Aféresis Terapéutica en la Práctica Clínica de la Sociedad Americana de Aféresis (ASFA) (Schwartz, J., Winters,
J.L., Padmanabhan, A., Balogun, R.A., Delaney, M., Linenberger, M.L., Szczepiorkowski, Z.M., Williams, M.E., Wu, Y., Shaz S.H. "Guidelines on the use of therapeutic apheresis in clinical practice-evidence-based approach from the Writing Committee of the American Soeiety for Apheresis: the sixth speeial issue" J. Glin. Apher. 2013 Jul; 28 (3) :145-284) . La categoría IV se refiere a trastornos en los que la evidencia publicada demuestra o sugiere que la aféresis es ineficaz o dañina. Lo anterior coincide con los resultados publicados hasta el momento.
Además, Kelemen y otros (Kelemen, J., Hedlund, W., Orlin, J.B., Berkman, E.M. and Munsat
T.L. "Plasmapheresis with immunosupression in Amyotrophic Lateral Sclerosis". Arch. Neurol. (1983) , Vol. 40: 752-753.) informaron del uso de recambio plasmático con albúmina al 5% en combinación con un tratamiento de inmunosupresión para el tratamiento de ELA. Una vez más, con dicho tratamiento no se observó en ninguno de los 4 pacientes estudiados ningún efecto beneficioso sobre la enfermedad, ni ninguna mejora clínica de la misma. Este hecho no hizo más que confirmar los resultados obtenidos con anterioridad sobre la ineficacia del recambio plasmático para el tratamiento de ELA.
Sin embargo, los presentes inventores han descubierto, sorprendentemente, que mediante el uso de una composición que comprende albúmina humana en un tratamiento específico P201 530074
mediante recambio plasmático sin la utilización de ningún tratamiento inmunosupresor, es posible obtener resultados que pueden considerarse beneficiosos para el tratamiento de ELA. Con estos re sultados, se supera un prejuicio científico relacionado con la falta de eficacia del recambio plasmático en el tratamiento de ELA; aunque hubo intentos anteriores, no se conoce que ninguno haya finalizado con éxito, consiguiendo en realidad un resultado inesperado.
Por lo tanto, un objetivo de la presente invención es dar a conocer el uso de una composición que comprende albúmina para la fabricación de un medicamento para el tratamiento de la Esclerosis Lateral Amiotrófica. Preferentemente, la concentración de la albúmina en dicha composición es de 5% (p/v) . La albúmina puede ser tanto recombinante como purificada a partir de plasma humano.
En la presente invención, el tratamiento con la composición que comprende albúmina se realiza preferentemente mediante recambio plasmático; es decir, que dicha composición que comprende albúmina se utiliza como líquido de reemplazo, que será retornado al paciente junto con las células sanguíneas, que han sido previamente separadas del plasma mediante plasmaféresis. Al paciente se le extrae, por lo general, un volumen de plasma determinado y el recambio plasmático con la composición que comprende albúmina se realiza con un volumen de dicha composición equivalente a aproximadamente el 100% del volumen de plasma extraído del paciente. Un experto en la materia entiende que pequeñas variaciones de aproximadamente ± 10% de este volumen quedarán comprendidas en el alcance de la presente invención.
Una diferencia fundamental del uso de una composición que comprende albúmina para el tratamiento de ELA, según la presente invención, es que en dicho tratamiento no es necesario el uso de inmunosupresores antes, durante o después de terminar dicho tratamiento. En la técnica anterior se ha relacionado la ELA con anormalidades del sistema inmunitario tales como anormalidades de antígenos de superficie, de linfocitos T, y de migración de macrófagos (Kelemen J. y otros, anterior) , lo que pudiera sugerir el uso de un tratamiento inmunosupresor de forma concomitante con cualquier tratamiento de la ELA. Sin embargo, en el presente documento se demuestra que con el tratamiento de la presente invención no es necesaria la utilización de inmunosupresores para obtener resultados satisfactorios para el tratamiento de la ELA.
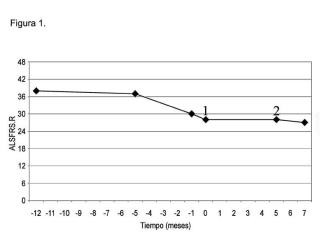
En el tratamiento de la presente invención, el recambio plasmático utilizando la composición que comprende albúmina como fluido de reemplazo, se realiza con una frecuencia de tres veces por semana las dos primeras semanas y una vez por semana durante las siguientes doce semanas, durante un periodo total 14 semanas. Durante el tiempo que dura el tratamiento, los pacientes pueden experimentar una tendencia, como minimo, a la estabilización de la enfermedad; es decir, al tratarse de una enfermedad cuya progresión es rápida y gradual una vez que comienza la misma, lograr una estabilización de la progresión de la misma durante el tiempo que dura el tratamiento, puede considerarse muy positiva.
Otro objetivo de la presente invención es dar a conocer una composición que comprende albúmina para el tratamiento de la Esclerosis Lateral Amiotrófica. Preferentemente, la concentración de la albúmina en dicha composición es de 5% (p/v) . La albúmina puede ser tanto recombinante como purificada a partir de plasma humano.
En la presente invención, el tratamiento con la...
Reivindicaciones:
1. Uso de una composición que comprende albúmina para la fabricación de un medicamento para el tratamiento de la Esclerosis Lateral Amiotrófica.
2. Uso, según la reivindicación 1, caracterizado porque la concentración de albúmina es de 5% (p/v) .
3. Uso, según la reivindicación 1 ó 2, caracterizado porque la albúmina es recombinante o 10 purificada a partir de plasma humano.
4. Uso, según cualquiera de las reivindicaciones anteriores, caracterizado porque el tratamiento se realiza mediante recambio plasmático.
5. Uso, según la reivindicación 4, caracterizado porque el recambio plasmático se realiza con un volumen equivalente a aproximadamente el 100% del volumen de plasma extraído del paciente.
6. Uso, según la reivindicación 4 ó 5, caracterizado porque el recambio plasmático se realiza con una frecuencia de tres veces por semana las dos primeras semanas y una vez por semana durante las siguientes doce semanas.
7. Uso, según cualquiera de las reivindicaciones anteriores, caracterizado porque el tratamiento se realiza sin la utilización de inmunosupresores.
8. Composición que comprende albúmina para su uso en el tratamiento de la Esclerosis Lateral Amiotrófica.
9. Composición para su uso, según la reivindicación 8, caracterizada porque la 30 concentración de albúmina es de 5% (p/v) .
10. Composición para su uso, según la reivindicación 8 Ó 9, caracterizada porque la albúmina es recombinante o purificada a partir de plasma humano.
11. Composición para su uso, según cualquiera de las reivindicaciones 8-10, caracterizada porque el tratamiento se realiza mediante recambio plasmático.
12. Composición para su uso, según la reivindicación 11, caracterizada porque el recambio plasmático se realiza con un volumen equivalente a aproximadamente el 100% del volumen de plasma extraído del paciente.
13. Composición para su uso, según la reivindicación 11 ó 12, caracterizada porque el recambio plasmático se realiza con una frecuencia de tres veces por semana las dos primeras semanas y una vez por semana durante las siguientes doce semanas.
14. Composición para su uso, según cualquiera de las reivindicaciones 8-13, caracterizada porque el tratamiento se realiza sin la utilización de inmunosupresores.
Patentes similares o relacionadas:
Tratamientos de combinación que comprenden imidazopirazinonas para el tratamiento de trastornos psiquiátricos y/o cognitivos, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de Fórmula (I) **(Ver fórmula)** en donde n es 0 o 1; q es 0 o 1; R1 se selecciona del grupo que consiste en bencilo, indanilo, indolina y heteroarilos […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composición farmacéutica basada en nanoestructura de grafeno para prevenir o tratar enfermedades neurodegenerativas, del 22 de Julio de 2020, de Seoul National University R & DB Foundation: Una composición farmacéutica para su uso en la prevención o el tratamiento de enfermedades neurodegenerativas, que comprende puntos cuánticos de grafeno como […]
Composición para el tratamiento de enfermedades isquémicas o trastornos inflamatorios neurogénicos, que contienen el secretoma de células progenitoras neurales como ingrediente activo, del 22 de Julio de 2020, de S-BIOMEDICS: Una composición para uso en el tratamiento de enfermedad cerebrovascular isquémica, cardiopatía isquémica, infarto de miocardio, enfermedad de Alzheimer, enfermedad […]
Triple combinación de antagonistas del receptor 5-HT6 puros, inhibidores de la acetilcolinesterasa y antagonista del receptor NMDA, del 15 de Julio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un antagonista del receptor 5-HT6 puro, un inhibidor de la acetilcolinesterasa y un antagonista del receptor NMDA, en el que el antagonista […]
Antagonistas del receptor p2x7 derivados de N-[2-(4-fenoxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida y N-[2-(4-benciloxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida sustituidas, del 15 de Julio de 2020, de AXXAM S.P.A: Un compuesto de la siguiente fórmula (I) o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** incluyendo cualquier forma estereoquímicamente […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]