Tratamiento de una septicemia con 5-etil-1-fenil-2(1H)-piridona.
Una composición para su uso en el tratamiento de una septicemia en un mamífero, comprendiendo la composición 5-etil-1-fenil-2-(1H)-piridona.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/036529.
Solicitante: Solanan, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9400 N. Central Expressway, Suite 305 Dallas, TX 75231 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MARGOLIN, SOLOMON B., GIRI,SHRI N, GOUX,WARREN J.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/4418 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo un carbociclo unido directamente al heterociclo, p. ej. ciproheptadina.
PDF original: ES-2509143_T3.pdf

Fragmento de la descripción:
Tratamiento de una septicemia con 5-etil-1-fenil-2 (1H) -piridona
CAMPO TÉCNICO
La presente invención se refiere a un compuesto de piridona, 5-etil-1-fenil-2- (1H) -piridona, a nuevos procedimientos para su síntesis y purificación, a composiciones farmacéuticas que lo contienen y a su uso en el tratamiento de una septicemia.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
La fig. 1 es una representación esquemática de la síntesis de la 5-etil-1-fenil-2- (1H) -piridona ("5-EPP") .
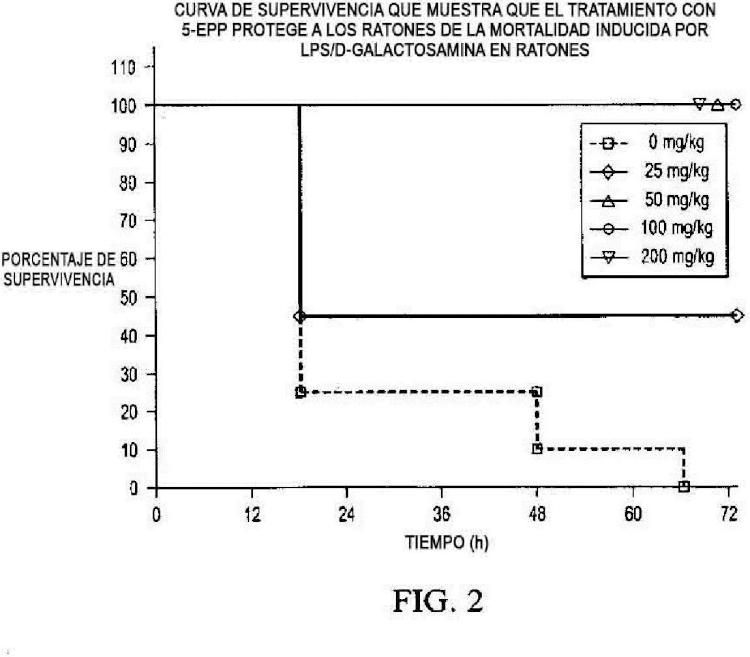
La fig. 2 es una gráfica que representa una curva de supervivencia para ratones en modelo de septicemia por LPS/D-galactosamina tratada con 5-etil-1-fenil-2- (1H) -piridona (5-EPP) .
La fig. 3 es un dibujo de la 5-etil-1-fenil-2- (1H) -piridona ("5-EPP") .
DESCRIPCIÓN DETALLADA
En la presente memoria descriptiva se describe un compuesto, la 5-etil-1-fenil-2- (1H) -piridona, y 25 nuevos procedimientos para prepararlo, purificarlo, emplearlo en una composición farmacéutica para el tratamiento de una septicemia y usarlo.
El documento US-2008/025.986 (Ozes y col.) desvela procedimientos para tratar trastornos mediados por el TNF. El documento US-6.300.349 (Margolin) desvela procedimientos para la inhibición de TNF-α.
Aunque la estructura química de la 5-etil-1-fenil-2- (1H) -piridona ha sido especificada en las patentes y la literatura especializada anterior, hasta ahora no se conoce la descripción de una forma eficaz de preparar y purificar este compuesto.
A continuación se proporcionan procedimientos de síntesis eficaces para la 5-etil-1-fenil-2- (1H) piridona a partir de un compuesto de partida, la 3-etilpiridina.
En la fig. 1 se proporciona un primer esquema de reacción útil para la síntesis de la 5-etil-1-fenil-2 (1H) -piridona.
En dicho primer esquema de reacción, los autores de la invención han encontrado que la 5-etil-1-fenil2- (1H) -piridona puede prepararse a partir de la 3-etilpiridina (disponible en Sigma-Aldrich Corporation, St. Louis, MO) que se hace reaccionar con NaNH2 en presencia de una pequeña cantidad de ácido oleico como catalizador para acelerar la reacción. Se proporciona un esquema general de la reacción para obtener un isómero de 2-amino-5
etilpiridina a partir de 3-etilpiridina en la patente de EE.UU. 5.003.069 para McGill y col., "Reacción de Chichibabinâ??, en el ejemplo 12. En esta reacción la 3-etilpiridina (I) se convierte en 2-amino-5-etilpiridina (II) así como en 2-amino3-etilpiridina (III) .
** (Ver fórmula) **
Después de destilación repetida, se obtiene el isómero deseado, 2-amino-5-etilpiridina (estructura II,
anterior) .
Los autores de la invención han encontrado que la 2-amino-5-etilpiridina puede convertirse en el
producto deseado, 5-etil-1-fenil-2- (1H) -piridona. En el procedimiento de la invención, primero se oxida el isómero 2amino-5-etilpiridina para formar 5-etil-2-piridona.
En el procedimiento de oxidación preferido de la invención, se disuelve 2-amino-5-etilpiridina en ácido sulfúrico al 20 % (H2SO4, p/v) y se enfría detenidamente en un baño de hielo. A continuación se añade el reactivo 10 preferido, una solución de nitrito de sodio (NaNO2, p/v, 1, 2 equivalentes en moles) durante 4-5 horas para oxidar la 2-amino-5-etilpiridina en 5-etil-2-piridona.
Después de la oxidación, se añade Na2CO3 (2, 0 equivalentes en moles) a la mezcla de reacción hasta que se alcanza un pH = 8-8, 5, y se obtiene una mezcla de dos fases, con una fase orgánica superior de color 15 amarillo oscuro y una fase acuosa inferior de color amarillo claro.
La fase acuosa se extrae con cloruro de metileno (CH2Cl2) y se guarda en reserva con la fase orgánica. Después del secado, se obtiene un sólido amarillo claro que es la 5-etil-2-piridona.
A continuación se lleva a cabo una reacción de sustitución con el fin de sustituir un grupo fenilo en el N del anillo de piridona de la 5-etil-2-piridona por hidrógeno. La 5-etil-2-piridona se hace reaccionar preferentemente en presencia de un catalizador de cobre-cinc y carbonato de potasio con un halobenceno. Preferentemente el halobenceno se selecciona entre yodobenceno y bromobenceno. Con la máxima preferencia, se usa bromobenceno. Se forma así la 5-etil-1-fenil-2- (1H) -piridona y estará en la mezcla de reacción.
El procedimiento de la invención incluye purificación de la 5-etil-1-fenil-2- (1H) -piridona a partir de la mezcla de reacción. Después de la terminación de la reacción, según se comprobó por cromatografía en capa fina (TLC) , el bromobenceno sin reaccionar se eliminó por destilación en alto vacío.
Se extrajo el resto de la solución con CH2Cl2. Se filtró el extracto al vacío a través de una columna corta de Celita para eliminar todas las partículas pequeñas.
Se trató el extracto anterior con carbón activado y se mantuvo en ebullición durante 10-15 minutos, a continuación se enfrió a temperatura ambiente antes de eliminar el carbón por filtrado al vacío a través de una 35 segunda columna de Celita.
Se redujo el volumen de filtrado por evaporación rotatoria. Se secó el concentrado oleoso resultante a temperatura ambiente para producir un sólido marrón oscuro que contenía 5-etil-1-fenil-2- (1H) -piridona al 75 %.
Se disolvió primero el sólido marrón oscuro en acetato de etilo caliente y a continuación se llevó a ebullición. Se añadió hexano a la solución en ebullición y se agitó de forma continua para separar la fase superior (rica en hexano) de la fase inferior (acetato de etilo) .
Se vertió la fase superior en un vaso de precipitado y se dejó enfriar y asentarse primero, y a 45 continuación se transfirió a una cubeta con recubrimiento de Teflón.
Después de evaporación y enfriamiento, se formaron cristales blancos de 5-etil-1-fenil-2- (1H) -piridona en toda la cubeta.
Los cristales blancos purificados después del secado produjeron un fino polvo cristalino blanco con un punto de fusión de 57-59 º C.
El análisis por HPCL de fase inversa y RMN reveló que el polvo contenía > 99 % de 5-etil-1-fenil-2 (1H) -piridona, 55 [0024] En un segundo esquema de reacción, se ha desarrollado también un procedimiento de síntesis de una etapa para preparar el compuesto 5-etil-1-fenil-2- (1H) -piridona. El primer esquema de reacción expuesto anteriormente implica un procedimiento en tres etapas.
** (Ver fórmula) **
Los autores de la invención han encontrado que la 5-etil-1-fenil-2- (1H) -piridona puede prepararse a partir del material de partida, 5-etil-2-piridona (J & W Pharlab LLC, Levitton, PA) . Se hace reaccionar 5-etil-2-piridona 5 con bromobenceno en presencia de un catalizador de Cu-Zn en una capa de argón para producir 5-etil-1-fenil-2 (1H) -piridona.
Preparación del catalizador: se preparó un catalizador de cobre-cinc (Cu-Zn) inmediatamente antes de la reacción anterior. En primer lugar se lavó polvo de Zn finamente dividido (1, 0 equivalentes en moles) de dos a 10 cuatro veces con ácido clorhídrico al 3 % hasta que la solución se hizo transparente y se desarrolló gas de hidrógeno. A continuación se lavó el cinc dos veces con agua 18 M-ohm. Seguidamente, se añadió una solución acuosa de CuSO4 al 2 % al polvo de Zn recién lavado con ácido y se mezcló la solución por medio de un agitador magnético hasta que se volvió incolora. Se decantó el sobrenadante incoloro y se añadió un segundo volumen de solución de CuSO4 al 2 % al polvo de Zn. Se repitió este procedimiento varias veces hasta que la solución de CuSO4
permaneció azul y el catalizador de Cu-Zn se convirtió en un polvo rojo. Finalmente, se deslavó el catalizador de Cu-Zn completado 3-4 veces con agua, seguido por 2-3 deslavados con metanol. A continuación se secó el polvo resultante de color rojo oscuro a bajo vacío durante al menos 2 horas a 40-50 º C, [0027] La reacción química es como sigue: se combinaron 5-etil-2-piridona (⥠96 %, 1, 0 equivalentes en moles) , y carbonato de potasio (1, 2 equivalentes en moles) en un matraz de reacción de 5 litros montado en una manta calefactora. Seguidamente, se añadieron el bromobenceno (2, 5 equivalentes en moles) y el catalizador de Cu-Zn (0, 05 equivalentes en moles) al matraz. Se fijó un aparato de agitación y se limpió el matraz de reacción con gas argón durante varios minutos. Después de ajustar el aparato de agitación, se calentó la mezcla durante 60-90 min hasta que se sometió a reflujo lentamente con argón durante 48-72 horas. La formación de un sólido blanquecino en el lado del matraz indicó el inicio de la reacción. El avance de la reacción se verificó por cromatografía en capa fina (TLC)... [Seguir leyendo]
Reivindicaciones:
1. Una composición para su uso en el tratamiento de una septicemia en un mamífero, comprendiendo la composición 5-etil-1-fenil-2- (1H) -piridona. 5
2. Una composición para su uso según la reivindicación 1, en la que el tratamiento de una septicemia comprende la administración de una cantidad eficaz de 5-etil-1-fenil-2- (1H) -piridona a un mamífero con necesidad de dicho tratamiento, en la que dicha cantidad eficaz es inyectada en dicho mamífero por medio de una vía seleccionada entre las vías intravenosa, intramuscular, intraperitoneal y oral.
3. Una composición para su uso según la reivindicación 2, en la que dicha vía se selecciona entre inyección intravenosa e infusión intravenosa.
4. Una composición para su uso según la reivindicación 2, en la que dicha cantidad eficaz es 15 aproximadamente de 5 mg/kg de peso corporal a 200 mg/kg de peso corporal al día de dicho mamífero.
5. Una composición para su uso según la reivindicación 4, en la que dicha cantidad eficaz se administra en una dosis única o en dosis múltiples.
6. Un producto farmacéutico para su uso en el tratamiento de una septicemia, que comprende 5-etil-1fenil-2- (1H) -piridona purificada.
7. El producto farmacéutico para su uso según la reivindicación 6, que comprende además un vehículo farmacéutico. 25
8. El producto farmacéutico para su uso según la reivindicación 7, en el que dicha 5-etil-1-fenil-2- (1H) piridona purificada se disuelve en un vehículo farmacéutico y es adecuada para su administración por medio de una vía seleccionada entre inyección intramuscular, inyección intraperitoneal, inyección intravenosa e infusión intravenosa en un mamífero.
9. El producto farmacéutico para su uso según la reivindicación 8 en el que dicho vehículo se selecciona entre suero salino, propilenglicol y combinaciones de los mismos.
10. El producto farmacéutico para su uso según la reivindicación 9, en el que dicho vehículo es suero
salino isotónico y dicha 5-etil-1-fenil-2- (1H) -piridona tiene una concentración de 20 mg/mL o menos y es incolora a temperatura ambiente.
11. El producto farmacéutico para su uso según la reivindicación 7, que comprende 5-etil-1-fenil-2- (1H) piridona purificada y un diluyente en forma de suero salino, en el que la concentración de dicha solución es 20
mg/mL, y en el que dicha solución se caracteriza por ser transparente a temperatura ambiente sin ningún precipitado visible.
12. El producto farmacéutico para su uso según la reivindicación 7, en el que dicho vehículo es suero salino; y en el que la concentración de 5-etil-1-fenil-2- (1H) -piridona es aproximadamente 20 mg/ml. 45
13. El producto farmacéutico destinado a su uso según la reivindicación 7, que comprende una solución que es incolora y no precipita a temperatura ambiente, y que se prepara según las etapas de: añadir una cantidad de 5-etil-1-fenil-2- (1H) -piridona sólida a un tubo hecho de un material seleccionado entre el grupo que consiste en polipropileno y poliestireno; añadir una cantidad de diluyente en forma de suero salino a dicha 5-etil-1-fenil-2- (1H)
piridona sólida hasta el volumen final deseado; disolver la 5-etil-1-fenil-2- (1H) -piridona por mezclado intermitente con un agitador vorticial, calentar dicho tubo a una temperatura de entre 40 º C y 45 º C y aplicar sonicación (3 x 15 min) a dicho tubo hasta que tiene lugar la disolución completa; permitir que dicha solución regrese a la temperatura ambiente a la cual se forma dicha solución de 5-etil-1-fenil-2- (1H) -piridona que es incolora y no precipita a temperatura ambiente; en el que la concentración de dicha 5-etil-1-fenil-2- (1H) -piridona es 20 mg/ml.
14. La composición para su uso según cualquiera de las reivindicaciones 1 a 5, o el producto farmacéutico para su uso según cualquiera de las reivindicaciones 6 a 13, en la que la composición o producto comprende 5-etil1-fenil-2- (1H) -piridona como único agente terapéutico.
Patentes similares o relacionadas:
Inhibidores de btk de tipo nicotinimida sustituida y su preparación y uso en el tratamiento del cáncer, la inflamación y las enfermedades autoinmunitarias, del 15 de Julio de 2020, de Guangzhou InnoCare Pharma Tech Co., Ltd: Un compuesto seleccionado del grupo que consiste en: 6-(1-acriloilpiperidin-4-il)-2-(4-fenoxifenil)nicotinamida; **(Ver fórmula)** 6-(4-acriloilpiperazin-1-il)-2-(4-fenoxifenil)nicotinamida; […]
FORMULACIÓN OFTÁLMICA DE PIRFENIDONA PARA LA PREVENCIÓN DEL DESARROLLO DE OPACIDAD CORNEAL POST CIRUGÍA FOTOREFRACTIVA LÁSER EXCIMER, del 25 de Junio de 2020, de CENTRO DE RETINA MÉDICA Y QUIRÚRGICA, S.C: El objeto de la invención es proporcional el uso de 5-metil-1-fenil-2-(1H)-piridona (pirfenidona) y quitosana en una solución oftálmica para la prevención del desarrollo de la […]
Métodos de administración de terapia con pirfenidona, del 13 de Mayo de 2020, de Intermune, Inc: Pirfenidona para su uso en el tratamiento de un paciente que necesita terapia con pirfenidona, caracterizada por que el tratamiento comprende reducir la dosis de […]
Moduladores heterocíclicos de transportadores de casete de unión a ATP, del 8 de Enero de 2020, de VERTEX PHARMACEUTICALS INCORPORATED: Un compuesto de Fórmula V-A: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: T es una cadena alifática C1-C2 […]
Compuestos aromáticos sustituidos para el tratamiento de la fibrosis pulmonar, la fibrosis del hígado, la fibrosis de la piel y la fibrosis cardíaca, del 1 de Enero de 2020, de Liminal Biosciences Limited: Un compuesto representado por la fórmula: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde A es alquilo C 5, alquilo […]
Derivados de 5-((halofenil)-3-halo-piridin-2-il)-nitrilo como intermedios para la preparación de derivados de ácido [(5-(halofenil)-3-hidroxipiridin-2-carbonil)-amino]alcanoico, del 11 de Diciembre de 2019, de Akebia Therapeutics Inc: Un compuesto que tiene la fórmula: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo en donde A es un anillo seleccionado […]
Composiciones farmacéuticas que comprenden lercanidipino, del 16 de Octubre de 2019, de RECORDATI IRELAND LIMITED: Composición farmacéutica que comprende lercanidipino o uno de sus análogos o una de sus sales farmacéuticamente aceptables como principio activo y un vehículo farmacéuticamente […]
Derivados de piridina, del 16 de Octubre de 2019, de ASTELLAS PHARMA INC.: Compuesto de fórmula (I) o una sal del mismo: **Fórmula** en la que R1 es alquilo C1-10 que tiene opcionalmente de 1 a 5 sustituyentes seleccionados […]