Perfil de temperatura en dos etapas para la propagación de virus.
Método para la producción de un virus, comprendiendo el método:
proporcionar una célula huésped infectada por el virus,
cultivar la célula huésped infectada a una primera temperatura entre 31ºC y 37ºC durante 1 a 48 horas,
cultivar a continuación la célula huésped infectada a una segunda temperatura que es de 1ºC a 6ºC inferior a la primera temperatura, y
recoger copias del virus producido mediante los pasos de cultivo,
consistiendo dicho virus en un ortomixovirus, alfavirus o flavivirus,
llevándose a cabo el método a escala industrial en más de 50 litros de cultivo celular y teniendo el método un efecto positivo en la pureza del antígeno en comparación con el mismo método llevado a cabo a temperatura constante.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/003532.
Solicitante: BAXTER INTERNATIONAL INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE BAXTER PARKWAY DEERFIELD, ILLINOIS 60015 ESTADOS UNIDOS DE AMERICA.
Inventor/es: REITER, MANFRED, MUNDT, WOLFGANG, GRILLBERGER, LEOPOLD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N7/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00).
- C12N7/02 C12N […] › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › Aislamiento o purificación.
PDF original: ES-2521496_T3.pdf
Fragmento de la descripción:
Perfil de temperatura en dos etapas para la propagación de virus.
La presente invención se refiere al campo de la propagación de virus.
La propagación de virus en cultivos celulares animales se lleva a cabo bajo condiciones de temperatura que dependen de las características del virus y del sistema huésped para la propagación. Para el crecimiento de las 5 células (en cultivo celular o siembra de huevos embrionarios) se seleccionan determinadas temperaturas, seguidas de una temperatura adecuada para la propagación viral. En la mayoría de los casos, la temperatura de propagación viral es menor que la temperatura de propagación celular. La propagación viral sensible a la temperatura se refiere a la influencia en la velocidad de propagación del virus y la formación de antígenos en un intervalo de temperatura centrado aproximadamente alrededor de 20º C en el caso de cultivos de células de insectos (por ejemplo con 10 producción de Baculovirus) y a temperaturas de hasta aproximadamente 37º C en el caso de la producción viral en cultivo celular de mamífero, existiendo valores óptimos específicos para cada combinación virus/célula huésped. Una temperatura más elevada afecta tanto a la cinética de infección como a la estabilidad viral. Cuando se propagan virus a una temperatura de 37º C, frecuentemente se observa un título viral reducido y una menor calidad de antígeno viral durante los períodos posteriores de replicación viral. Este efecto puede tener consecuencias 15 perjudiciales para la propagación del virus a gran escala en la producción de vacunas. En este contexto, Wehchuk y col. (Wehchuck, J. B. y col.; Biotechnology and Bioengineering, 79 (1) , julio de 2002, pp. 112-119) describen el uso de vectores basados en el virus de herpes simple de tipo 1 (VHS-1) genómico de replicación defectiva para transferir genes terapéuticos en células del sistema nervioso central y otros tejidos. El documento EP 1 526 172 A1 describe un proceso para la replicación del virus de la gripe en cultivo celular donde las células se cultivan a una temperatura 20 entre 30º C y 36º C después de infectarlas con el virus de la gripe. Rott y col. (Rott, R. y col.; Journal of General Virology, 3 (2) ; 1968; pp. 239-524) describen la síntesis del virus de la gripe aviar en fibroblastos de embrión de pollo a 37º C y 25º C. Yuk y col. (Yuk, I. H. y col.; Cytotechnology, 51 (3) ; noviembre de 2006; pp. 183-192) describen el cultivo de un virus quimérico del virus de la parainfluenza de tipo 3 (VPI3) y del virus respiratorio sincitial (VRS) a 37º C y 33º C después de infectar células huésped respectivas. Además, Jardon y col.; Biotechnology Progress, 25 19 (1) ; febrero de 2003; pp. 202-208) describen los efectos de variaciones de la temperatura de cultivo en la producción de un vector de adenovirus recombinante (AVr) en células HEK293. Por otro lado, McTaggart y col. (McTaggart, S. y col.; Biotechnology Progress, 16 (5) ; septiembre de 2000; pp. 859-865) describen la influencia de unas condiciones de cultivo a 32º C en comparación con unas condiciones de cultivo a 37º C en el título y el rendimiento celular cuando se producen vectores retrovirales en una línea celular empaquetadora. Finalmente, el 30 documento WO 03/085138 A describe la influencia de la reducción de la temperatura antes de la infección y vuelta a una temperatura más óptima en el momento de la infección viral o cerca del mismo en células huésped para la producción de virus térmicamente estables, tales como adenovirus y picornavirus.
Un objetivo de la presente invención es proporcionar unas condiciones de crecimiento mejoradas que no afecten a la calidad de los antígenos producidos con fines de vacunación. 35
La presente invención proporciona un método para la producción de un virus donde una o más células huésped se infectan con el virus y después se cultivan a una primera temperatura de 31º C a 37º C durante 1 a 48 horas y, a continuación, se cultivan a una segunda temperatura que es de 1 a 6º C inferior que la primera temperatura. Después se recoge el virus producido mediante estos pasos de cultivo, siendo dicho virus un ortomixovirus, alfavirus o flavivirus, llevándose a cabo el método a escala industrial en más de 50 litros de cultivo celular y teniendo el método 40 un efecto positivo sobre la pureza del antígeno en comparación con el mismo método llevado a cabo a temperatura constante.
Ahora se ha comprobado sorprendentemente que las condiciones de cultivo para muchos virus, incluyendo el virus de la gripe (Orthomyxoviridae) , virus del río Ross (Alphaviridae) y virus del Nilo occidental (Flaviviridae) , se puede mejorar considerablemente mediante el uso de un perfil de dos temperaturas. Para la primera fase de la propagación 45 viral se aplica una temperatura más alta, que acelera la formación de partículas virales infecciosas. En una segunda fase, se aplica una temperatura más baja para mantener el alto título inicial obtenido en el período de propagación a alta temperatura y para permitir una formación de antígeno estable, que puede ser utilizado para la producción adicional de vacunas inmunógenas.
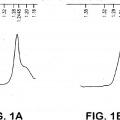
Fig. 1: Diagrama de bandas del antígeno del virus de Nueva Caledonia propagado en células Vero a (A) 50 32º C y (B) 36º C.
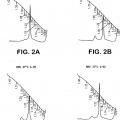
Fig. 2: Gráfico NaBr de infección por el virus del río Ross a 37º C en diferentes momentos después de la infección.
Fig. 3: Gráfico NaBr de infección por el virus del río Ross a 35º C en diferentes momentos después de la infección. 55
Fig. 4: Gráfico NaBr de infección por el virus del río Ross a 32º C en diferentes momentos después de la infección.
Fig. 5: Gráfico NaBr de infección por el virus del río Ross a 35º C/32º C en diferentes momentos después de la infección.
Fig. 6: Western blot de inóculo de infecciones por el virus del río Ross a 37º C y 35º C/32º C.
Fig. 7: Gráfico NaBr de infección por el virus del Nilo occidental a 35º C en diferentes momentos después de la infección, con imágenes microscópicas.
Fig. 8: Gráfico NaBr de infección por el virus del Nilo occidental a 32º C en diferentes momentos después de la infección, con imágenes microscópicas. 5
Fig. 9: Gráfico NaBr de infección por el virus del Nilo occidental a 35º C/32º C en diferentes momentos después de la infección, con imágenes microscópicas.
Un aspecto de la invención se refiere a que el perfil de temperatura en dos pasos tal como se describe aquí permite la optimización independiente y el control de (1) la formación de virus activos para infección de ciclo múltiple de células huésped, (2) el mantenimiento del alto título obtenido en la última fase de replicación y (3) la formación de 10 antígenos en la fase posterior del proceso de producción.
Preferentemente, el virus es un virus de la gripe y en determinadas realizaciones se selecciona de entre el grupo consistente en virus de la gripe A y B, virus del río Ross y virus del Nilo occidental. Aunque los ejemplos aquí proporcionados ilustran la producción mejorada de antígenos para estos virus utilizando el método de dos temperaturas de la invención, ejemplos no limitativos de otros virus considerados por la invención incluyen virus 15 seleccionados de entre el grupo de familias de ARN-virus tales como Reoviridae, Picornaviridae, Caliciviridae, Togaviridae, Arenaviridae, Retroviridae, Flaviviridae, Orthomyxoviridae, Paramyxoviridae, Bunyaviridae, Rhabdoviridae, Filoviridae, Coronaviridae, Astroviridae o Bornaviridae, y familias de ADN-virus tales como Adenoviridae, Papovaviridae, Parvoviridae, Herpesviridae, Poxviridae o Hepadnaviridae. En determinadas realizaciones, los virus se seleccionan de entre el grupo consiste en Influenza A/Panamá/2007/99, A/Nueva 20 Caledonia/20/99, B/Shangdong/7/97, B/Malasia/2506/2004, A/Hiroshima/52/2005 y A/Islas Salomón/3/2006.
El virus se puede producir en cualquier célula adecuada para la producción viral. Preferentemente, las células son de un cultivo celular o línea celular animal. Estas células pueden ser de un tejido específico o de células embrionarias. Preferentemente, el animal es un mamífero o un ave. En diversas realizaciones de la invención se pueden utilizar líneas celulares caninas, líneas celulares de roedor, líneas celulares aviares o líneas celulares de 25 tejido de primate. Por ejemplo, en determinadas realizaciones, las células pueden ser células MDCK, células CHO, células perC6, células HEK 293 u otras células utilizadas comúnmente en la propagación viral. En algunas realizaciones específicas, las células son células epiteliales, en particular células epiteliales renales, como células Vero de mono verde africano.
En ciertas realizaciones... [Seguir leyendo]
Reivindicaciones:
1. Método para la producción de un virus, comprendiendo el método:
proporcionar una célula huésped infectada por el virus, cultivar la célula huésped infectada a una primera temperatura entre 31º C y 37º C durante 1 a 48 horas, 5
cultivar a continuación la célula huésped infectada a una segunda temperatura que es de 1º C a 6º C inferior a la primera temperatura, y recoger copias del virus producido mediante los pasos de cultivo, consistiendo dicho virus en un ortomixovirus, alfavirus o flavivirus, llevándose a cabo el método a escala industrial en más de 50 litros de cultivo celular y teniendo el método 10 un efecto positivo en la pureza del antígeno en comparación con el mismo método llevado a cabo a temperatura constante.
2. Método según la reivindicación 1, caracterizado porque dicho virus es un virus de la gripe.
3. Método según la reivindicación 2, caracterizado porque dicho virus se selecciona de entre el virus de la gripe A y B. 15
4. Método según la reivindicación 1, caracterizado porque dicho virus es el virus del río Ross.
5. Método según la reivindicación 1, caracterizado porque dicho virus es el virus del Nilo occidental.
6. Método según la reivindicación 1, caracterizado porque dicha célula huésped es de un cultivo celular o línea celular animal.
7. Método según la reivindicación 6, caracterizado porque dicha célula huésped es una célula epitelial. 20
8. Método según la reivindicación 7, caracterizado porque dicha célula huésped es una célula epitelial renal.
9. Método según la reivindicación 8, caracterizado porque dicha célula huésped es una célula Vero.
10. Método según la reivindicación 1, caracterizado porque dicha primera temperatura oscila entre 32º C y 37º C.
11. Método según la reivindicación 10, caracterizado porque dicha primera temperatura oscila entre 33º C y 36º C. 25
12. Método según la reivindicación 11, caracterizado porque dicha primera temperatura oscila entre 34º C y 35, 5º C.
13. Método según la reivindicación 1, caracterizado porque dicha segunda temperatura es de 1, 5º C a 5º C inferior a dicha primera temperatura.
14. Método según la reivindicación 13, caracterizado porque dicha segunda temperatura es de 2º C a 4º C 30 inferior a dicha primera temperatura.
15. Método según la reivindicación 1, caracterizado porque dicha segunda temperatura oscila entre 29º C y 35º C.
16. Método según la reivindicación 15, caracterizado porque dicha segunda temperatura oscila entre 30º C y 34º C. 35
17. Método según la reivindicación 16, caracterizado porque dicha segunda temperatura oscila entre 31º C y 33º C.
18. Método según la reivindicación 1, caracterizado porque dicha célula huésped se cultiva directamente después de la inoculación.
19. Método según la reivindicación 1, caracterizado porque el virus producido se aísla. 40
20. Método según la reivindicación 1, caracterizado porque dicho virus se fragmenta.
21. Método según la reivindicación 1, caracterizado porque dicho virus se inactiva.
22. Método según la reivindicación 1, que adicionalmente comprende el paso de preparar una vacuna de dicho virus.
23. Método según la reivindicación 1, en el que dicho cultivo a una primera temperatura se lleva a cabo durante al menos dos horas. 5
Patentes similares o relacionadas:
Métodos mejorados para la preparación de escualeno, del 15 de Julio de 2020, de NOVARTIS AG: Un procedimiento para la preparación de escualeno a partir de una composición que comprende escualeno a partir de una fuente animal, dicho procedimiento comprendiendo […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Nueva especie de tobamovirus, del 17 de Junio de 2020, de Nunhems B.V: Un tobamovirus cuyo genoma comprende al menos 83% de identidad de secuencia con la SEQ ID NÚM.: 1 y en el que el virus causa síntomas sistémicos en plantas homocigotas […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Métodos para la transducción y el procesamiento de células, del 27 de Mayo de 2020, de Juno Therapeutics, Inc: Un método de transducción, que comprende incubar, en una cavidad interna de una cámara de centrífuga, una composición de entrada que comprende células y partículas […]
Composiciones para tratar MPSI, del 22 de Abril de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector que lleva un casete de expresión que comprende un gen de la alfa-L-iduronidasa humana (hIDUA) que tiene la secuencia de nucleótidos de SEQ ID NO: […]
Métodos mejorados para producir terapias celulares adoptivas, del 22 de Abril de 2020, de Bluebird Bio, Inc: Un método in vitro para producir un producto terapéutico de células T que comprende: a) proporcionar una población de células mononucleares […]
Nuevo bacteriófago y composición que comprende el mismo, del 25 de Marzo de 2020, de CJ CHEILJEDANG CORPORATION: Un bacteriófago ΦCJ26 (KCCM11464P) que tiene una capacidad específica para matar Salmonella. Una composición que comprende el bacteriófago ΦCJ26 (KCCM11464P) según […]