La actividad neuroprotectora de la proteína C activada es independiente de su actividad anticoagulante.
Una composición farmacéutica que comprende al menos una variante funcional de una proteína C humana activada (APC) o una proteína C humana para uso en el tratamiento de una enfermedad neurodegenerativa seleccionada del grupo consistente en isquemia y apoplejía,
en la que la variante funcional consta al menos de la mutación KKK191-193AAA, caracterizada porque la variante funcional está presente en una cantidad eficaz para proporcionar neuroprotección para células estresadas o lesionadas en un sujeto.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/038764.
Solicitante: ZZ BIOTECH L.L.C.
Inventor/es: GRIFFIN, JOHN, H., ZLOKOVIC,BERISLAV V.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01N1/02 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 1/00 Conservación de cuerpos humanos o animales, o partes de ellos. › Conservación de partes vivas.
- A61K49/00 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones para examen in vivo.
- C07K17/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos fijados sobre un soporte o inmovilizados; Su preparación.
- C07K7/00 C07K […] › Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados.
- C12N5/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
- C12P1/00 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › Preparación de compuestos o de composiciones, no prevista en los grupos C12P 3/00 - C12P 39/00, utilizando microorganismos o enzimas; Procedimientos generales de preparación de compuestos o composiciones que utilizan microorganismos o enzimas.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
PDF original: ES-2504365_T3.pdf

Fragmento de la descripción:
La actividad neuroprotectora de la proteína C activada es independiente de su actividad anticoagulante INVESTIGACIÓN O DESARROLLO PATROCINADOS POR EL GOBIERNO FEDERAL
El gobierno de EE.UU. tiene ciertos derechos sobre esta invención proporcionados por las subvenciones de los NIH HL6329 y HL52246 del Departamento de salud y servicios sociales.
ANTECEDENTES DE LA INVENCIÓN
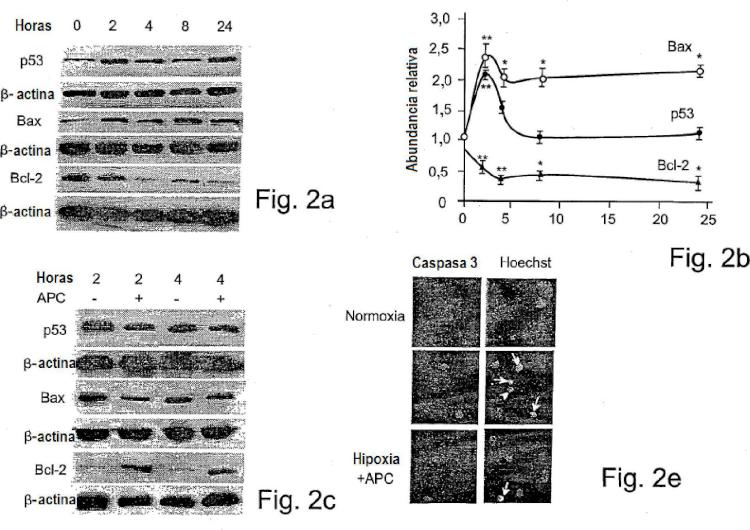
Esta invención se refiere al uso de proteína C activada (APC), un profármaco y/o una variante de la misma como se define en las reivindicaciones como inhibidor de la apoptosis o la muerte celular y/o factor de supervivencia celular, especialmente para células o tejidos del sistema nervioso que estén estresados o dañados. Esta función biológica de la APC puede separarse de su función anticoagulante (concretamente, la inhibición de la coagulación). La invención puede usarse para tratar isquemia y apoplejía al inhibir la ruta proapoptótica de señalización de p53 en células cerebrales estresadas o dañadas. Aquí se ha mostrado esto en endotelio cerebral humano in vitro y en animales in vivo (apoplejía isquémica y modelos de NMDA). La APC puede actuar a través del receptor de proteína C endotelial (EPCR) y el receptor activado de proteasa 1 (PAR-1) sobre células endoteliales cerebrales estresadas, o del PAR-1 y el receptor activado de proteasa 3 (PAR-3) sobre neuronas estresadas, activando rutas antiapoptóticas y y/o rutas prosupervivencia en estas células cerebrales estresadas y/o dañadas.
La proteína C se identificó originalmente por sus actividades anticoagulante y profibrinolítica. Tras la activación de la forma de zimógeno, la proteína C activada (APC) es una serinproteasa que desactiva los factores Va y Villa. La proteína C humana se fabrica principalmente en el hígado como polipéptido único de 461 aminoácidos. Esta molécula precursora se modifica postraduccionalmente entonces mediante (i) escisión de una secuencia señal de 42 aminoácidos, (¡I) retirada proteolítica del zimógeno monocatenario del residuo de lisina en posición 155 y del residuo de arginina en posición 156, produciendo la forma bicatenaria (concretamente, la cadena ligera de 155 residuos aminoacídicos unida por ligamiento disulfuro con la cadena pesada de 262 residuos aminoacídicos que contiene la serinproteasa), (iii) carboxilación de los residuos de ácido glutámico agrupados en los primeros 42 aminoácidos de la cadena ligera, dando como resultado nueve residuos de ácido y-carboxiglutámico (Gla), y (iv) glicosilación en cuatro sitios (uno en la cadena ligera y tres en la cadena pesada). La cadena pesada contiene la tríada de serinproteasa de Asp257, His211 y Ser36.
De forma similar a la mayoría de los demás zimógenos de las proteasas extracelulares y los factores de coagulación, la proteína C tiene una estructura nuclear de la familia de la quimotripsina, que tiene inserciones y una extensión N-terminal que posibilitan la regulación del zimógeno y la enzima. Son de interés dos dominios con secuencias aminoacídicas similares al factor de crecimiento epidérmico (EGF). Es conocida al menos una porción de las secuencias nucleotídica y aminoacídica de la proteína C de ser humano, mono, ratón, rata, hámster, conejo, perro, gato, cabra, cerdo, caballo y vaca, así como mutaciones y polimorfismos de la proteína C humana (véase el acceso a GenBank P47). Son conocidas otras variantes de la proteína C humana que afectan a diferentes actividades biológicas.
Recientemente, se ha aprobado la drotrecogina a (activada) (proteína C activada humana recombinante) para uso como tratamiento de la sepsis. Aunque su eficacia puede deberse en parte a la actividad antitrombótica de la APC, Grinnell y sus colegas proponen que sus efectos en la sepsis podrían atribuirse a las actividades antiinflamatoria y de supervivencia celular de la APC.
La capacidad de la proteína C activada de suprimir las rutas proinflamatorias y los mecanismos de supervivencia celular en la interfase de célula endotelial-mononuclear sugiere una compleja respuesta adaptativa en la pared del vaso para proteger al organismo del ataque vascular y para prolongar la supervivencia endotelial, celular y orgánica. Joyce y Grinnell, Crit. Care Med. 3: S288-S293 (22). Basándose en el perfil transcripcional, la apoptosis inducida por estaurosporina en células endoteliales de vena umbilical humana (FIUVEC) y la lesión mediada por factor de necrosis tumoral a de FIUVEC, Joyce et al. (J. Biol. Chem. 276: 11199-1123, 21) sugieren que la inhibición por APC de la señalización de NF-kB causa la regulación negativa de moléculas de adhesión, mientras que la inducción de genes antiapoptóticos (por ejemplo, proteína A1 relacionada con Bcl2 o Bcl2A1, inhibidor de la apoptosis 1 o clAP1, óxido nítrico sintasa endotelial o eNOS) se ha interpretado como un posible mecanismo ligado a los efectos antiapoptóticos de APC en el modelo de estaurosporina. Pero la expresión estos genes no se ha estudiado aquí. El papel directo de estos genes en el modelo de estaurosoprina tiene que mostrarse todavía y otros informes no sugieren un papel protector principal (Ackerman et al., J. Biol. Chem. 274: 11245-11252, 1999). Tampoco se han obtenido datos en células endoteliales cerebrales ni en estudios sobre estrés celular generalizado frente a ningún otro inductor de la apoptosis. El papel de estos genes antiapoptóticos no se ha mostrado en ninguno de los modelos; el único efecto directo de la APC que se ha determinado ha sido la inhibición de la señalización de NF-kB. Fia de observarse que NF-kB es un factor de transcripción que puede tener una función dual en el sistema nervioso
y endotelio y podría ser antiapoptótico o proapoptótico (Ryan ef al. Nature 44: 892-897, 2; Yu ef al. J. Neurosci. 19: 8856-8865, 1999; Yabe et al. J. Biol. Chem. 276: 43313-43319, 21). Por lo tanto, los efectos de supervivencia celular o citoprotección a través de la regulación negativa de NF-kB en el sistema nervioso y el sistema vascular no explican los efectos protectores celulares directos de la APC. Estas observaciones estaban también limitadas al modelo de estaurosporina o a un mecanismo de TNF-a en HUVEC.
Taylor y Esmon (patente de EE.UU. 5.9.889) dan a conocer que la APC Inhibe los estímulos Inflamatorios que desestabilizan los procesos de permeabilidad celular y coagulación normal en un paciente que padece disfunción del endotelio vascular. Estaban Interesados en tratar un trastorno slstémlco de células endotellales en sepsis (presuntamente reduciendo la respuesta Inflamatoria), en lugar de prevenir la apoptosls o promover la supervivencia celular. Tampoco han sugerido el tratamiento de enfermedades neurodegenerativas ni la prevención de la muerte y lesión de células neuronales.
Griffin et al. (patente de EE.UU. 5.84.274) y Grlnnell et al. (patente de EE.UU. 6.37.322) dan a conocer que la APC puede usarse para tratar oclusión trombótica o tromboembolla, que podrían Implicar apoplejía. De nuevo, no se ha proporcionado ningún dato en un modelo de apoplejía ni de los efectos de la APC sobre el resultado neurológico o neuropatológlco. Estas patentes estaban Interesadas en la actividad anticoagulante de APC en el tratamiento de trombosis. Pero no han sugerido efectos neuroprotectores celulares directos de la APC, ni que la actividad antlcoagulante no fuera necesaria para este efecto. Es posible que esta actividad antlcoagulante pueda limitar el uso de la APC en el tratamiento de apoplejía debido a complicaciones hemorrágicas. En contraposición, se muestra que esta actividad no es crítica para la neuroprotecclón.
Griffin ef al. (WO 1/56532) da a conocer que la APC puede usarse para el tratamiento de trastornos neuropatológlcos y enfermedades inflamatorias cerebrales. Se muestra que la APC proporciona neuroprotección en un modelo de Isquemia cerebral focal de murlno.
Rlewald ef al. (Science 296:188-1882, 22) han reseñado que la APC usa el receptor de proteína C de célula endotellal (EPCR) como correceptor para la activación del receptor activado de proteasa 1 (PAR-1) en células endotellales. Han encontrado también que Bcl2A1 y clAP1 se regulan positivamente. Sin embargo, sus resultados sobre el endotelio estaban limitados a HUVEC y la activación de la fosforilación de proteína clnasa activada por mltógeno (MAPK). Además, existen diferencias significativas en las respuestas celulares y su regulación de la expresión génica entre HUVEC y células endotellales cerebrales o cualquier otro tipo de células cerebrales (Berger ef a/., Molec. Med. 5: 795-85, 1999; Petzelbauer ef al. J. Immunol. 151: 562-572, 1993; Abbot ef al., Arthritis & Rheumatism 35: 41-46, 1992; Masón ef al.. Am. J. Phvsiol. 273: C1233-C124, 1997).
La técnica anterior no ha mostrado... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica que comprende al menos una variante funcional de una protema C humana activada (APC) o una proteína C humana para uso en el tratamiento de una enfermedad neurodegenerativa
seleccionada del grupo consistente en isquemia y apoplejía, en la que la variante funcional consta al menos de la mutación KKK191-193AAA, caracterizada porque la variante funcional está presente en una cantidad eficaz para proporcionar neuroprotección para células estresadas o lesionadas en un sujeto.
2. La composición farmacéutica de la reivindicación 1, que da como resultado una anticoagulación sistémica 1 al menos reducida o insignificante cuando se administra al sujeto.
3. La composición farmacéutica de la reivindicación 1 o 2, en la que la dosis unitaria se administra al sujeto en menos de 72 horas.
4. Uso de al menos una variante funcional de una proteína C humana activada (APC) o una proteína C
humana, en el que la variante funcional consta al menos de la mutación KKK191-193AAA, para la fabricación de una composición farmacéutica para tratar una enfermedad neurodegenerativa seleccionada del grupo consistente en isquemia y apoplejía, que comprende administrar una cantidad eficaz de la composición farmacéutica a un sujeto de tal modo que se mejora al menos un efecto del estrés o lesión en uno o más tipos celulares del sujeto; en el que 2 el uno o más tipos celulares están en el cerebro del sujeto y en el que el sujeto es un ser humano.
Patentes similares o relacionadas:
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Arginina desiminasa con reactividad cruzada reducida hacia anticuerpos para ADI - PEG 20 para el tratamiento del cáncer, del 6 de Mayo de 2020, de TDW Group: Una composición terapéutica que comprende una arginina desiminasa (ADI) aislada y un vehículo farmacéuticamente aceptable, en donde la ADI aislada comprende la secuencia de […]
Redes moleculares, del 29 de Abril de 2020, de Sienna Cancer Diagnostics Inc: Una estructura de red molecular multipolimérica estratificada que tiene múltiples capas con múltiples especies de agentes de captura unidas […]
Composiciones y métodos para la distribución de moléculas en células vivas, del 25 de Marzo de 2020, de THE TEXAS A & M UNIVERSITY SYSTEM: Un compuesto que tiene la fórmula: **(Ver fórmula)** En donde X es un resto de unión, Y es un residuo de aminoácido acoplado de forma covalente […]
Vacuna peptídica para la prevención e inmunoterapia de demencia del tipo Alzheimer, del 4 de Marzo de 2020, de UNITED BIOMEDICAL, INC.: Una composición que comprende una combinación de construcciones de inmunógenos de péptidos Aβ que consiste en las secuencias de aminoácidos de SEQ […]
Péptidos, dispositivos y procedimientos para la detección de anticuerpos de Anaplasma, del 20 de Noviembre de 2019, de Abaxis, Inc: Una composición que comprende una población de péptidos aislados, comprendiendo dicha población tres o más péptidos diferentes, en la que cada péptido en la población […]
Anticuerpos humanos que se unen al gen de activación de linfocitos 3 (LAG-3) y sus usos, del 6 de Noviembre de 2019, de E. R. Squibb & Sons, L.L.C: Un anticuerpo monoclonal humano aislado, o una porción de unión a antígeno del mismo, que se une al gen de activación de linfocitos humanos 3 (LAG-3) y se une […]
Métodos y composiciones para el tratamiento de la esclerosis múltiple y trastornos asociados, del 14 de Mayo de 2019, de UTI Limited Partnership: Un complejo de nanopartícula que comprende: un núcleo de nanopartícula; una serie de complejos de antígeno- MHC (pMHC) que comprenden una serie de proteínas […]