Fosfaplatinos y su uso en el tratamiento de cánceres resistentes a cisplatino y carboplatino.
Una composición para el uso en un método para tratar el cáncer que comprende:
uno o más complejos de platino (II) o (IV) monoméricos aislados según las fórmulas I, II, III y IV:
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir;
en la que cada R3 se selecciona de aminas alifáticas sustituidas o sin sustituir;
en la que cuando uno de R1 y R2 es NH3, el otro de R1 y R2 no es NH3; y
en la que cada S se selecciona independientemente de hidróxido, ácido acético, ácido butírico, y alfa-hidroxi ácidos; o
cis-diamino-trans-dihidroxo(dihidrogenopirofosfato)platino(IV) monomérico aislado;
o las sales farmacéuticamente aceptables de los mismos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/072398.
Solicitante: OHIO UNIVERSITY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: TECHNOLOGY TRANSFER OFFICE UNIT 14 340 WEST STATE STREET ATHENS, OHIO 45701 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BOSE,RATHINDRA N.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/282 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos del platino.
- A61K33/24 A61K […] › A61K 33/00 Preparaciones medicinales que contienen ingredientes activos inorgánicos. › Metales pesados; Sus compuestos.
PDF original: ES-2495743_T3.pdf



Fragmento de la descripción:
Fosfaplatinos y su uso en el tratamiento de cánceres resistentes a cisplatino y carboplatino Antecedentes de la invención
Los complejos de platino-diamina se conocen bien en la técnica debido al éxito extraordinario de cis- diaminodicloroplatino(ll) (cisplatino) para el tratamiento del cáncer ovárico, testicular, de cabeza y cuello, y otras formas de cáncer. Además, el cisplatino se usa junto con otros regímenes terapéuticos que incluyen la radioterapia. Este platino quimioterápico actúa como mediador en la apoptosis en la fase G2 del ciclo celular de manera predominante por medio de la inhibición de la transcripción y por medio de procesos de inhibición de la replicación, especialmente a dosis elevadas. En general se cree que la unión covalente al ADN por medio de los sitios N7 de las bases de guanina y adenina, de modo intra- e inter-catenario, es el suceso molecular clave en la transducción de una cascada de respuestas celulares que conducen a la apoptosis.
Aunque el cisplatino es muy eficaz, exhibe toxicidad renal, nefrotoxicidad, y neurotoxicidad. Además, muchos pacientes desarrollan resistencia al tratamiento con cisplatino con el tiempo, y por lo tanto no se curan mediante el tratamiento con cisplatino. Se cree también que otros dos fármacos de platino aprobados por la FDA, carboplatino (diamino-1,1-dicarboxilatociclobutano-platino(ll)) y oxaliplatino (diamino-oxalatoplatino(ll)), funcionan de una manera similar a la de cisplatino. El carboplatino es especialmente eficaz hacia las células tumorales resistentes a cisplatino, pero se necesitan dosis relativamente elevadas para tratar de manera eficaz a pacientes que son resistentes a cisplatino. Tales dosis elevadas también tienen toxicidades asociadas.
Se han sintetizado muchos complejos nuevos de platino-amina y se han ensayado sus actividades antineoplásicas. Sin embargo, solamente algunos de estos complejos (algunos de los cuales se enumeran en la Figura 14) han exhibido resultados prometedores. Estos complejos nuevos contienen una diversidad de ligandos sustituibles distintos de amina, así como ligandos amina no sustituibles que se cree que son importantes para la unión al ADN y la absorción celular. En general, estos y otros complejos de platino-amina relevantes conocidos en la técnica se sintetizan mediante el proceso usado para preparar cisplatino, concretamente en el que tetracloroplatinato (PtCU2 ) recibe los ligandos amina para convertirse en PtCbíamina/diamina). Partiendo del complejo de tetracloro se proporcionan en general otros productos, y así también se puede usar PtU2" para asegurar un rendimiento elevado y la pureza del isómero cis, seguido por la conversión de PtU2" en PtUíamina/diamina) y después en PtCI2(amina/diamina). Al convertir PtUjamina/diamina) en PtCbjamina/diamina), el complejo di-yodo se convierte en complejo diaqua tratando el primero con dos equivalentes de nitrato de plata u otras sales de plata solubles a pH bajo. El complejo diaqua resultante reacciona fácilmente con cloruro potásico o ácido clorhídrico para producir el complejo dicloro de interés. En general, los complejos de platino de interés se sintetizan a partir del complejo diaqua correspondiente a un pH bajo para introducir los ligandos sustituibles, ya que la dimerización o polimerización del complejo diaqua tiene lugar rápidamente a un pH superior, lo que genera productos indeseables.
En vez de ligandos cloro sustituibles, los complejos de platino-amina de la técnica también tienen nitrógeno, azufre, carboxilato, y fosfonato como ligandos sustituibles. Sin embargo, una característica de esos complejos, que son los más prometedores para tratar el cáncer, es un ligando de base fuerte sustituible coordinado con platino (un ácido débil). Los ejemplos de tales combinaciones fuerte-débil que han exhibido propiedades antineoplásicas excelentes son los complejos de platino con carboxilato, carbonato, fosfonato.
A pesar de los intentos extraordinarios de sustituir cisplatino con agentes quimioterápicos más eficaces, los complejos de platino(ll) y platino(IV) con fosfatos como ligandos sustituibles han quedado en gran medida sin investigar. Esto es principalmente debido al hecho de que los primeros trabajos sobre los complejos de platino(ll)- fosfato normalmente dieron como resultado complejos dinucleares conectados por fosfato. A pesar de los informes sobre las propiedades antineoplásicas excelentes de ciertos complejos de fosfatoplatino(ll) dinucleares, el estudio adicional de sus aplicaciones fue limitado debido a la escasa solubilidad de estos complejos en disoluciones acuosas. Aunque se conocen ciertos complejos monoméricos de pirofosfato y trifosfato en la técnica, tales complejos no son adecuados para las composiciones farmacéuticas porque experimentan la hidrólisis del fosfato en disoluciones moderadamente ácidas, lo que da como resultado productos dinucleares insolubles (véase el documento US 7.342.122 de Odani et al., que describe un dímero del complejo monomérico am-2 que se describe en la presente memoria y en Bose et al., Inorg. Chem. 1985, 24, 3989-3996; véase también el documento WO 25/858 de Odani et al., que describe am-2 monomérico como un fármaco antineoplásico potencial).
Por lo tanto, sigue existiendo la necesidad en la técnica de alternativas estables y eficaces al cisplatino y carboplatino para el tratamiento de cánceres.
Compendio de la invención
La presente invención proporciona composiciones que comprenden fosfaplatinos, complejos de fosfato monoméricos estables de platino (II) y (IV), para el uso en un método para tratar el cáncer, como se define en las reivindicaciones.
También se proporcionan métodos para producir y aislar fosfaplatinos, como se define en las reivindicaciones.
Se describen métodos para tratar cánceres, que incluyen los cánceres resistentes a cisplatino y/o carboplatino, mediante la administración de una cantidad eficaz de fosfaplatinos, solos o en combinación, con un excipiente farmacéuticamente aceptable, a un sujeto que necesita tal tratamiento.
Descripción breve de los dibujos
La FIGURA 1 muestra estructuras de algunos de los complejos de platino (II) y platino (IV) de la presente invención, en los que R1, R2, R3 y S son como se definen en las reivindicaciones. De acuerdo con las reivindicaciones 1 y 2, ciertos complejos que se excluyen de estas estructuras también forman parte de la invención. En ciertas realizaciones, R1 y R2 se seleccionan de amina, metil amina, etil amina, propil amina, isopropil amina, butil amina, ciclohexano amina, anilina, piridina, y piridina sustituida. En ciertas realizaciones, R3 se selecciona de etilendiamina y ciclohexanodiamina.
En ciertas realizaciones, se reivindican las sales farmacéuticamente aceptables de los compuestos.
La FIGURA 2 muestra estructuras de ciertos complejos aislados de la presente invención, concretamente (A) diamino(dihidrogenopirofosfato)platino(ll), también conocido como am-2; (B) c/s-diamino-frans-dihidroxo
(dihidrogenopirofosfato)platino(IV), también conocido como am-4; (C) 1,2-etanodiamino(dihidrogenopirofosfato) platino(ll), también conocido como en-2; (D) 1,2-etanodiamino-frans-dihidroxo(dihidrogenopirofosfato)platino(IV), también conocido como en-4; (E) (frans-1,2-ciclohexanodiamino)(dihidrogenopirofosfato)platino(ll), también conocido como dach-2; y (F) (frans-1,2-ciclohexanodiamino)-frans-dihidroxo(dihidrogenopirofosfato)platino(IV), también conocido como dach-4.
La FIGURA 3 muestra la estructura cristalina de rayos X de am-4 con un contraión de sodio.
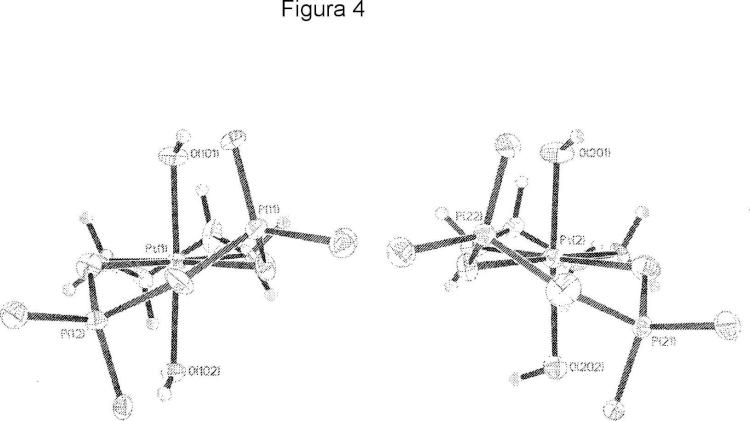
La FIGURA 4 muestra la estructura cristalina de rayos X de en-4 en sus diferentes conformaciones, vista desde el lado de pirofosfato.
La FIGURA 5 muestra el grado de protonación de los complejos mostrados en la Figura 2, tal como se mide mediante el desplazamiento químico de 31P, como función del pH. Las constantes de acidez estimadas se enumeran en la Tabla 1. Estos datos proporcionan conocimientos sobre las diferencias de solubilidad de estos complejos entre la disolución ácida y la disolución neutra. En las condiciones descritas a valores de pH por debajo de 2, estos complejos están completamente protonados, y por lo tanto se espera que exhiban una solubilidad reducida.
La FIGURA 6 exhibe la estabilidad diferencial de dach-2 a (A) pH 4,2 y (B) pH 8. A pH 8, no se observó descomposición de dach-2, tal como se demuestra mediante la retención del ión de pirofosfato coordinado con platino(ll) hasta seis días. En contraste, a pH 4,2, es evidente una descomposición considerable debida a la aparición de la señal de pirofosfato libre. Partiendo del espectro inferior en cada panel, se registraron los espectros a intervalos de tiempo de 24 horas.
La FIGURA 7 es un... [Seguir leyendo]
Reivindicaciones:
Una composición para el uso en un método para tratar el cáncer que comprende:
uno o más complejos de platino (II) o (IV) monoméricos aislados según las fórmulas I, II, III y IV:
| , VH R \/° \ Pt | , oV" "xl/ \ |
| / \-p( cr oh (i) | rl u é' NoH(n) |
| o-V (X )° v\ oh (ni) | \/H cV\ U\ / s OP. <X OH (IV) |
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir; en la que cada R3 se selecciona de aminas alifáticas sustituidas o sin sustituir; en la que cuando uno de R1 y R2 es NH3, el otro de R1 y R2 no es NH3; y
en la que cada S se selecciona independientemente de hidróxido, ácido acético, ácido butírico, y alfa-hidroxi ácidos; o
c/s-diamino-frans-dihidroxo(dihidrogenopirofosfato)platino(IV) monomérico aislado; o las sales farmacéuticamente aceptables de los mismos.
2. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que R1 y R2 se seleccionan cada uno independientemente de NH3, metil amina, etil amina, propil amina, isopropil amina, butil amina, y ciclohexano amina.
3. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que R3 se selecciona de etilenodiamina y ciclohexanodiamina.
4. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que el complejo de platino monomérico aislado es:
1.2- etanodiamino(dihidrogenopirofosfato)platino(ll), o (frar7S-1,2-ciclohexanodiamino)(dihidrogenopirofosfato)platino(ll), o c/s-diamino-frans-dihidroxo(dihidrogenopirofosfato)platino(IV), o
1.2- etanodiamino-frans-dihidroxo(dihidrogenopirofosfato)platino(IV), o (trans-1,2-ciclohexanodiamino)-frar7S-dihidroxo(dihidrogenopirofosfato)platino(IV).
5. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que el complejo de platino monomérico aislado es (transé ,2-ciclohexanodiamino)(dihidrogenopirofosfato)platino(ll).
6. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que el complejo de platino monomérico aislado es (transé ,2-ciclohexanodiamino)-frar7S-dihidroxo(dihidrogenopirofosfato)platino(IV).
7. Una composición para el uso en un método para tratar el cáncer según la reivindicación 1 que comprende: uno o más complejos de platino monoméricos aislados seleccionados de
(i) cis-diamino-trans-dihidroxo(dihidrogenopirofosfato)platino(IV);
(ii) 1,2-Etanodiamino(dihidrogenopirofosfato)platino(ll);
(iii) 1,2-Etanodiamino-trans-dihidroxo(dihidrogenopirofosfato)platino(IV);
(iv) (Trans-?,2-ciclohexanodiamino)(dihidrogenop¡rofosfato)platino(ll);
(v) Trans-1,2-ciclohexanodiam¡no)-frans-dihidroxo(dihidrogenopirofosfato)plat¡no(IV); y
(vi) sales farmacéuticamente aceptables de los mismos.
8. La composición para el uso en un método para tratar el cáncer de la reivindicación 7, en la que el complejo de platino monomérico aislado es estable en disolución acuosa a un pH de alrededor de 6 a alrededor de 8.
9. La composición para el uso en un método para tratar el cáncer de la reivindicación 7, en la que el complejo de platino monomérico aislado no se une al ADN.
1. La composición para el uso en un método para tratar el cáncer de la reivindicación 7, en la que el complejo de platino monomérico aislado desencadena la sobreexpresión de fas y factores de transcripción relacionados con fas, o de genes proapoptóticos.
11. La composición para el uso en un método para tratar el cáncer de la reivindicación 1, en la que los genes proapoptóticos son Bak y Bax.
12. Un método para preparar un complejo de platino (II) monomérico aislado que comprende:
(i) mantener una mezcla de reacción acuosa que comprende pirofosfato en exceso y un complejo de platino según la fórmula V o VI:
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir, en la que R3 se selecciona de aminas alifáticas sustituidas o sin sustituir; y en la que X se selecciona independientemente de halógenos;
a una temperatura de alrededor de 3 a alrededor de 6 grados Celsius durante un periodo de alrededor de 12 a alrededor de 18 horas a un pH de alrededor de 7 a alrededor de 9;
(¡i) concentrar posteriormente la mezcla de reacción acuosa de manera que no se formen precipitados de pirofosfatos;
(iii) bajar rápidamente el pH de la mezcla de reacción hasta un pH menor de 2 mediante la adición de un ácido; en la que el complejo de platino (II) monomérico aislado tiene una fórmula de I o III:
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir;
en la que R3 se selecciona de diaminas alifáticas sustituidas o sin sustituir; y
en la que el complejo de platino monomérico aislado es estable en disolución acuosa a un pH de alrededor de 6 a alrededor de 9.
13. El método de la reivindicación 12, en el que el complejo de platino monomérico aislado preparado es (Trans-1,2- ciclohexanodiamino)(dihidrogenopirofosfato)platino(ll).
14. Un método para preparar un complejo de platino (IV) monomérico aislado que comprende:
(V)
(VI)
(i) mantener una mezcla de reacción acuosa que comprende pirofosfato en exceso y un complejo de platino según la fórmula V o VI:
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir, en la que R3 se selecciona de aminas alifáticas sustituidas o sin sustituir, y en la que X se selecciona independientemente de halógenos;
a una temperatura de alrededor de 3 a alrededor de 6 grados Celsius durante un periodo de alrededor de 12 a alrededor de 18 horas a un pH de alrededor de 7 a alrededor de 9;
(ii) añadir a la mezcla de reacción peróxido de hidrógeno, y opcionalmente un reactivo seleccionado del grupo de sales de acetato, sales de butirato, y sales de alfa-hidroxi ácidos, y las combinaciones de las mismas;
(iii) concentrar posteriormente la mezcla de reacción acuosa de manera que no se formen precipitados de pirofosfato;
(iv) bajar rápidamente el pH de la mezcla de reacción hasta un pH menor de 2 mediante la adición de ácido nítrico;
en la que el complejo de platino (IV) monomérico aislado tiene una fórmula de II o IV:
Pl O
/\ /
S C-PX
.OH
`OH (II)
en la que cada R1 y R2 se selecciona independientemente de NH3, y aminas alifáticas sustituidas o sin sustituir;
en la que R3 se selecciona de aminas alifáticas sustituidas o sin sustituir;
en la que cada S se selecciona independientemente de hidróxido, ácido acético, ácido butírico, y alfa- hidroxi ácidos; y
en la que el complejo de platino monomérico aislado es estable en disolución acuosa a un pH de alrededor de 6 a alrededor de 9.
15. El método de la reivindicación 12 o la reivindicación 14, en el que la temperatura es 4 grados Celsius y el tiempo de reacción es 15 horas y el pH es de 7 a 8.
16. El método de la reivindicación 12 o la reivindicación 14, que comprende además enfriar la mezcla de reacción a una temperatura de entre 5 grados Celsius y la temperatura ambiente después de concentrar la mezcla de reacción, o después de bajar el pH de la mezcla de reacción.
17. El método de la reivindicación 14, en el que el reactivo opcional añadido junto con peróxido de hidrógeno antes de la concentración de la mezcla de reacción se selecciona de acetato sódico, butirato sódico, y sales sódicas de alfa-hidroxi ácidos, o de acetato potásico, butirato potásico, y sales potásicas de alfa-hidroxi ácidos.
18. El método de la reivindicación 14, en el que el peróxido de hidrógeno está a una concentración vol/vol inicial del 3%.
19. El método de la reivindicación 14, en el que el complejo de platino monomérico aislado preparado es: c/s-diamino-fra/is-dihidroxo(dihidrogenopirofosfato)platino(IV), o
1,2-Etanod¡am¡no-frans-d¡h¡droxo(d¡h¡drogenopirofosfato)plat¡no(IV), o Trans-1,2-c¡clohexanod¡am¡no)-frans-d¡hidroxo(d¡h¡drogenop¡rofosfato)plat¡no(IV).
2. Una composición que comprende una cantidad terapéuticamente eficaz de al menos un complejo de platino monomérico aislado seleccionado de diamino(dihidrogenopirofosfato)platino(lI) y los complejos de la reivindicación 1
y al menos un excipiente, diluyente, adyuvante, o vehículo farmacéuticamente aceptable, para el uso en un método para tratar un cáncer que es resistente a uno o más agentes antineoplásicos seleccionados de cisplatino, carboplatino, y oxaliplatino.
21. La composición para el uso en un método para tratar el cáncer de la reivindicación 1 o la reivindicación 2, en el que el cáncer se selecciona de cáncer testicular, pulmonar de células pequeñas, y de cabeza y cuello.
22. La composición para el uso en un método para tratar el cáncer de la reivindicación 1 o la reivindicación 2, en el
que el cáncer es ovárico.
23. La composición para el uso en un método para tratar el cáncer de cualquiera de las reivindicaciones 2 a 22, en el que el complejo de platino monomérico aislado es como se definió en cualquiera de las reivindicaciones 2 a 4.
24. La composición para el uso en un método para tratar el cáncer de la reivindicación 23, en la que el complejo de 15 platino monomérico aislado es (frans-1,2-ciclohexanodiamlno)(d¡h¡drogenop¡rofosfato)plat¡no(ll).
25. La composición para el uso en un método para tratar el cáncer de la reivindicación 23, en la que el complejo de platino monomérico aislado es (frar7s-1,2-ciclohexanod¡am¡no)-frans-d¡h¡droxo(d¡h¡drogenop¡rofosfato)plat¡no(IV).
Patentes similares o relacionadas:
Método de tratamiento del cáncer, del 22 de Julio de 2020, de Intensity Therapeutics, Inc: Una composición que comprende una cantidad terapéuticamente efectiva de un agente terapéutico y un agente mejorador de la permeación intracelular para uso en el tratamiento […]
Anticuerpo anti-Notch 4 humano, del 1 de Julio de 2020, de EISAI R&D MANAGEMENT CO., LTD: Un anticuerpo anti-Notch4 o un fragmento de unión a Notch4 de este, donde dicho anticuerpo o un fragmento de unión a Notch4 de este comprende cadenas pesadas y ligeras y […]
Formulaciones no tóxicas de nanopartículas radioluminiscentes para usar como agentes radiosensibilizantes del cáncer, del 24 de Junio de 2020, de PURDUE RESEARCH FOUNDATION: Una formulacion, que comprende una particula cristalina o agregado de particulas encapsulado dentro de un copolimero en bloque anfifilico […]
Actividad antitumoral de inhibidores de multicinasas en cáncer colorrectal, del 10 de Junio de 2020, de ENTRECHEM, S.L: Composición para uso en la prevención y/o el tratamiento de cáncer colorrectal en un paciente, que comprende: a) un compuesto de fórmula (I) **(Ver fórmula)** […]
Clústeres cuánticos atómicos estables, su método de obtención y uso de los mismos, del 6 de Mayo de 2020, de UNIVERSIDADE DE SANTIAGO DE COMPOSTELA: Clústeres cuánticos atómicos, AQCs, estables caracterizados por estar compuestos por menos de 500 átomos de metal, su procedimiento de obtención caracterizado […]
Enlazadores sensibles al pH para suministrar un agente terapéutico, del 8 de Abril de 2020, de GNT Biotech & Medicals Corporation: Un enlazador sensible al pH que tiene la siguiente fórmula (I), **(Ver fórmula)** en donde X es **(Ver fórmula)** -SH, -NH2, Boc-NH-, Fmoc-NH-, -COOH; n […]
Combinaciones y modos de administración de agentes terapéuticos y terapia combinada, del 8 de Abril de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden paclitaxel y una albúmina, para uso en un método para el tratamiento de cáncer de pulmón en un individuo, en […]
Activación de procaspasa 3 mediante terapia de combinación, del 19 de Febrero de 2020, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ILLINOIS: Una composición que comprende: (a) un compuesto PAC-1: **(Ver fórmula)** (b) un segundo agente activo, en donde el segundo agente activo es bortezomib, […]