Uso de tris(hidroximetil) aminometano para la estabilización de péptidos, polipéptidos y proteínas.
Método de estabilización de una solución acuosa de péptido, polipéptido o proteína,
y análogos y/o derivados de losmismos, comprendiendo: la adición de una cantidad de tris(hidroximetil)aminometano a la solución acuosa suficiente parainducir estabilización, donde el tris(hidroximetil)-aminometano es un agente tampón o un aditivo donde la solución acuosacomprende además un modificador orgánico que es seleccionado de: metanol, etanol, 1-propanol, 2-propanol, butanol,hexilenglicol, acetonitrilo y n-metil-2-pirrolidona, y donde el modificador orgánico está presente en una concentración de 1%p/p a 70% p/p.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/054209.
Solicitante: NOVO NORDISK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: Novo Allé 2880 Bagsvaerd DINAMARCA.
Inventor/es: STABY,ARNE, CHRISTIANSEN,INGUN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K1/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Procedimientos generales de preparación de péptidos.
PDF original: ES-2442223_T3.pdf
Fragmento de la descripción:
Uso de tris (hidroximetil) aminometano para la estabilización de péptidos, polipéptidos y proteínas [0001] Esta invención se refiere generalmente a un método para la reducción de la aparición o incidencia de gelificación/fibrilación/agregación durante el “upstream y downstream processing” (procesado previo y procesado de separación y purificación) y purificación de péptidos, polipéptidos y proteínas.
Un gran número de polipéptidos han sido aprobados para uso en la práctica médica. Estos polipéptidos se pueden producir en células huéspedes adecuadas por tecnología del ADN recombinante o se pueden producir sintéticamente por tecnología de síntesis de péptidos bien establecida. No obstante, polipéptidos nativos al igual que análogos y derivados de los mismos tienden a mostrar niveles elevados de aclaramiento que son inaceptables para muchas indicaciones clínicas donde una elevada concentración de plasma del péptido se requiere durante un periodo temporal prolongado. Ejemplos de péptidos que en su forma nativa con un índice de aclaramiento elevado son: ACTH, factor liberador de corticotropina,
angiotensina, calcitonina, exendina, exendina-3, exendina-4, insulina, glucagón, péptido 1 de tipo glucagón, péptido 2 de tipo glucagón, factor 1 de crecimiento de tipo insulina, factor 2 de crecimiento de tipo insulina, péptido inhibitorio gástrico, factor liberador de la hormona del crecimiento, péptido activador de adenilato-ciclasa de la pituitaria, secretina, enterogastrina, somatostatina, somatotropina, somatomedina, hormona paratiroidea, trombopoyetina, eritropoyetina, factores de liberación hipotalámica, prolactina, hormonas estimuladoras de la tiroides, endorfinas, enquefalinas, vasopresina, oxitocina, opioides y
sus análogos, superóxido-dismutasa, interferón, asparaginasa, arginasa, arginina desaminasa, adenosina-desaminasa y ribonucleasa.
Mientras que varias formulaciones acuosas que estabilizan composiciones de péptidos, polipéptidos y de proteínas han sido identificadas en la técnica, la desestabilización de péptidos, polipéptidos y proteínas tanto en soluciones de formulación como en solución durante el proceso continúa generándose difícilmente, especialmente en el “upstream y downstream processing” de estos péptidos. Consecuentemente, hay una necesidad de nuevos métodos que superan las insuficiencias del estado de la técnica. (Senderhoff et al., J. Pharm. Sc. Vol. 87, No. 2, págs. 183-189, febrero 1998) .
EP 1 396 499 describe un proceso para estabilizar compuestos de péptido de tipo glucagón (GLP-1) .
EP 0 747 390 describe métodos de reducción de la gelificación de una proteína acilada de ácido graso usando un tampón de citrato.
S.E.Bondos y A.Bicknell Analytical Biochemistr y 316 (2003) 223-231. Tris (hidroximetil) aminometano no se menciona 35 como un agente que puede promover solubilidad de proteína en este artículo.
EP 0 722 492 se refiere a estabilización de enzimas, anticuerpos, antígenos etc.
EP 1 344 533 se refiere a composiciones farmacéuticas que comprenden MBL (lectina de unión a la manosa) y/o 40 variantes de MBL.
WO 01/52937 divulga composiciones farmacéuticas para polipéptidos que comprenden un tampón de combinación.
RESUMEN DE LA INVENCIÓN
La presente invención se refiere a métodos para la reducción de la aparición o incidencia de gelificación/fibrilación/agregación durante el “upstream y downstream processing” y purificación de péptidos, polipéptidos y proteínas incluyendo péptidos de tipo glucagón (GLPs) , exendina y sus análogos y/o derivados.
La presente invención proporciona un método para tratar una solución acuosa de péptidos, polipéptidos y proteínas con o sin un modificador orgánico a concentraciones más altas, con menos regulación de la temperatura y del pH que los métodos habitualmente utilizados.
Más particularmente, la presente invención se refiere a un método de procesamiento y purificación de péptidos,
polipéptidos y proteínas incluyendo compuestos de péptido de tipo glucagón (GLP) en presencia de tris (hidroximetil) aminometano (TRIS) y un modificador orgánico que es seleccionado de: metanol, etanol, 1-propanol, 2-propanol, butanol, hexilenglicol, acetonitrilo y N-metil-2-pirrolidona.
La presente invención también proporciona soluciones acuosas de péptidos, polipéptidos y proteínas con una 60 tendencia reducida a gelificación/fibrilación/agregación.
BREVE DESCRIPCIÓN DEL DIBUJO
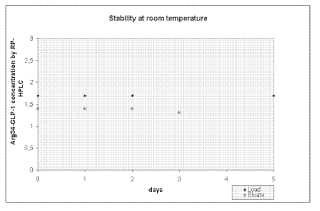
Figura 1: una representación gráfica de un estudio de estabilidad para una solución acuosa de Arg34-GLP-1[7-37] que contiene aproximadamente 2% en peso de etanol y 10 mM de tris- (hidroximetil) aminometano, a pH 9, 2, temperatura ambiente.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
La presente invención detalla el descubrimiento sorprendente de que el procesamiento de péptidos o proteínas en presencia de un tampón de TRIS o aditivo de TRIS, tal como en el flujo de proceso, particularmente un flujo de proceso con un solvente orgánico polar tal como etanol, la tendencia de péptidos, polipéptidos y proteínas para formar un gel, fibrilar o agregar es inmensamente reducida.
En métodos de la presente invención, tris- (hidroximetil) aminometano, y sustancias tampón biológico similares han mostrado ser superiores en péptidos estabilizantes, polipéptidos y proteínas, incluyendo péptidos de tipo glucagón (GLPs, análogos y derivados del mismo) en solución, durante el “upstream y downstream processing” y en que previenen la degradación física del producto de fármaco final. TRIS generalmente se refiere a 2-amino-2-hidroximetil-1, 3-propanodiol, y a cualquier sal derivada farmacéuticamente aceptable. La base libre y la forma de hidrocloruro son dos formas comunes de TRIS. TRIS es también conocido en la técnica como aminometano de trimetilol, tampón de tris amina, THAM, y trometamina. TRIS tiene un pKA de aproximadamente 8.05. TRIS usado como un "aditivo" se refiere al uso de TRIS fuera de su variedad de tampón típico, por ejemplo por debajo de un pH de aproximadamente 7.0, o por encima de un pH de aproximadamente 9.1.
“Upstream o downstream processing” y purificación de péptidos, polipéptidos y proteínas incluye, pero no se limita a fermentación, evaporación giratoria, cultivo, filtración, centrifugado, métodos de cromatografía, síntesis enzimática, síntesis orgánica, conversión enzimática, precipitación, cristalización, liofilización, liofilización u otros medios conocidos por el artesano experto.
El término "modificadores orgánicos" se refiere a un solvente orgánico o compuesto orgánico soluble en agua o mezclas derivadas, este modificador induce una selectividad favorable y cambiada entre la impureza o impurezas relacionada (s) indeseada (s) y el péptido y el intercambiador iónico. Si un modificador seleccionado induce o no dicha selectividad normalmente dependerá de la impureza o impurezas relacionada (s) , y se puede evaluar por prueba-y-error. El modificador orgánico incluye pero no se limita a alcanol C1-6, alquenol C1-6 o alquinol C1-6, acetonitrilo, N-metil pirrolidona, urea, guanidina-HCl, o ácido alcanoico C1-6, tal como ácido acético, glicol C2-6, polialcohol C3-7 incluyendo azúcares o mezclas derivadas.
El término, " alcanol C1-6 ", " alquinol C1-6" o " alquenol C1-6", como se utiliza en este caso solo o en la combinación se destina a incluir aquellos grupos alcano C1-6, alqueno C1-6 o alquina C1-6 de la longitud designada en bien una configuración cíclica o ramificada o lineal a la cual se enlaza un hidróxilo (-OH) (véase Morrison & Boyd, Organic Chemistr y , 4ª ed.) . Ejemplos de alcoholes lineales son metanol, etanol, n-propanol, alcohol alílico, n-butanol, n-pentanol y n-hexanol. Ejemplos de alcoholes ramificados son 2-propanol y alcohol tert-butílico. Ejemplos de alcoholes cíclicos son alcohol de ciclopropilo y 2-ciclohexen-1-ol.
El término "ácido alanoico C1-6", como se utiliza en este caso, se destina a incluir un grupo de la fórmula R'COOH donde R' es H o alquilo C1-5, tal como ácido acético, propiónico, butírico, a-metilbutírico, o valérico (véase Morrison & Boyd, Organic Chemistr y , 4ª ed.) .
El término " alquilo C1-5", como se utiliza en este caso, se destina a incluir un grupo ramificado o recto de alquilo teniendo de uno a cinco átomos de carbono. Típicos grupos de alquilo C1-5 incluyen, pero de forma no limitativa metilo, etilo, n-propilo, isopropilo, butilo, isobutilo, sec-butilo, tert-butilo, pentilo, isopentilo, y similares (véase Morrison & Boyd, Organic Chemistr y , 4ª... [Seguir leyendo]
Reivindicaciones:
1. Método de estabilización de una solución acuosa de péptido, polipéptido o proteína, y análogos y/o derivados de los mismos, comprendiendo: la adición de una cantidad de tris (hidroximetil) aminometano a la solución acuosa suficiente para inducir estabilización, donde el tris (hidroximetil) -aminometano es un agente tampón o un aditivo donde la solución acuosa comprende además un modificador orgánico que es seleccionado de: metanol, etanol, 1-propanol, 2-propanol, butanol, hexilenglicol, acetonitrilo y n-metil-2-pirrolidona, y donde el modificador orgánico está presente en una concentración de 1% p/p a 70% p/p.
2. Método según la reivindicación 1, donde el modificador orgánico está presente en una concentración de 1% p/p a 50% p/p.
3. Método según cualquiera de las reivindicaciones 1-2, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 1 mM a 1000 mM.
4. Método según la reivindicación 3, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 1 mM a 200 mM.
5. Método según la reivindicación 3, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 1 mM a 100 mM.
6. Método según la reivindicación 3, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 2 mM a 75 mM.
7. Método según la reivindicación 3, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 3 mM a 50 mM.
8. Método según la reivindicación 3, donde la solución acuosa tiene una concentración de tris (hidroximetil) aminometano de 5 mM a 25 mM.
9. Método según cualquiera de las reivindicaciones 1-8 donde la solución acuosa tiene un pH de 1.0 a 10.0.
10. Método según la reivindicación 9 donde la solución acuosa tiene un pH de 3.0 a 9.5.
11. Método según cualquiera de las reivindicaciones 1-10, donde el péptido, polipéptido o proteína es seleccionado de: péptidos de tipo glucagón (GLPs) y sus análogos y derivados.
12. Método según la reivindicación 11, donde el GLP es seleccionado del grupo: GLP-1 y análogos de GLP-1 y sus derivados, GLP-2 y análogos de GLP-2 y sus derivados, y exendina-4 y sus análogos y derivados.
13. Método según cualquiera de las reivindicaciones 1-11, donde el péptido, polipéptido o proteína es seleccionado de: proinsulinas, insulinas, y sus análogos y derivados.
Patentes similares o relacionadas:
Formulación de inmunoglobulina y procedimiento de preparación de la misma, del 17 de Junio de 2020, de Biogen MA Inc: Una formulación acuosa estable que comprende natalizumab en una concentración de 15 mg/mL a 50 mg/mL, un tampón fosfato, polisorbato 80 en […]
Arginina desiminasa con reactividad cruzada reducida hacia anticuerpos para ADI - PEG 20 para el tratamiento del cáncer, del 6 de Mayo de 2020, de TDW Group: Una composición terapéutica que comprende una arginina desiminasa (ADI) aislada y un vehículo farmacéuticamente aceptable, en donde la ADI aislada comprende la secuencia de […]
Proteínas variantes de empalme her2 y her3 solubles, oligonucleótidos de cambio de empalme y su uso en el tratamiento de enfermedades, del 15 de Abril de 2020, de Sarepta Therapeutics, Inc: Una proteína del receptor 2 del factor de crecimiento epidérmico humano (HER2) aislada y soluble que consiste en la secuencia establecida en la SEQ ID NO: […]
Composiciones y métodos para la distribución de moléculas en células vivas, del 25 de Marzo de 2020, de THE TEXAS A & M UNIVERSITY SYSTEM: Un compuesto que tiene la fórmula: **(Ver fórmula)** En donde X es un resto de unión, Y es un residuo de aminoácido acoplado de forma covalente […]
Nuevas composiciones inmunogénicas para la prevención y tratamiento de enfermedad meningocócica, del 11 de Marzo de 2020, de WYETH HOLDINGS LLC: Una composición que comprende al menos una proteína que comprende una secuencia de aminoácidos que tiene identidad de secuencia mayor de 80 % con la […]
Vacuna peptídica para la prevención e inmunoterapia de demencia del tipo Alzheimer, del 4 de Marzo de 2020, de UNITED BIOMEDICAL, INC.: Una composición que comprende una combinación de construcciones de inmunógenos de péptidos Aβ que consiste en las secuencias de aminoácidos de SEQ […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
Uso de moléculas inhibidoras de semaforina-4D en combinación con una terapia inmunomoduladora para inhibir el crecimiento tumoral y la metástasis, del 8 de Enero de 2020, de Vaccinex, Inc: Un anticuerpo aislado o fragmento de unión a un antígeno del mismo que se une específicamente a semaforina-4D (SEMA4D) para su uso en la inhibición, el retraso o la reducción […]