Sistema mejorado de expresión de pentraxina 3 larga humana y sus usos.
Uso de un vector de expresión eucariótico que comprende una secuencia de nucleótidos que codifica la proteína pentraxina PTX3 larga humana puesta bajo el control de un promotor efectivo y de una secuencia de nucleótidos que codifica un marcador seleccionable,
que tiene esencialmente la secuencia de SEQ ID 1, para transformar una célula anfitriona humana recombinante que ya es capaz de expresar la proteína pentraxina PTX3 larga humana, en donde dicha célula anfitriona humana recombinante es el clon 293F/PTX3/2F12 recombinante depositado en la ECACC con el nº 08011001.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/060469.
Solicitante: SIGMA-TAU INDUSTRIE FARMACEUTICHE RIUNITE S.P.A..
Nacionalidad solicitante: Italia.
Dirección: VIALE SHAKESPEARE 47 00144 ROMA ITALIA.
Inventor/es: CASSANI, GIOVANNI, SASSANO,MARICA, ESPOSITO,ADELAIDE, RIVIECCIO,VINCENZO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/67 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Métodos generales para favorecer la expresión.
- C12N15/79 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a huéspedes eucariotas.
- C12N5/16 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células animales.
PDF original: ES-2432242_T3.pdf
Fragmento de la descripción:
Sistema mejorado de expresión de pentraxina 3 larga humana y sus usos
CAMPO DEL INVENTO
El presente invento se refiere a un sistema celular derivado de seres humanos, capaz de expresar altos niveles de la proteína pentraxina 3 humana (hPTX3) , a unos métodos y al material usado.
ANTECEDENTES DEL INVENTO
La pentraxina 3 larga humana, PTX3 o hPTX3 (número de acceso en el GeneBank BD 131701) es una glicoproteína multimérica que se compone de ocho subunidades engarzadas por puentes de disulfuro.
Los autores del presente invento ya han diseñado un sistema de expresión para la producción de la PTX3 en el linaje de células humanas HEK293F. Este sistema está basado en un plásmido que contiene el gen de resistencia a neomicina, en donde el gen de PTX3 está puesto bajo el control de una secuencia del promotor de ubiquitina C humana. Dicho sistema evita la formación potencial de una PTX3 quimérica derivada de una producción endógena de PTX3 por un linaje de células de origen no humano. El clon aislado mejor productor, denominado 2F12, se seleccionó entre los que se habían obtenido. Se obtuvo una producción de aproximadamente 20 mg/l de PTX3, que no era suficiente para las necesidades de producción a escala comercial.
Con la meta de aumentar los niveles de expresión de PTX3, los autores del presente invento han construido un plásmido en el que el gen de PTX3 estaba bajo el control de promotor de CMV. El plásmido se usó para volver a transfectar el clon 2F12 que expresa la PTX3. El nivel de productividad detectado en los nuevos transfectomas aislados era más alto que lo esperado, a saber alrededor de 80 mg/l.
DESCRIPCIÓN DEL INVENTO
Se obtuvo un clon de origen humano que expresaba altos niveles de la PTX3 humana usando una estrategia experimental que incluía las siguientes etapas:
a) la construcción de unas casetes de expresión de plásmidos que son portadoras de la PTX3 humana bajo el control de un promotor de CMV (citomegalovirus) ;
b) la inserción de la casete de resistencia a higromicina en dicho plásmido, con el fin de seleccionar unos transfectomas estables que se originan a partir de una transfección renovada del clon G418 resistente que expresa la PTX3;
c) la modificación de la identidad y de los niveles de las proteínas recombinantes expresadas;
d) la caracterización bioquímica de la hPTX3 recombinante.
El contenido del documento de solicitud de patente internacional PCT/EP2009/050937 se incorpora a la presente memoria descriptiva por su referencia.
Es un objeto del invento el uso de un vector de expresión eucariótico que comprende una secuencia de nucleótidos que codifica la proteína pentraxina PTX3 larga humana bajo el control de un promotor efectivo y de una secuencia de nucleótidos que comprende un marcador seleccionable, que tiene esencialmente la secuencia de SEQ ID 1, para transformar a una célula anfitriona humana recombinante que ya es capaz de expresar la proteína pentraxina PTX3 larga humana, en donde la célula anfitriona humana recombinante es el clon 293F/PTX3/2F12 recombinante depositado en la ECACC con el nº 08011001. En un aspecto particular, el vector está linealizado.
Otro objeto del invento es una célula humana recombinante transformada que es capaz de expresar la proteína pentraxina PTX3 larga humana que es el clon 293F/PTX3/2F12 recombinante depositado en la ECACC bajo el nº 08011001, transformado adicionalmente por uso del vector que más arriba se ha descrito. En una forma preferida de realización, la célula humana recombinante transformada es el clon MS24PTX recombinante depositado en la Health Protection Agency, Culture Collections Centre For Emergency Preparedness and Response Salisbur y UK [Agencia de Protección de la Salud, Centro de Colecciones de Cultivo para Preparación y Respuesta de Emergencia], Salisbur y , Reino Unido, con el nº 09072902.
Otro aspecto del invento es el uso de la célula recombinante humana transformada, que más arriba se ha descrito, para la producción de la proteína pentraxina PTX3 larga humana.
Otro objeto del invento es un procedimiento para la producción de la proteína pentraxina PTX3 larga humana recombinante que comprende:
a) transfectar una célula humana recombinante que ya expresa la proteína pentraxina PTX3 larga humana recombinante, con un plásmido seleccionable en el que el gen de la pentraxina larga humana está puesto bajo el control del promotor de CMV;
b) seleccionar y cultivar la célula humana recombinante transfectada;
c) purificar la proteína pentraxina PTX3 larga humana a partir del medio de cultivo de la célula humana recombinante transfectada,
en donde la célula humana recombinante que ya expresa la proteína PTX3 pentraxina larga humana recombinante es el clon 293F/PTX3/2F12 depositado en la ECACC bajo el nº 08011001. De manera preferible, la célula humana recombinante transfectada es el clon MS24PTX recombinante depositado en la Health Protection Agency, Culture Collections Centre For Emergency Preparedness and Response Salisbur y UK Salisbur y , Reino Unido, con el nº 09072902.
En una forma preferida de realización, la etapa de purificación incluye por lo menos una de las siguientes etapas: una cromatografía de intercambio aniónico, una cromatografía con hidroxiapatito o una cromatografía de exclusión por tamaños.
El invento será ilustrado ahora por medio de unos Ejemplos no limitadores, refiriéndose en particular a las siguientes figuras:
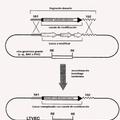
Figura 1: mapa y características principales del pSASSI-hPTX3
Figura 2: crecimiento, viabilidad y productividad en un matraz de agitación de (A) el clon MS24PTX y (B) el clon 293F/PTX3/2F12.
Figura 3: caracterización por el gradiente de SDS-PAGE 4-15% (A) y de cromatografía de exclusión por tamaños (B) de la PTX3 humana recombinante purificada a partir del clon MS24PTX.
Figura 4: capacidad de fijación de FGF2 del clon de hPTX3 293F/PTX3/2F12 y del clon de hPTX3 MS24PTX.
Figura 5: mapa y características principales de pSC1-hPTX3.
EJEMPLOS
Ejemplo 1: clon 293F/PTX3/2F12
Construcción del plásmido pSC1-PTX3
1. Construcción del pSG/Ub
1.1 Preparación de la secuencia del promotor de ubiquitina C humana El promotor de ubiquitina C humana se toma a partir del plásmido pUB/Bsd (de Invitrogen, nº de catálogo V512-20) , por amplificación con una PCR (= acrónimo de Polymerase Chain Reaction = reacción en cadena de la polimerasa) . Como una parte de la estrategia de clonación, se introducen en ambos extremos unas secuencias de reconocimiento por endonucleasas de restricción. Se construyen un sitio BsaAI en el cebador de amplificación situado secuencia arriba y un sitio EcoRI en el cebador situado secuencia abajo. La región amplificada corresponde a los nucleótidos 1.941 hasta 3.161 en la secuencia de pUB/Bsd.
Los oligonucleótidos se designan de la siguiente manera:
5’p UbC: longitud: 26mero (SEQ ID 3) ATATCACGTG ATC TGG CCT CCG CGC C
3’p UbC: longitud: 23mero (SEQ ID 4) GGAATTC GGT CCG GTC TAA CAA A
El protocolo para la amplificación es el siguiente: 1 ng/µl de un ADN plasmídico, 2 mM de MgCl2, 0, 2 mM de dNTP’s, 400 nM de cada cebador, 1X del tampón suministrado y 0, 04 u/ml de la polimerasa de ADN de Taq (de Sigma Genosys) ; perfil de temperaturas: 3 min. a 94ºC, 30 veces (30 s (segundos) a 94ºC, 30 s a 46ºC, 2 min. a 72ºC) , 5 min. a 72ºC, enfriamiento a 4ºC hasta el uso ulterior.
El producto de la amplificación (con un tamaño de 1.238 pb = pares de bases) se purifica mediante una columna de centrifugación con una membrana de sílice (NucleoSpin, de Macher y -Nagel GmbH & Co.) , se liga en el vector pGEM-T (de Promega nº de catálogo A1360) y se transforma en el seno de la cepa anfitriona de E.coli HB2151 (de Pharmacia Biotech) . Los transformantes se seleccionan por el crecimiento en un medio LB suplementado con 50 mg/l de ampicilina.
Los ADN plasmídicos, aislados a partir de las colonias resistentes a la ampicilina, se comprueban mediante un análisis por restricción con las enzimas StuI más SacI (se esperan unos fragmentos de ~ 3.650 y 600 pb) .
Los plásmidos que muestran el modelo de restricción correcto se comprueban adicionalmente mediante un análisis de la secuencia del inserto entero y subsiguientemente se digieren con las enzimas de restricción EcoRI (de Sigma-Genosys) y BsaAI (de New England Biolabs) .
El promotor de ubiquitina C humana se purifica mediante una separación en un gel de agarosa y una elución en una columna de centrifugación con una membrana de sílice.
1.2 Preparación del fragmento del... [Seguir leyendo]
Reivindicaciones:
1. Uso de un vector de expresión eucariótico que comprende una secuencia de nucleótidos que codifica la proteína pentraxina PTX3 larga humana puesta bajo el control de un promotor efectivo y de una secuencia de nucleótidos que codifica un marcador seleccionable, que tiene esencialmente la secuencia de SEQ ID 1, para transformar una célula anfitriona humana recombinante que ya es capaz de expresar la proteína pentraxina PTX3 larga humana, en donde dicha célula anfitriona humana recombinante es el clon 293F/PTX3/2F12 recombinante depositado en la ECACC con el nº 08011001.
2. El uso del vector de acuerdo con la reivindicación 1, en el que el vector está linealizado.
3. Una célula humana recombinante transformada que es capaz de expresar la proteína pentraxina PTX3 larga humana, que es el clon 293F/PTX3/2F12 depositado en la ECACC con el nº 08011001 transformado ulteriormente por uso del vector de acuerdo con la reivindicación 1.
4. La célula humana recombinante transformada de acuerdo con la reivindicación 3, que es el clon MS24PTX recombinante depositado en la Health Protection Agency, Culture Collections Centre For Emergency Preparedness and Response Salisbur y , Reino Unido, con el nº 09072902.
5. Uso de la célula humana recombinante transformada de acuerdo con la reivindicación 3 ó 4 para la producción de la proteína pentraxina PTX3 larga humana.
6. Un procedimiento para la producción de la proteína pentraxina PTX3 larga humana que comprende
a) transfectar una célula humana recombinante que ya expresa la proteína pentraxina PTX3 larga humana recombinante, con un plásmido en el que el gen de la pentraxina larga humana está puesto bajo el control del promotor de CMV;
b) seleccionar y cultivar la célula humana recombinante transfectada;
c) purificar la proteína pentraxina PTX3 larga humana a partir del medio de cultivo de la célula humana recombinante transfectada,
en donde la célula humana recombinante que ya expresa la proteína pentraxina PTX3 larga humana recombinante es el clon 293F/PTX3/2F12 recombinante depositado en la ECACC bajo el nº 08011001.
7. El procedimiento de acuerdo con la reivindicación 6, en el que la célula humana recombinante transfectada es el clon MS24PTX depositado en la Health Protection Agency, Culture Collections Centre For Emergency Preparedness and Response Salisbur y , Reino Unido, con el nº 09072902.
8. El procedimiento de la reivindicación 6 ó 7, en el que la etapa de purificación incluye por lo menos una de las siguientes etapas: cromatografía con intercambio aniónico, cromatografía con hidroxiapatito o cromatografía de exclusión por tamaños.
Patentes similares o relacionadas:
Métodos mejorados para producir terapias celulares adoptivas, del 22 de Abril de 2020, de Bluebird Bio, Inc: Un método in vitro para producir un producto terapéutico de células T que comprende: a) proporcionar una población de células mononucleares […]
Anticuerpos anti-ricina y sus usos, del 8 de Abril de 2020, de HER MAJESTY THE QUEEN IN RIGHT OF CANADA AS REPRESENTED BY THE MINISTER OF NATIONAL DEFENCE: Un anticuerpo, aislado o purificado, o fragmento de este, que comprende una cadena ligera variable que comprende una CDR L1 de secuencia KASQDINNYLR […]
Usos de anticuerpos IL-1 alfa, del 18 de Marzo de 2020, de XBIOTECH, INC: Un método para cuantificar la cantidad de IL-1α en una muestra biológica, el método comprendiendo las etapas de: (a) separar una muestra biológica […]
Uso de moléculas inhibidoras de semaforina-4D en combinación con una terapia inmunomoduladora para inhibir el crecimiento tumoral y la metástasis, del 8 de Enero de 2020, de Vaccinex, Inc: Un anticuerpo aislado o fragmento de unión a un antígeno del mismo que se une específicamente a semaforina-4D (SEMA4D) para su uso en la inhibición, el retraso o la reducción […]
Sistemas y procedimientos de anticuerpos anti-SOX10, del 11 de Diciembre de 2019, de Biocare Medical, LLC: Preparación aislada de un anticuerpo monoclonal de ratón que se une específicamente a una proteína SOX10, en la que dicho anticuerpo monoclonal de […]
 Producción de células provenientes de líneas neurales a partir de sangre, del 25 de Septiembre de 2019, de KWALATA TRADING LIMITED: Una composición de materia, derivada por la estimulación in vitro de una población de células centrales (CCP) derivada de la sangre de al menos 5 millones […]
Producción de células provenientes de líneas neurales a partir de sangre, del 25 de Septiembre de 2019, de KWALATA TRADING LIMITED: Una composición de materia, derivada por la estimulación in vitro de una población de células centrales (CCP) derivada de la sangre de al menos 5 millones […]
 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de polipéptidos recombinantes, del 12 de Junio de 2019, de MEDIMMUNE, LLC: Un método para producir un polipéptido recombinante en un cultivo celular de ovario de hámster chino (CHO), comprendiendo el método: (a) cultivar células CHO que tienen […]