Proteína de fusión de somatostatina deficiente en cloranfenicol acetiltransferasa (CAT) y el uso de ésta en ganado vacuno vacuno.
Un polipéptido quimérico que tiene la inmunogenicidad de la somatostatina,
que comprende: una secuencia deaminoácido de la somatostatina-14 ligada a un polipéptido de cloranfenicol acetiltransferasa truncado ysustancialmente inactivo en donde la somatostatina-14 se liga a la cloranfenicol acetiltransferasa inactiva medianteun espaciador, en donde la cloranfenicol inactiva tiene al menos 193 residuos de histidina reemplazados con unaalanina, glicina u otro aminoácido de este tipo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/068195.
Solicitante: Braasch Biotech LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 421 Rose Avenue Garretson, SD 57030 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MENDELSOHN,ANDREW R, HAFFER,KEITH N, LARRICK,JAMES.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/31 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Somatostatinas.
- A61K39/385 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Haptenos o antígenos, unidos a soportes.
- C07K14/655 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Somatostatinas.
- C12P21/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › que tienen una secuencia conocida de varios aminoácidos, p. ej. glutation.
PDF original: ES-2445403_T3.pdf
Fragmento de la descripción:
Proteina de fusion de somatostatina deficiente en cloranfenicol acetiltransferasa (CAT) y el uso de esta en ganado vacuno Campo tecnico La presente invencion se refiere a polipeptidos quimericos a base de somatostatina, y a los usos de los mismos. La presente invencion tambien se refiere a nuevos adyuvantes y composiciones de inmunizacion para mejorar la inmunogenicidad de, por ejemplo, polipeptidos quimericos a base de somatostatina de la invencion asi como a otros antigenos de este tipo.
Antecedentes de la invencion La somatostatina (tambien conocida como hormona inhibidora de la hormona de crecimiento o GHIH) es una hormona peptidica producida en el hipotalamo asi como ciertas partes del sistema digestivo. La somatostatina generalmente se implica en la regulacion del sistema endocrino a traves de interacciones con los receptores de la somatostatina acoplados a la proteina G. Esta cascada de senalizacion basada en la somatostatina conduce a un numero de acciones extendidas por todo el cuerpo.
Pertinente para los aspectos de la presente invencion, se sabe que la somatostatina inhibe la liberacion de la hormona de crecimiento y la hormona estimulante de la tiroides de la pituitaria anterior. (Patel YC and Srikant CB, Somatostatin and its receptors Adv Mol Cell Endocrinol, 1999, 3 43-73) . Otras hormonas inhibidas por la somatostatina incluyen la insulina, el glucagon, secretina, gastrina, pepsina, maletina, etc. (Patel YC and Srikant CB, Somatostatin and its receptors Adv Mol Cell Endocrinol, 1999, 3 43-73) . La capacidad de la somatostatina para regular muchos factores/hormonas necesarias para el crecimiento y la utilizacion de alimentos ha hecho de la somatostatina un objetivo central para el control del crecimiento de animales en el campo de la cria de animales, i.e., la inhibicion de la somatostatina da lugar a que mayores niveles de la hormona de crecimiento esten presentes en un animal objetivo y por lo tanto da lugar a animales con una capacidad mayor para producir leche, para proveer mayores cantidades de carne, etc.
En particular, se ha reconocido la inmunizacion de los animales a la somatostatina como un medio de neutralizacion de la somatostatina en un animal objetivo y eliminando asi los efectos inhibidores normales de la somatostatina sobre diversos aspectos de la productividad del animal, por ejemplo, produccion de leche en una vaca lechera. Reichlin S., ed., 1987, Somatostatin, Basic and Clinical Status, Plenum Press, New York (pp 3-50, 121-136, 146-156, 169-182, 221-228, 267-274) Spencer G.S., 1985, Hormonal systems regulating growth, review, Livestock Production Science, 12, 31-46. Es importante destacar que, estos procedimientos de inmunizacion basados en la somatostatina evitan el uso directo de hormonas anabolicas, por ejemplo, hormona de crecimiento, y similares, en el animal y permiten pequenos cambios en la concentracion de los factores anabolicos endogenos y por consiguiente productos alimenticios ecologicamente puros.
Se sabe que la somatostatina tiene una vida media relativamente corta en la sangre. Con el fin de mejorar los efectos inmunologicos de la somatostatina, se han desarrollado los protocolos de inmunizacion para mejorar la vida media de las proteinas por medio de la conjugacion de la somatostatina con proteinas portadoras diana. Estas proteinas de somatostatina conjugadas estan disenadas para tener una mayor vida media y una mayor antigenicidad en la sangre y por consiguiente proveer beneficios mejorados (especialmente a la luz de los costos de preparacion de la somatostatina) . Por ejemplo, las proteinas quimericas de la somatostatina se revelan en U.S. Patent No.
6, 316, 004, (y la correspondiente European Patent EP0645454) donde se muestra que diferentes conjugados de proteinas que contienen somatostatina tienen una mayor antigenicidad y funcion con respecto a la productividad de animales de granja en comparacion con otros procedimientos de inmunizacion convencional o basados en hormonas anabolicas.
Sin embargo, se necesitan dosis mas bajas, procedimientos y composiciones de inmunizacion a basados en un 45 antigenicidad mayor, para mejorar una productividad total y rapidez en el campo de la cria de animales. La presente invencion esta dirigida a proveer estos procedimientos, composiciones y compuestos de inmunizacion basados en somatostatina funcionalmente activa y mas antigenicos.
En este contexto, se proporciona la siguiente divulgacion.
Resumen de la invencion 50 La presente invencion provee nuevos polipeptidos que tienen una mayor inmunogenicidad de la somatostatina. Los polipeptidos de la invencion incluyen somatostatina-14 fusionada a una proteina cloranfenicol acetiltransferasa inactivada sustancialmente a traves de un ligador funcionalmente optimizado. Los polipeptidos quimericos de la
invencion proveen materiales de bajo costo y altamente efectivos, para utilizar en el campo de la cria de animales, como se describe con mas detalle a continuacion. Las modalidades de la invencion incluyen las secuencias de aminoacidos como se definen en SEQ ID NOs: 3, 7, 8, 10, 11 y 13.
En este documento se describen los procedimientos de produccion y purificacion para la fabricacion de los polipeptidos quimericos en una condicion libre de endotoxina y altamente funcional. Los polipeptidos libres de endotoxina proveen una ventaja sustancial e inesperada para utilizar en ciertos animales objetivos, donde las cantidades pequenas de endotoxina, normalmente concebidas ventajosas para provocar una respuesta inmunogenica, actualmente conducen a una desventaja funcional significante. Este es particularmente el caso cuando los polipeptidos de la invencion se utilizan para inmunizar vacas lecheras criadas y reproducidas en los Estados Unidos. Ademas, debido a que los polipeptidos quimericos de la invencion muestran una funcion mejorada en comparacion con los materiales convencionales, se utiliza un numero de dosis inferior y mas pequeno, para inmunizar a los animales objetivo. Esta disminucion en las cantidades requeridas tambien provee una resultante reduccion de la endotoxina en las vacunas de la invencion. La combinacion de un aislado libre de endotoxina y una menor cantidad utilizada de los polipeptidos quimericos de la invencion, permite que vacunas sustancialmente libres de endotoxina sean utilizadas en este documento.
La invencion tambien provee composiciones de adyuvantes que tienen una mayor seguridad y funcion en comparacion con los materiales adyuvantes convencionales. Los adyuvantes en este documento no contienen materiales derivados de animales y son libres de carcinogenos quimicos mas conocidos, por ejemplo, el benceno y otros materiales similares. Se ha demostrado que las composiciones de adyuvantes en este documento son inesperadamente efectivas para provocar la respuesta inmune cuando se combina con antigenos diana.
La invencion ademas provee las vacunas que contienen los polipeptidos quimericos de la invencion con las composiciones de adyuvantes de la invencion. En este documento, las vacunas se utilizan para inducir respuestas inmunes en aves y mamiferos vacunados, por ejemplo, animales objetivos de granja. Los animales de granja ilustrativos para utilizar en este documento incluyen: vacas lecheras, cerdos, ovejas, cabras, pavos, conejos, y terneros. En algunos aspectos los polipeptidos de la invencion se preparan y purifican con baja o ninguna endotoxina asociada. Estas vacunas se han optimizado para provocar reacciones inmunogenicas seguras y mejoradas en el animal objetivo.
La invencion ademas incluye los metodos para la vacunacion de aves y mamiferos diana utilizando las vacunas de la invencion. Se proporcionan los metodos ilustrativos de vacunacion de vacas lecheras para mejorar la produccion de leche de una manera segura (tanto para los animales como para el usuario final) , rentable y de gran utilidad. Otros metodos ilustrativos incluyen vacunacion de cerdos, ovejas, pavos, cabras, conejos o terneros para mejorar la produccion de carne (y particularmente carne magra) en un animal objetivo de manera segura y rentable.
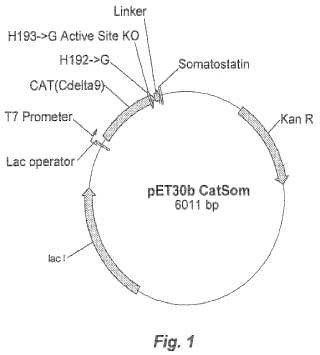
Estas y otras diferentes caracteristicas y ventajas de la invencion seran aparentes a partir de una lectura de la siguiente descripcion detallada y una revision de las reivindicaciones anexas Breve descripcion de los dibujos Figura 1 es un esquema ilustrativo de un plasmido pET30b CatSom de acuerdo con las modalidades de la presente invencion. El plasmido incluye un marcador de resistencia de la canamicina, un operador Lac, promotor T7, secuencia codificante de CAT, todas de acuerdo con las modalidades de la invencion, tambien se incluyen una region ligadora de acuerdo con la invencion en este documento y una region codificante de la somatostatina de acuerdo con la invencion.
Figura 2 es un SDS-PAGE tenido ilustrativo que muestra una... [Seguir leyendo]
Reivindicaciones:
1. Un polipeptido quimerico que tiene la inmunogenicidad de la somatostatina, que comprende: una secuencia de aminoacido de la somatostatina-14 ligada a un polipeptido de cloranfenicol acetiltransferasa truncado y sustancialmente inactivo en donde la somatostatina-14 se liga a la cloranfenicol acetiltransferasa inactiva mediante un espaciador, en donde la cloranfenicol inactiva tiene al menos 193 residuos de histidina reemplazados con una alanina, glicina u otro aminoacido de este tipo.
2. El polipeptido quimerico de la reivindicacion 1, en donde el espaciador tiene una secuencia de aminoacido de SEQ ID NO: 10 o SEQ ID NO: 11.
3. El polipeptido quimerico de la reivindicacion 1, en donde el polipeptido de cloranfenicol acetil transferasa truncado y sustancialmente inactivo tiene una secuencia de aminoacido de SEQ ID NO: 3, SEQ ID NO: 7 o SEQ ID NO 8.
4. El polipeptido quimerico de la reivindicacion 1, que tiene una secuencia de aminoacido con al menos 99% de identidad de la secuencia con la secuencia de aminoacido de SEQ ID NO: 13.
5. El polipeptido quimerico de la reivindicacion 1, que tiene una secuencia de aminoacido de SEQ ID NO: 13.
6. Una composicion inmunogenica que comprende el polipeptido quimerico de la reivindicacion 1, junto con un adyuvante farmaceuticamente apropiado en una cantidad efectiva para provocar una respuesta inmune.
7. Una composicion inmunogenica, que comprende el polipeptido quimerico de la reivindicacion 1, junto con un adyuvante en donde el adyuvante comprende una emulsion aceite-en-agua mezclada con una premezcla de emulsion en donde la emulsion aceite-en-agua comprende un aceite mineral, Tween 80, Span 85 y uno o mas polimeros y en donde la premezcla de emulsion comprende un polimero de alto peso molecular, un agente tensoactivo y un emulsificante en una base oleosa acuosa.
8. Un metodo no-terapeutico para aumentar la produccion de leche en vacas lecheras, que comprende:
vacunar una vaca lechera con una o mas dosis de la composicion de la reivindicacion 6; y
dejar por lo menos diez dias, durante los cuales la produccion de leche de las vacas lecheras aumentara en comparacion con la misma produccion de leche de vaca en la ausencia de la vacunacion.
9. El metodo de la reivindicacion 8, en donde la vaca lechera se vacuna con solo una dosis de la composicion de la reivindicacion 6.
10. Un metodo no-terapeutico para aumentar la produccion de leche en vacas lecheras que comprende:
vacunar una vaca lechera con una o mas dosis de la composicion de la reivindicacion 7; y
dejar por lo menos diez dias, durante los cuales la produccion de leche de las vacas lecheras aumentara en comparacion con la misma produccion de leche de vaca en la ausencia de la vacunacion.
11. Un metodo no-terapeutico para aumentar la produccion de carne magra en ganaderia de granja, que comprende vacunar la ganaderia de granja con la composicion de la reivindicacion 7.
Patentes similares o relacionadas:
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
PROCEDIMIENTO DE OBTENCIÓN DE SUBPRODUCTOS A PARTIR DE RESIDUOS DE CAFÉ Y APLICACIONES DE LOS MISMOS, del 13 de Julio de 2020, de UNIVERSIDAD DE GRANADA: Procedimiento de obtención de subproductos a partir de residuos de café y aplicaciones de los mismos. La presente invención consiste en un proceso […]
Biblioteca de péptidos y su uso, del 8 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Una biblioteca de péptidos que comprende una pluralidad de péptidos diferentes en la que los péptidos comprenden cada uno una secuencia de aminoácidos […]
Métodos para controlar la producción de proteasas, del 1 de Julio de 2020, de ROAL OY: Una célula hospedadora que comprende al menos un gen cromosómico inactivado en donde el gen cromosómico inactivado comprende una secuencia de ácido nucleico que codifica un […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Proceso para la purificación de daptomicina, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina que comprende: a) someter a la daptomicina a condiciones en las que una solución micelar de daptomicina se forma alterando el pH; y […]
Lipopéptidos de alta pureza, micelas de lipopéptidos y procesos para preparar los mismos, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina a partir de moléculas o agregados de alto peso molecular, en donde la daptomicina se proporciona en forma micelar, dicho […]
Métodos para ajustar los niveles de producción de carotenoides y composiciones en géneros de Rhodosporidium y Rhodotorula, del 15 de Abril de 2020, de TEMASEK LIFE SCIENCES LABORATORY LIMITED: Un método para ajustar el nivel de producción y la composición de carotenoides en un huésped fúngico que comprende: (a) manipular genéticamente […]