Proceso para la preparación de glicopéptidos que tienen oligosacáridos unidos a asparagina.
Proceso para la síntesis en fase sólida de un glicopéptido que tiene al menos un oligosacárido unido auna asparagina en una posición deseada de la cadena peptídica del mismo,
el proceso comprende lasetapas de:
(1) esterificación de un grupo hidroxilo de una resina que tiene el grupo hidroxilo y un grupocarboxilo de un aminoácido que tiene un nitrógeno del grupo amino protegido por un grupoprotector liposoluble,
(2) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(3) amidación del grupo amino libre y de un grupo carboxilo de un aminoácido que tiene unnitrógeno de grupo amino protegido por un grupo protector liposoluble,
(4) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(5) repetición de las etapas (3) y (4) al menos una vez,
(6) preparación de un disialooligosacárido unido a una asparagina o un
monosialooligosacárido unido a una asparagina que tiene los grupos hidroxilos noprotegidos y que tiene un nitrógeno del grupo amino protegido por un grupo protectorliposoluble y el grupo carboxilo del ácido siálico protegido por un grupo bencilo, alilo odifenilmetilo,
(7) amidación del grupo amino libre y de un grupo carboxilo de la porción asparagina deldisialooligosacárido unido a una asparagina o del monosialooligosacárido unido a unaasparagina que tiene un nitrógeno del grupo amino protegido por un grupo protectorliposoluble y el grupo carboxilo del ácido siálico protegido por un grupo bencilo, alilo odifenilmetilo,
(8) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(9) amidación del grupo amino libre y un grupo carboxilo de un aminoácido que tiene unnitrógeno del grupo amino protegido por un grupo protector liposoluble,
(10) repetición de las etapas (8) y (9) al menos una vez,
(11) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(12) corte de la resina con un ácido.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2003/008551.
Solicitante: Glytech, Inc.
Nacionalidad solicitante: Japón.
Dirección: 134, Chudoji minami-machi, Shimogyo-ku, Kyoto-shi Kyoto 600-8813 JAPON.
Inventor/es: KAJIHARA,YASUHIRO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K5/103 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › la cadena lateral del primer aminoácido es acíclica, p. ej. Gly, Ala.
- C07K9/00 C07K […] › Péptidos de hasta 20 aminoácidos, que contienen radicales sacáridos y una secuencia totalmente determinada; Sus derivados.
- C08B37/00 C […] › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
PDF original: ES-2449495_T3.pdf
Fragmento de la descripción:
Proceso para la preparación de glicopéptidos que tienen oligosacáridos unidos a asparagina ÁREA TÉCNICA
La presente invención se refiere a un proceso para preparar glicopéptidos que tienen oligosacáridos 5 unidos a asparagina en la cadena peptídica de los mismos, y a glicopéptidos que pueden obtenerse mediante el proceso.
ANTECEDENTES DE LA TÉCNICA
En los últimos años, las moléculas de oligosacáridos han llamado la atención como moléculas de vida de cadena tercera seguidas de ácidos nucleicos (ADN) y proteínas. El cuerpo humano es una sociedad de células enorme que comprende aproximadamente 60 trillones de células, y las superficies de todas las células están cubiertas con moléculas de oligosacáridos. Por ejemplo, los grupos sanguíneos ABO se determinan según la diferencia de oligosacáridos sobre las superficies de las células.
Los oligosacáridos funcionan en relación con el reconocimiento de células e interacción de células y son sustancias claves para el establecimiento de la sociedad celular. El ruido en la sociedad celular conlleva, por
ejemplo, cánceres, enfermedades crónicas, enfermedades infecciosas y envejecimiento.
Por ejemplo, se sabe que, cuando las células desarrollan cáncer, tienen lugar cambios en la estructura de los oligosacáridos. También se sabe que el Vibrio cholerae, los virus gripales, etc. acceden a las células y provocan infecciones al reconocer y unirse a un oligosacárido específico.
La aclaración de las funciones de los oligosacáridos conlleva el desarrollo de productos farmacéuticos y
alimentos basados en nuevos principios, lo que contribuye a la prevención y terapia de las enfermedades, y se espera una amplia variedad de aplicaciones de los oligosacáridos.
La estructura de los oligosacáridos es mucho más compleja que la de los ácidos nucleicos o proteínas por la diversidad de disposiciones de los azúcares simples, modos o sitios de enlaces, longitud de las cadenas, formas de las ramas y de las estructuras globales de nivel superior. En consecuencia, la información biológica derivada de las estructuras de los mismos es más diversificada que en el caso de los ácidos nucleicos y proteínas. Aunque se ha reconocido la importancia de la investigación sobre los oligosacáridos, la complejidad y variedad de las estructuras de los mismos han retrasado el progreso en la investigación de oligosacáridos a diferencia de los estudios sobre los ácidos nucleicos y las proteínas.
Muchas de las proteínas presentes en las superficies de las membranas celulares o en el suero tienen oligosacáridos unidos a las mismas como se describe anteriormente. Las moléculas en las que se combinan de manera covalente los oligosacáridos con proteínas se denominan glicoproteínas, que pueden dividirse en dos grupos según la diferencia en el modo de enlace entre el oligosacárido y la proteína. Los oligosacáridos de un tipo son oligosacáridos unidos a asparagina (tipo de enlace N-glicósido) donde un grupo amino de la cadena lateral de asparagina (Asn) está unido al oligosacárido. Los oligosacáridos de otro tipo son oligosacáridos unidos a mucina (tipo de enlace O-glicósido) donde el oligosacárido está unido al alcohol de serina (Ser) o treonina (Thr) . Todos los oligosacáridos unidos a asparagina tienen una estructura principal básica que comprende cinco residuos de azúcar, y están divididos en subgrupos de tipo alta manosa, de tipo compuesto y de tipo mezcla, de acuerdo con el tipo de residuo de azúcar terminal no reductor del oligosacárido unido. Por otro lado, los oligosacáridos unidos a mucina se dividen en cuatro grupos según la diferencia de la estructura principal básica.
El proceso para preparar péptidos de uso generalizado en la actualidad es el proceso de síntesis en fase sólida desarrollado por R. B. Merrifield en 1963. El proceso de síntesis en fase sólida es en el que los aminoácidos están unidos a una fase sólida llamada resina para proporcionar una cadena peptídica alargada. Cuando está completamente extendida, la cadena de péptidos se corta desde la fase sólida para obtener el producto deseado. Como aplicación de este proceso, puede preparase una cadena de glicopéptidos 45 incorporando un aminoácido que tenga un oligosacárido unido al mismo en la cadena peptídica para ser alargada.
En consecuencia, las cadenas de glicopéptidos se preparan ampliamente mediante el uso de oligosacáridos unidos a aminoácidos donde un oligosacárido está unido a Asn o Ser (Thr) para la preparación de péptidos. No obstante, hay pocos ejemplos de cadenas peptídicas preparadas químicamente que tienen una 50 gran cadena de azúcar a pesar del progreso técnico en la síntesis química.
Uno de los problemas que se genera son las cantidades absolutas insuficientes de oligosacáridos para ser unidos con el residuo de asparagina. Los métodos para obtener oligosacáridos incluyen el aislamiento de oligosacáridos solo a partir de glicoproteínas que están presentes en un organismo vivo. No obstante, utilizar hidracina para cortar oligosacáridos a partir de glicoproteínas es arriesgado, presenta dificultad en la preparación de grandes cantidades de oligosacáridos. Además, en el organismo vivo hay muchos oligosacáridos que se parecen mucho en la estructura, y es difícil obtener sólo un oligosacárido único. Por otro lado, puesto que la descomposición de hidracina libera el oligosacárido del residuo de asparagina, surge la necesidad de unir el oligosacárido liberado con el residuo de asparagina de nuevo, de ahí el incremento de pasos necesarios.
En la síntesis química de oligosacáridos, hay ejemplos de preparar oligosacáridos en los que se unen 10 residuos de azúcar, mientras que muchos de estos casos son así que el oligosacárido deseado puede prepararse en una cantidad de sólo varios miligramos durante un año. Por esta razón, surgen dificultades en la preparación química de oligosacáridos.
El segundo de los problemas está relacionado con el tratamiento llevado a cabo con el uso de TFA (ácido trifluoroacético) para cortar la cadena peptídica a partir de la fase sólida. Por ejemplo, el ácido siálico presente en los extremos no reductores de los oligosacáridos se hidroliza fácilmente en condiciones ácidas, de modo que existe la posibilidad de que el tratamiento con TFA cortará el ácido siálico del glicopéptido preparado. En consecuencia, no existe casi ningún caso en el que los oligosacáridos que tienen ácido siálico sean usados para la síntesis en fase sólida. Con el fin de resolver este problema, se ha expuesto un proceso en el que el ácido siálico es transferido a un oligosacárido con transferasa de ácido siálico después de la síntesis de péptidos. Aunque es útil para introducir ácido siálico, este proceso todavía presenta el problema de que surgen dificultades al preparar glicopéptidos en grandes cantidades porque la transferasa es cara.
No obstante, como se describe a continuación, la presente invención ha posibilitado la preparación de modo artificial de glicopéptidos en grandes cantidades. Por tanto, hace posible introducir de modo industrial ácido siálico o derivados del mismo en oligosacáridos empleando transferasa de ácido siálico.
Aunque existen oligosacáridos de origen natural que tienen ácido siálico enlazado a los mismos, los oligosacáridos que presentan derivados de ácido siálico unidos a estos no están disponibles de modo natural.
Por eso, es a través del uso de transferasa de ácido siálico como los derivados de ácido siálico pueden introducirse en los oligosacáridos de cualquiera modo.
E. Meinjohanns et al., J. Chem. Soc., Perkin Trans.1., 1, 549-560 (1998) describe la síntesis de glicopéptidos N-ligados empleando métodos estándares de síntesis en fase sólida y empleando componentes básicos de aminoácidos Fmoc-Asn (azúcar) y una resina HPMA-PEGA. Después de liberarse de la resina, los glicopéptidos obtenidos pueden ser modificados por una sialil-transferasa.
También se presentan métodos similares que emplean resina funcionalizada con amino en lugar de resina funcionalizada con hidroxilo y que lleva a glicopéptidos que tienen un grupo amido de extremo C-terminal, p.ej., en L. Otvos Jr. et al., Tetrahedron Lett. 31, 5889-5892 (1991) ; L. Urge et al., Tetrahedron Lett. 32, 3445-3448 (1991) ; L. Urge et al., Carbohydrate Res. 235, 83-93 (1992) ; I. Laczko et al., Biochemistr y 31, 4282-4288 (1992) y
L. Urge et al., Tetrahedron Lett. 50, 2373-2390 (1994) .
T. Inazu et al., Peptide Sci., 153-156 (1998) describe un método para la síntesis de glicopéptidos en el que el acoplamiento se lleva a cabo en solución y la unidad... [Seguir leyendo]
Reivindicaciones:
1. Proceso para la síntesis en fase sólida de un glicopéptido que tiene al menos un oligosacárido unido a una asparagina en una posición deseada de la cadena peptídica del mismo, el proceso comprende las 5 etapas de:
(1) esterificación de un grupo hidroxilo de una resina que tiene el grupo hidroxilo y un grupo carboxilo de un aminoácido que tiene un nitrógeno del grupo amino protegido por un grupo protector liposoluble,
(2) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(3) amidación del grupo amino libre y de un grupo carboxilo de un aminoácido que tiene un nitrógeno de grupo amino protegido por un grupo protector liposoluble,
(4) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(5) repetición de las etapas (3) y (4) al menos una vez,
(6) preparación de un disialooligosacárido unido a una asparagina o un
monosialooligosacárido unido a una asparagina que tiene los grupos hidroxilos no protegidos y que tiene un nitrógeno del grupo amino protegido por un grupo protector liposoluble y el grupo carboxilo del ácido siálico protegido por un grupo bencilo, alilo o difenilmetilo,
(7) amidación del grupo amino libre y de un grupo carboxilo de la porción asparagina del
disialooligosacárido unido a una asparagina o del monosialooligosacárido unido a una asparagina que tiene un nitrógeno del grupo amino protegido por un grupo protector liposoluble y el grupo carboxilo del ácido siálico protegido por un grupo bencilo, alilo o difenilmetilo,
(8) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(9) amidación del grupo amino libre y un grupo carboxilo de un aminoácido que tiene un nitrógeno del grupo amino protegido por un grupo protector liposoluble,
(10) repetición de las etapas (8) y (9) al menos una vez,
(11) eliminación del grupo protector liposoluble para formar un grupo amino libre,
(12) corte de la resina con un ácido.
2. Proceso según la reivindicación 1, en el que el disialooligosacárido unido a una asparagina o el monosialooligosacárido unido a una asparagina tienen el grupo carboxilo del ácido siálico protegido por un grupo bencilo, en el que el grupo bencilo se introduce en el grupo carboxilo del ácido siálico ajustando una solución de disialooligosacárido unido a una asparagina o de monosialooligosacárido unido a una asparagina a un pH de 5 a 6, liofilizando la solución, disolviendo el producto liofilizado en dimetilformamida seca y haciéndolo reaccionar con bromuro de bencilo.
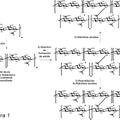
3. Proceso según la reivindicación 1, en el que el disialooligosacárido unido a una asparagina o el monosialooligosacárido unido a una asparagina está representado por la fórmula (7)
en la que uno de Rx y de Ry es un grupo representado por la fórmula (8) y el otro es un átomo de hidrógeno o un grupo representado por una de las fórmulas (3) a (5) y (8) :
4. Proceso según cualquiera de las reivindicaciones de la 1 a la 3, en el que el disialooligosacárido unido a una asparagina o el monosialooligosacárido unido a una asparagina de la etapa (6) tiene al menos 6 residuos de azúcar.
5. Proceso según la reivindicación 4, en el que el disialooligosacárido unido a una asparagina o el 10 monosialooligosacárido unido a una asparagina de la etapa (6) tiene de 9 a 11 residuos de azúcar.
6. Proceso según la reivindicación 4 o 5, en el que el disialooligosacárido unido a una asparagina o el monosialooligosacárido unido a una asparagina de la etapa (6) tiene un oligosacárido bifurcado unido al mismo.
7. Proceso según cualquiera de las reivindicaciones de la 1 a la 6, en el que el grupo protector liposoluble 15 es un grupo 9-fluorenil-metoxicarbonil (Fmoc) .
8. Proceso según cualquiera de las reivindicaciones de la 1 a la 7, en el que el grupo protector del grupo carboxilo del ácido siálico es un grupo bencilo.
9. Proceso según cualquiera de las reivindicaciones de la 1 a la 8, que además comprende (1) la
eliminación del grupo bencilo, alilo o difenilmetilo del grupo carboxilo del ácido siálico después de la 5 etapa (12) .
10. Glicopéptido que puede obtenerse mediante un proceso de acuerdo con cualquiera de las reivindicaciones de la 1 a la 8 y que tiene al menos un oligosacárido unido a una asparagina en una posición deseada de la cadena peptídica del mismo, el glicopéptido que tiene al menos un oligosacárido seleccionado entre un disialooligosacárido unido a una asparagina y un monosialooligosacárido unido a una asparagina unido como el oligosacárido unido a una asparagina y un grupo carboxílico del ácido siálico protegido por un grupo bencilo, alilo o difenilmetilo.
Patentes similares o relacionadas:
Separación de contaminantes de polisacárido de Streptococcus pneumoniae por manipulación del pH, del 17 de Junio de 2020, de WYETH LLC: Un procedimiento de reducción del contenido de proteínas y preservar el contenido de polisacárido capsular en un caldo de lisado celular complejo de Streptococcus pneumoniae, […]
Compuestos y sus efectos sobre el control del apetito y la sensibilidad a la insulina, del 10 de Junio de 2020, de IMPERIAL COLLEGE INNOVATIONS LIMITED: Un éster de propionato de inulina para su uso en la terapia para la reducción del apetito, ingesta de alimentos y/o ingesta de calorías y/o para mejorar […]
Evaluación de preparaciones de heparina, del 10 de Junio de 2020, de MOMENTA PHARMACEUTICALS, INC: Un procedimiento para identificar si se utilizó un procedimiento que incluye oxidación u oxidación seguido de tratamiento con un ácido para elaborar […]
Preparación de poli(ésteres de alfa-1,3-glucano) usando anhídridos orgánicos cíclicos, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un compuesto de poli(éster de alfa-1,3-glucano) representado por la estructura **(Ver fórmula)** en donde (i) n es al menos […]
Composiciones detergentes, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un derivado de polisacárido, en donde el derivado de polisacárido comprende un polisacárido sustituido con: a) uno o más grupos de poliamina; […]
 Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Reticulante de carbohidratos, del 6 de Mayo de 2020, de GALDERMA S.A.: Un producto de hidrogel que comprende moléculas de glucosaminoglucano como el polímero hinchable, en donde las moléculas de glucosaminoglucano se reticulan covalentemente […]
Hidrogeles polimerizables fluorados para vendajes de heridas y procedimientos para hacerlos, del 18 de Marzo de 2020, de THE UNIVERSITY OF AKRON: Un hidrogel que comprende: polímeros reticulados, los polímeros tienen cadenas principales de polisacáridos, donde las cadenas principales […]