Nuevo procedimiento.
Una bacteria capaz de producir timidina cuando se desarrolla en un medio de cultivo,
en el cual la cepahospedadora tiene un gen de TMPasa y un gen de timidilato-sintasa, caracterizada porque la bacteria comprendemodificaciones genéticas que dan como resultado que el camino biosintético de la timidina produzcapreferentemente TdR a expensas de UdR por aumento de la disponibilidad de una unidad de un solo carbono paradUMP con objeto de su conversión en dTMP, en donde las modificaciones genéticas comprenden la sobreexpresiónde un gen thyA de E. coli o un gen td del bacteriófago T4 e incluye una unidad de transcripción T4 frd capaz deexpresar una dihidrofolato-reductasa (EC 1.5.1.3), y en la que el gen que codifica una nucleósido-difosfato-quinasa(EC 2.7.4.6) ha sido silenciado o desactivado o escindido de algún otro modo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/051072.
Solicitante: GLAXO GROUP LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: 980 GREAT WEST ROAD BRENTFORD, MIDDLESEX TW8 9GS REINO UNIDO.
Inventor/es: ANDERSON, DAVID, MARTIN, LIU,LIN, PODKOVYROV,SERGEY, PRESTON,CHRISTOPHER, COLLIS,ANDREW JOHN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/52 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican enzimas o proenzimas.
- C12N9/06 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › actúan sobre compuestos que contienen nitrógeno como dadores (1.4, 1.5, 1.7).
- C12N9/12 C12N 9/00 […] › transfieren grupos que contienen fósforo, p. ej. Quinasas (2.7).
- C12P19/38 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Nucleósidos.
PDF original: ES-2410857_T3.pdf
Fragmento de la descripción:
Nuevo procedimiento Campo de la Invención La presente invención se refiere a la producción biológica de timidina. Más particularmente, la misma se refiere a un método que utiliza materiales biológicos manipulados genéticamente. Los materiales biológicos manipulados genéticamente pueden incluir un organismo productor de timidina, tal como una bacteria o uno o más constructos de DNA, por ejemplo plásmidos, que en combinación con una célula hospedadora adecuada conducirán, cuando se desarrollan en un medio de cultivo apropiado, a la producción biológica de timidina.
Antecedentes de la Invención El desoxirribonucleósido de pirimidina timidina es útil como compuesto farmacéutico intermedio. El mismo es particularmente importante para la síntesis química del AZT, conocido también como zidovudina o azidotimidina. Este es un fármaco antirretroviral de la clase de los inhibidores nucleosídicos de la transcriptasa inversa (NRTI) , que, bajo la marca comercial Retrovir, fue el primer fármaco autorizado para tratar la infección de HIV.
El HIV/SIDA se trata usualmente con combinaciones de tres o más fármacos antirretrovirales (De Clercq, Med.
Chem. Res. 13: 439-478, 2004) . AZT tiene un papel importante y expandido como componente principal de terapias de combinación y es vendido bajo una diversidad de marcas comerciales que incluyen Retrovir, Zidovir, Viro-Z, Aviro-Z y Zido-H.
AZT es particularmente valioso cuando se combina con el fármaco NRTI 3TC (lamivudina) . Estos dos fármacos están disponibles, formulados en una sola píldora, bajo las marcas comerciales Combivir y Duovir. Una combinación NRTI triple de AZT, 3TC y abacavir se vende bajo la marca comercial Trizivir. Otros fármacos NRTI utilizados en conjunción con AZT incluyen didanosina, emtricitabina y zalcitabina.
AZT es útil también en combinación con fármacos inhibidores de la proteasa de HIV que incluyen amprenavir, atazanavir, indinavir, ritonavir y saquinavir, y con inhibidores de la transcriptasa inversa no nucleosídicos (NNRTI) que incluyen delavirdina, efavirenz y nevirapina.
AZT es el único fármaco anti-HIV aprobado para uso durante el embarazo (Lyall, et al., HIV Med. 2: 314-334, 2001) . En 1997, aproximadamente 600.000 niños murieron de SIDA contraído por transmisión de la madre al bebé. AZT, tomado durante el último trimestre del embarazo, puede reducir el riesgo de transmisión viral en un 67% (Mitchla & Sharland, Expert Opin. Pharmacother. 1: 239-248, 2000) .
La tecnología de fermentación es una alternativa atractiva a la síntesis química para la preparación comercial de las grandes cantidades de timidina requeridas para la fabricación de AZT. Los procesos de fermentación están bien establecidos en la industria como medio para producir moléculas biológicas tales como antibióticos, aminoácidos y vitaminas en gran escala y con costes relativamente bajos (Atkinson, & Mavituna, Biochemical Engineering and Biotechnology Handbook, 2nd Edition, New York, Stockton Press, 1991) .
Sin embargo, la timidina no se encuentra usualmente en su forma "libre" en la naturaleza, sino que se produce como el ácido monofosfato-timidílico y se incorpora en el DNA como el trifosfato. Los sistemas biológicos no producen naturalmente cantidades significativas de timidina, por lo que se requiere un mutante u organismo modificado por ingeniería genética.
En EP 0.344.937 se dan a conocer cepas de Brevibacterium seleccionadas para producir timidina en cultivo aerobio. Se hace referencia también a una publicación de patente japonesa No. 39-16345, que expone el uso de una cepa mutante de Bacillus subtilis en la producción por fermentación de un polisacárido que contiene timidina.
En US 5.213.972 (McCandliss & Anderson) , se da a conocer un proceso para la producción de desoxirribonucleósidos de pirimidina (PdN) tales como timidina y 2'-desoxiuridina. Se propone un microorganismo replicable, que incorpora y expresa una secuencia de DNA que codifica una PdN-fosfohidrolasa que convierte un PdN-monofosfato en un PdN.
Más particularmente, McCandliss & Anderson, supra, describen un método de fermentación que puede utilizarse para producir timidina que implica la expresión de desoxitimidilato-fosfohidrolasa (dTMPasa) a partir del bacteriófago PBS1 de Bacillus subtilis. Este tipo de enzima se encuentra en la naturaleza expresada por bacteriófagos que incorporan PdNs tales como 2'-desoxiuridina o 5-hidroximetil-2'-desoxiuridina en su DNA en lugar de timidina.
En la fermentación de timidina descrita en US.5.213.972, las enzimas que degradan la timidina (timidina-fosforilasa y 50 uridina-fosforilasa) , se han eliminado por mutación, con lo que se acumula timidina. Así, el uso de la enzima dTMPasa contribuye a crear el camino que permite la síntesis de timidina. Una expresión de dTMPasa sola, sin embargo, no puede asegurar un nivel comercialmente viable de producción de timidina.
En WO 01/02580, se describen mejoras que dan como resultado la producción incrementada de timidina por células que expresan dTMPasa.
No obstante, un problema en la fabricación de timidina producida biológicamente reside en la producción concomitante de 2'-desoxiuridina (UdR) en el proceso de fermentación. Las dos moléculas tienen propiedades similares, difiriendo en estructura por un solo grupo metilo, y su separación durante el procesamiento aguas abajo es difícil y costosa. Para una aplicación farmacéutica, tal como la síntesis de AZT, puede requerirse timidina de alta pureza con niveles bajos de UdR.
Sería ventajoso que la timidina producida biológicamente por fermentación diera niveles significativamente reducidos de UdR comparada con los procesos corrientes, de tal modo que el requerimiento para la purificación agua abajo a fin de eliminar este material se minimizara o eliminara.
Por significativamente reducido se entiende que los niveles (contaminantes) de UdR constituyen menos de 25%, más preferiblemente menos de 10%, todavía más preferiblemente menos de 5%, pasando por 4%, 3%, y 2%, hasta niveles de 1% e inferiores en el producto timidina fermentado.
Idealmente, deberían alcanzarse niveles "altos" de timidina. Los niveles de timidina pueden expresarse como cifras de "productividad específica" en las que la medida se determina 4-6 horas después de la inducción. Se prefieren niveles mayores que 5 mg TdR/litro/hora/g de peso de células secas, más particularmente mayores que 10 mg TdR/litro/hora/g de peso de células secas y más preferiblemente cifras de productividad específica mayores que 15 a 20 y 25.
Estos niveles deberían obtenerse muy preferiblemente con los niveles reducidos de UdR arriba descritos y por consiguiente pueden combinarse de tal manera que, por ejemplo, pudiera obtenerse un título de TdR de 5 g/l que contenga menos de, por ejemplo, 5% de UdR.
De hecho, el proceso de la técnica anterior, que utiliza el plásmido pCG532 en la cepa hospedadora CMG2451,
como se da a conocer en WO 01/02580, produce un contenido medio de UdR en tests en matraces de sacudidas de 34, 5%. A tales niveles, el procesamiento aguas abajo para separar timidina de UdR es difícil y costoso.
Es una finalidad de la presente invención modificar organismos productores de timidina de tal manera que los mismos produzcan timidina sin producción concomitante significativa de UdR.
Como se utiliza en esta memoria, el término "organismo" incluye un organismo que pueda producir timidina por
expresión del DNA codificado en su cromosoma (como se expone, por ejemplo, en EP0344937) o DNA que hospeda la misma (como se expone, por ejemplo, en US 5.213.972 y WO 01/2580) . Este DNA hospedador puede estar presente como uno o más constructos de DNA, tales como, por ejemplo, uno o más plásmidos.
En particular, es una finalidad proporcionar una mejora en la calidad de la timidina producida en comparación con la combinación constructo/hospedador dada a conocer en WO 01/2580.
Es una finalidad adicional asegurar que cualquier modificación génica realizada en un constructo sea estable de tal manera que cuando el constructo se introduce en una célula hospedadora, y se deja crecer la combinación, el hospedador sea incapaz de propagarse por sí mismo sin que esté presente el constructo, es decir que, si el constructo se pierde, el organismo muere.
Sumario de la Invención Inesperadamente, se ha encontrado que existe un paso significativo limitante de la velocidad en la producción de timidina que ocurre alrededor de la conversión de dUMP en dTMP, de tal manera que puede dirigirse simultáneamente dUMP hacia la producción de UdR. Esta limitación no puede atenuarse por simple sobreexpresión... [Seguir leyendo]
Reivindicaciones:
1. Una bacteria capaz de producir timidina cuando se desarrolla en un medio de cultivo, en el cual la cepa hospedadora tiene un gen de TMPasa y un gen de timidilato-sintasa, caracterizada porque la bacteria comprende modificaciones genéticas que dan como resultado que el camino biosintético de la timidina produzca preferentemente TdR a expensas de UdR por aumento de la disponibilidad de una unidad de un solo carbono para dUMP con objeto de su conversión en dTMP, en donde las modificaciones genéticas comprenden la sobreexpresión de un gen thyA de E. coli o un gen td del bacteriófago T4 e incluye una unidad de transcripción T4 frd capaz de expresar una dihidrofolato-reductasa (EC 1.5.1.3) , y en la que el gen que codifica una nucleósido-difosfato-quinasa (EC 2.7.4.6) ha sido silenciado o desactivado o escindido de algún otro modo.
Figura 1: Biosíntesis de Timidina en Escherichia coli K12
Figura 2: Reacciones de la Timidilato-sintasa
Figura 3: Regeneración de CH2 a partir de Serina y Glicina Figura 4: Regeneración de CH2 a partir de Formiato Figura 5: Dianas Genéticas para Mejorar de Regeneración de CH2-THF
Figura 6: pCG532
Figura 7: pCG609
Figura 8: pCG376
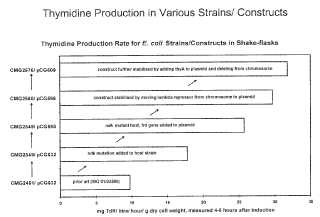
Figura 9: Producción de Timidina en Diversas Cepas/Constructos
Tasa de Producción de Timidina para Cepas/Constructos de E. coli en Matraces de Sacudidas mg TdR/litro/hora/g peso de células secas, medido 4-5 horas después de la inducción
Patentes similares o relacionadas:
PRODUCCION BIOTECNOLOGIA DE D-D!BOA Y SUS DERIVADOS CLORADOS A PARTIR DE SUS PRECURSORES NITROFENOXIDO-ACETATO, del 25 de Junio de 2020, de UNIVERSIDAD DE CADIZ: La invención tiene como propósito la producción biotecnológica de D-DIBQA, un compuesto análogo al herbicida natural DIBOA, a partir del precursor 2-(2'-nitrofenoxi)- […]
Producción de FDCA catalizada por deshidrogenasa, del 17 de Junio de 2020, de PURAC BIOCHEM B.V.: Proceso para oxidar ácido 5-hidroximetil-2-furancarboxílico (HMFCA) a ácido 5-formil-2-furoico (FFA), donde el proceso comprende la etapa de incubar una […]
Fábrica de células bacterianas modificadas genéticamente para la producción de tiamina, del 22 de Abril de 2020, de Biosyntia ApS: Bacteria modificada genéticamente para la producción de tiamina no fosforilada; en la que dicha bacteria se caracteriza por tener transgenes […]
Procedimiento para la producción de L-aminoácidos bajo empleo de una bacteria alcalífila, del 5 de Febrero de 2020, de Evonik Operations GmbH: Procedimiento para la sobreproducción de un L-aminoácido, caracterizado por que en este procedimiento se emplea Corynebacterium humireducens.
Producción microbiana de aminas grasas, del 20 de Noviembre de 2019, de Genomatica, Inc: Una célula bacteriana recombinante para la producción de una amina grasa, que comprende: (i) uno o más genes expresados que co 5 difican una […]
Composiciones y métodos para preparar (s)-norcoclaurina y (s)-norlaudanosolina e intermedios de síntesis de las mismas, del 23 de Octubre de 2019, de Willow Biosciences Inc: Un método de preparación de (S)-norcoclaurina o (S)-norlaudanosolina que comprende: (a) proporcionar al menos un precursor de la vía de la […]
Expresión modificada de prolil-4-hidroxilasa en physcoitrella patens, del 19 de Junio de 2019, de Albert-Ludwigs-Universität Freiburg: Un procedimiento de fabricación de una proteína recombinante que comprende los pasos de - proporcionar células de Physcomitrella patens que comprende […]
Procedimientos para la producción de líneas celulares de mamífero modificadas con transgenes amplificados, del 29 de Mayo de 2019, de Precision Biosciences, Inc: Un procedimiento para la inserción de una secuencia exógena en un locus que se pueda amplificar de una célula de mamífero que comprende: (a) proporcionar […]