Lisado plaquetario inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF y su procedimiento de preparación.
Un lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10163843.
Solicitante: GwoWei Technology Co., Ltd.
Nacionalidad solicitante: Taiwan, Provincia de China.
Dirección: 1F, N 86, Sec. 1, Zhongcheng Road, Shilin District Taipei City 111 TAIWAN.
Inventor/es: BURNOUF, THIERRY, SU,CHENG-YAO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61K38/36 A61K 38/00 […] › Factores de coagulación sanguínea o de fibrinolisis.
- C12N5/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00).
PDF original: ES-2402144_T3.pdf
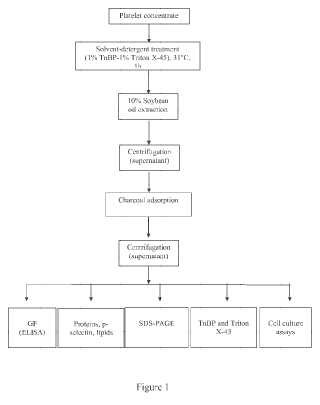
Fragmento de la descripción:
Lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF y su procedimiento de preparación Campo de la invención La presente invención se refiere al campo de derivados plaquetarios y más específicamente al campo de concentrados con factores de crecimiento que se obtienen de plaquetas de origen humano y animal. La presente invención también se refiere a procedimientos para preparar dichos lisados plaquetarios que contienen factores de crecimiento, así como al uso de los mismos para cultivos celulares in vitro y ex vivo (tal como para el desarrollo y diferenciación de células madre) , aplicaciones cosméticas o aplicaciones clínicas, por ejemplo, en combinación con injertos de hueso.
Antecedentes Como se pone de manifiesto mediante análisis proteómico, las plaquetas humanas contienen una gran cantidad de moléculas que presentan importantes funciones fisiológicas, entre las que destacan los factores de crecimiento (GF, Growth Factors) . Estos factores de crecimiento, que se acumulan en el interior de los gránulos α plaquetarios, incluyen principalmente tres isoformas de Factores de Crecimiento Derivados de Plaquetas (PDGF-AA, -AB y -BB) , el Factor de Crecimiento Endotelial Vascular (VEGF) , el Factor de Crecimiento Transformante º (TGF-β1 y TGF-β2) , el Factor de Crecimiento Epidérmico (EGF) , el Factor de Crecimiento de Fibroblastos (FGF) y algún Factor de Crecimiento similar a Insulina (IGF) . De acuerdo con el interés terapéutico de dichos factores de crecimiento, las mezclas complejas de factores de crecimiento con plaquetas humanas ya se están usando en aplicaciones terapéuticas en forma de biomateriales en gel con plaquetas de un solo donante resultantes de la activación por trombina de plasma que contiene plaquetas.
La activación plaquetaria generalmente conduce a la liberación de los factores de crecimiento contenidos en su interior y a su atrapamiento en una matriz de gel obtenida por conversión simultánea, inducida por trombina, de fibrinógeno en fibrina. Generalmente, este biomaterial se aplica en tejidos, en solitario o en combinación con materiales de injerto. Los geles plaquetarios que contienen factores de crecimiento se usan por tanto en medicina regenerativa para promover la curación y la regeneración de tejidos blandos y duros. Los concentrados con factores de crecimiento obtenidos de plaquetas también se usan para complementar los medios de crecimiento para cultivos celulares in vitro o ex vivo. Recientemente se ha demostrado, la posibilidad de usar secretomas plaquetarios ricos en factores de crecimiento como sustitutos de suero bovino fetal (SBF) para el desarrollo ex vivo de células madre mesenquimales o hematopoyéticas.
El uso de secretomas plaquetarios ricos en factores de crecimiento es de particular interés para el desarrollo de células madre, y más específicamente, Células Madre Mesenquimales (CMM) (o células madre hematopoyéticas) que se consideran como células “universales” emergentes, como un sustituto del Suero Bovino Fetal (SBF) o del Suero de Ternero Fetal (STF) que se consideran como posibles fuentes de transmisión de priones y virus, así como una causa de problemas inmunológicos en pacientes debido a proteínas bovinas residuales y antígenos dentro del suero Bovino o de Ternero.
Recientemente se han desarrollado nuevas estrategias consistentes en la producción de factores de crecimiento derivados de plaquetas recombinantes en sistemas de expresión convencionales. Por ejemplo, algunos factores de crecimiento humano recombinantes (Rh) individuales se usan en aplicaciones terapéuticas. En algunos países el Rh-PDGF-BB, expresado por levaduras modificadas por ingeniería genética, está autorizado en particular para el tratamiento de úlceras diabéticas neuropáticas crónicas en extremidades inferiores aunque para conseguir eficacia clínica al parecer se requieren grandes dosis y diversas aplicaciones semanales de este factor de crecimiento sencillo. De manera similar, las proteínas morfogénicas óseas (BMP) - 2 y -7 de tipo (Rh) , que pertenecen a la superfamilia del TGF-β, pueden producirse a partir de células de Ovario de Hámster Chino y están autorizadas para curar determinadas fracturas quirúrgicas. Sin embargo, la cantidad de factores de crecimiento recombinantes disponibles permanece extremadamente limitada, en parte debido a la dificultad para aislar, identificar, clonar y expresar estos factores de crecimiento. Adicionalmente, las preparaciones derivadas de plaquetas aún proporcionan un beneficio complementario sobre el uso de factores recombinantes sencillos, ya que en algunas aplicaciones puede conseguirse un efecto sinérgico beneficioso de la combinación de factores de crecimiento.
No obstante parece que los factores de crecimiento PDGF y VEGF han demostrado estar directamente relacionadas con la propagación y/o diferenciación anómala de células (véase por ejemplo Ferrara y col., Nature Medicine, vol. 9, no. 6, 2003, págs. 669-676; así como en la publicación EMA/ 92326/2010 de la European Medical Agency con fecha 18 de febrero del 2010 y en la comunicación de la FDA con fecha 27 de marzo de 2008 sobre “una revisión continua de seguridad de regranex (becaplermin) . Por tanto, en vista del aumento de susceptibilidad del desarrollo de cánceres después del tratamiento con cada uno de estos dos factores de crecimiento, el PDGF y el VEGF deben evitarse para el cultivo de células madre o para la curación de pacientes, en particular cuando se sabe que dichos pacientes están en riesgo de padecer cáncer.
Existe por lo tanto una necesidad de desarrollar procedimientos de procesamiento de materiales plaquetarios humanos que permitan la preparación de preparaciones de factores de crecimiento a nivel industrial que sean viralmente inocuas y estén bien caracterizadas y más particularmente de preparaciones con empobrecimiento en PDGF y VEGF.
La Solicitud de Patente WO 2009/087560 desvela que los concentrados plaquetarios humanos pueden someterse a un tratamiento mediante una combinación de disolvente y detergente (S/D) que consigue dos propósitos: (a) la inactivación de virus con envoltura lipídica y (b) la liberación masiva de los factores de crecimiento de los gránulos α plaquetarios. Después, podría obtenerse una mezcla compleja de factores de crecimiento derivados de plaquetas que comprendiese PDGF-AB, -BB, y -AA, TGF-β, EGF, VEGF y factores de crecimiento similares a insulina β1 (IGFβ1) por tratamiento con la combinación de S/D, extracción con aceite y cromatografía de interacción hidrófoba (CIH) , en la que la extracción con aceite y la CHI se usaron para eliminar los agentes S/D sin influir significativamente en el contenido de PGF y de proteína. Se demostró que la preparación resultante de factores de crecimiento plaquetarios estimulaba in vitro diversas líneas celulares y potenciaba el desarrollo de células madre procedentes de liposucción de tejido adiposo. Adicionalmente, el documento WO 2009/087560 desvela que la sustitución de la CIH por una columna de intercambio catiónico de SP-sefarose permite la preparación de una fracción de PDGF-VEGF purificada. De hecho, en esta estrategia, el PDGF y el VEGF se adsorben sobre la columna pero el TGF-β, el EGF y el IGF se encuentran en límite, junto con los agentes S/D usados para la etapa de inactivación de virus. Por el contrario, el documento WO 2009/087560 desvela que el TGF-β y el EGF pueden purificarse hasta un determinado nivel sustituyendo la CIH por un intercambiador aniónico de DEAE-sefarose.
En la publicación de El-Ekiaby y col. (El-Ekiaby y col;, “Solvent-detergent filtered (S/D-F) fresh frozen plasma and cr y oprecipitate minipools prepared in a newly designed integral disposable processing bag system”, Transfusion medicine, 2010, 20, 48-61) , los autores desvelan un proceso aplicado para el tratamiento de inactivación viral de singletes o miniconjuntos de plasma y crioprecipitado para transfusión y comprende, como etapas principales, el tratamiento con S/D de Plasma Fresco Congelado (FFP) o de CrioPlasma Pobre (CPP) , o de crioprecipitado con una mezcla de TnBP y Triton X-45, la extracción con aceite del material plasmático tratado con S/D y el filtrado del material plasmático extraído con aceite a través de un filtro de adsorción con S/D que contiene carbón vegetal activado. Como se describe en esta publicación, el procedimiento desvelado conserva en particular la actividad funcional de las proteínas plasmáticas (tales como factores de coagulación) , no modifica la composición multimérica del VWF, reduce el TnBP y el Tritón X-45 por debajo de los niveles aceptables y permite la filtración estéril por gravedad... [Seguir leyendo]
Reivindicaciones:
1. Un lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF.
2. El lisado plaquetario viralmente inactivado que contiene factores de crecimiento de acuerdo con la reivindicación 1, que comprende los factores de crecimiento TGF-β, IGF y EGF.
3. El lisado plaquetario viralmente inactivado que contiene factores de crecimiento de la reivindicación 1 o 2, en el que:
-el nivel de PDGF-AB es menor que 3 ng/ml de dicho lisado; y/o
-el nivel de VEGF es menor que 0, 01 ng/ml de dicho lisado; y/o
-el nivel de TGF-β es mayor que 50, más preferentemente mayor que 100, más preferentemente mayor que 10 150, más preferentemente mayor que 200, más preferentemente mayor que 250 ng/ml de dicho lisado; y/o
-el nivel de EGF es mayor que 0, 5, más preferentemente mayor que 1, más preferentemente mayor que 1, 5, más preferentemente mayor que 2, más preferentemente mayor que 2, 5 ng/ml de dicho lisado; y/o
-el nivel de IGF es mayor que 20, más preferentemente mayor que 50, más preferentemente mayor que 100 ng/ml de dicho lisado.
4. Un procedimiento para preparar un lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF que comprende las siguientes etapas:
a) poner en contacto un concentrado plaquetario de partida con un disolvente y/o un detergente, b) incubar dicho concentrado plaquetario de partida con el disolvente y/o detergente
- durante un periodo de al menos 5 minutos a 6 horas.
20. a un pH mantenido en un intervalo de aproximadamente 6, 0 a aproximadamente 9, 0, y
- a una temperatura dentro del intervalo de 2 ºC a 50 ºC,
c) retirar opcionalmente el disolvente y/o el detergente mediante extracción con aceite y obtener una fase de proteína acuosa; e d) incubar con carbón vegetal el concentrado plaquetario tratado con el disolvente y/o el detergente de la etapa b) o la fase de proteína acuosa de la etapa c) .
5. El procedimiento de la reivindicación 4, en el que dicho disolvente está seleccionado en el grupo que consiste en di- o trialquilfosfatos, di o trialquilfosfatos con diferentes cadenas alquilo y es preferentemente el tri-n-butilfosfato (TnBP) .
6. El procedimiento de una cualquiera de las reivindicaciones 4 a 5, en el que dicho detergente está seleccionado del
grupo que consiste en derivados de polioxietileno de ácidos grasos, ésteres parciales de anhídridos de sorbitol, detergente no iónicos, desoxicolato sódico y sulfobetaínas y es preferentemente Triton X-45®, Triton X-100® o Tween 80®.
7. El procedimiento de una cualquiera de las reivindicaciones 4 a 6, en el que la concentración de cada uno de dicho disolvente y/o dicho detergente en la etapa b) varía del 0, 2 al 5% en volumen con respecto al volumen del 35 concentrado plaquetario de partida.
8. El procedimiento de una cualquiera de las reivindicaciones 4 a 7, en el que la extracción con aceite se realiza con un aceite de calidad farmacéutica, usándose el aceite en una cantidad del 2 al 20% en peso o del 5 al 15% en peso o del 5 al 10% en peso, en base al peso de la mezcla del concentrado plaquetario con el disolvente y/o el detergente.
9. El procedimiento de una cualquiera de las reivindicaciones 4 a 8, en el que
- cuando la extracción con aceite de la etapa c) se realiza, la extracción con carbón vegetal se realiza sobre la fase de proteína acuosa de la etapa c) , con carbón vegetal en una cantidad que varía de 50 a 250 g/l, preferentemente de 55 a 200 g/l, o de 60 a 150 g/l, o de 65 a 100 g/l de dicha fase proteína acuosa; y
- cuando no se realiza la extracción con aceite, la extracción con carbón vegetal se realiza sobre el concentrado
plaquetario tratado con el disolvente y/o el detergente de la etapa b) , con carbón vegetal en una cantidad que varia de 250 a 1250 g/l, preferentemente de 275 a 1000 g/l, o de 300 a 750g/l, o de 325 a 500 g/l de dicha fase de proteína acuosa.
10. El procedimiento de una cualquiera de las reivindicaciones 4 a 9, en el que el carbón vegetal activado adsorbe el
azul de metileno en el intervalo de 100 a 550, y preferentemente de 300 a 500 g/m2 o de 100 a 300 g/m2 de carbón 50 vegetal activado.
11. El procedimiento de una cualquiera de las reivindicaciones 4 a 10, que adicionalmente comprende al menos una etapa de centrifugación después de la etapa de extracción con aceite c) y/o después de la incubación con carbón vegetal de la etapa d) .
12. El procedimiento de una cualquiera de las reivindicaciones 4 a 11, que adicionalmente comprende una etapa (e) de purificación cromatográfica y/o de ultrafiltración y/o de nanofiltración.
13. El procedimiento de una cualquiera de las reivindicaciones 4 a 12, que adicionalmente comprende una etapa
preliminar de preparación de un concentrado plaquetario de partida antes de dicha etapa a) , preferentemente por 5 aféresis o por aislamiento de la capa leucocitoplaquetaria de sangre completa.
14. El procedimiento de una cualquiera de las reivindicaciones 4 a 13, en el que el concentrado plaquetario de partida de la etapa a) se obtiene a partir de un conjunto de concentrados plaquetarios.
15. Un lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF que puede obtenerse mediante el procedimiento de acuerdo con una cualquiera de las reivindicaciones 4 a 14.
16. El lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF obtenido mediante el procedimiento de una cualquiera de las 4 a 15 o el lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecidos en PDGF y VEGF de acuerdo con una cualquiera de las reivindicaciones 1 a 3 para su uso en cosmética, para su uso para promover la regeneración o la reconstitución ósea, o para su uso en el tratamiento de un hueso fracturado.
17. El lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecido en PDGF y VEGF que puede obtenerse mediante el procedimiento de una cualquiera de las reivindicaciones 4 a 14 o el lisado plaquetario viralmente inactivado que contiene factores de crecimiento empobrecidos en PDGF y VEGF de acuerdo con una cualquiera de las reivindicaciones 1 a 3 para el cultivo celular in vitro o ex vivo y preferentemente para promover la diferenciación de células madre hacia un linaje osteoblástico y/o condrocítico.
Patentes similares o relacionadas:
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones que comprenden cócteles de fagos antibacterianos y usos de las mismas para el tratamiento de infecciones bacterianas, del 24 de Junio de 2020, de Tecnifar-Indústria Técnica Farmacêutica, S.A: Una composicion que comprende: una primera y una segunda cepa purificada de bacteriofago, cada una de dichas cepas que tiene un genoma que comprende […]
Formulaciones con oxidación reducida, del 3 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Una formulación líquida que comprende un anticuerpo y un compuesto que previene la oxidación del anticuerpo en la formulación líquida, en la que el compuesto es […]
Trampas de GDF, del 3 de Junio de 2020, de ACCELERON PHARMA, INC: Un polipéptido aislado que comprende la secuencia de aminoácidos de SEQ ID NO: 28.
Combinacion de peptidos tolerogenos con TFG-â para inducir y mantener la tolerancia oral en mamiferos jovenes, del 3 de Junio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Una composición nutricional - que contiene al menos un péptido de cinco hasta doce aminoácidos de longitud e incluye una secuencia elegida entre […]
Modulación de la actividad del factor de crecimiento epidérmico de unión a heparina para la curación de la membrana timpánica, del 6 de Mayo de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un agente que proporciona actividad de factor de crecimiento epidérmico de unión a heparina (HB-EGF) para su uso en el tratamiento de una perforación crónica de la membrana […]
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial, del 6 de Mayo de 2020, de ACORDA THERAPEUTICS, INC: Factor de crecimiento glial 2 (GGF2) para su uso en la promocion de la remielinizacion celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de […]