Procedimiento para la fabricación de un blíster que contiene comprimidos de topiramato.
Un procedimiento para la producción de un envase en blister (burbuja) para contener tabletas de topiramato que comprende las etapas de:
(a) secado de una pluralidad de tabletas de topiramato hasta un contenido de agua libre de entre aproximadamente 0, 4% a aproximadamente 1, 4%; (b) colocación de las tabletas de topiramato secadas de la etapa (a) en una lámina recipiente que tiene una pluralidad de cavidades; y (c) sellado de una lámina de cubierta a la lámina recipiente (b) para formar el envase en blister, siempre que las tabletas de topiramato secadas tengan un contenido en agua libre de menos de aproximadamente 1, 4% en el momento en que la lámina de cubierta se sella a la lámina recipiente y donde el envase en blister no contiene desecante.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2001/005878.
Solicitante: CILAG AG.
Nacionalidad solicitante: Suiza.
Dirección: HOCHSTRASSE 201 8205 SCHAFFHAUSEN SUIZA.
Inventor/es: DOBLER, MONIKA, MERKLE, STEFAN, LORCA, PEDRO, BACHMANN, DIETER.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61J1/03 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61J RECIPIENTES ESPECIALMENTE ADAPTADOS PARA USOS MEDICOS O FARMACEUTICOS; DISPOSITIVOS O METODOS ESPECIALMENTE CONCEBIDOS PARA CONFERIR A LOS PRODUCTOS FARMACEUTICOS UNA FORMA FISICA O DE ADMINISTRACION PARTICULAR; DISPOSITIVOS PARA ADMINISTRAR ALIMENTOS O MEDICINAS VIA ORAL; CHUPETES PARA BEBES; ESCUPIDERAS. › A61J 1/00 Recipientes especialmente adaptados a fines médicos o farmacéuticos (cápsulas o similares para administración vía oral A61J 3/07; adaptados especialmente para instrumentos o aparatos quirúrgicos o de diagnóstico A61B 50/30; recipientes para sustancias radioactivas G21F 5/00). › para píldoras o comprimidos (recipientes con para píldoras o comprimidos especiales para su distribución B65D 83/04).
- A61K31/7024 A61 […] › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Esteres de sacáridos.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61P25/08 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Antiepilépticos; Anticonvulsivos.
- B65D65/40 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B65 TRANSPORTE; EMBALAJE; ALMACENADO; MANIPULACION DE MATERIALES DELGADOS O FILIFORMES. › B65D RECIPIENTES PARA EL ALMACENAMIENTO O EL TRANSPORTE DE OBJETOS O MATERIALES, p. ej. SACOS, BARRILES, BOTELLAS, CAJAS, LATAS, CARTONES, ARCAS, BOTES, BIDONES, TARROS, TANQUES; ACCESORIOS O CIERRES PARA RECIPIENTES; ELEMENTOS DE EMBALAJE; PAQUETES. › B65D 65/00 Envolturas o embalajes flexibles; Material de embalaje de tipo o forma particular (envoltorios o sobres con medios para absorber los golpes B65D 81/03). › Empleo de estratificados para fines especiales de embalaje.
- B65D75/32 B65D […] › B65D 75/00 Paquetes que tienen objetos o materiales parcial o totalmente encerrados en cintas, hojas, bandas, tubos o bandas de material flexible fino, p. ej. en envolturas plegables (B65D 71/00 tiene prioridad). › estando una o las dos hojas o tiras ahuecadas para adoptar la forma del contenido.
- B65D75/34 B65D 75/00 […] › y teniendo varios huecos para adaptarse a una serie de objetos o de cantidades de materiales.
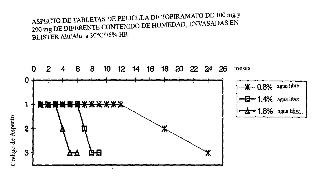
Fragmento de la descripción:
Procedimiento para la fabricación de un blister que contiene comprimidos de topiramato.
Referencias cruzadas a solicitudes relacionadas
Esta solicitud reivindica la prioridad de solicitud de Patente europea No. 00111 229.1, registrada el 25 de mayo, 2000.
Campo industrial
La presente invención se refiere a un procedimiento de manufactura de un envase en blister
(burbujas) que contiene tabletas de topiramato. Más en particular, el envase en blister contiene tabletas de topiramato secadas y comprende una lámina de cubierta sellada a una lámina recipiente.
Antecedentes de la invención
La industria farmacéutica emplea una diversidad de formulaciones de dosificación para administración oral de agentes medicinales a pacientes. Las formulaciones típicas para administración oral incluyen soluciones, emulsiones o suspensiones, líquidas, así como formas sólidas tales como cápsulas o tabletas (tal como aquí se usa, el término tableta
significa cualquier forma de dosificación sólida conformada y comprimida, incluyendo píldoras). Los métodos de preparación de tabletas son muy conocidos en la técnica, como aquellos en que el agente fármaco allí contenido se mantiene estable y activo. Según esto, la cualidad de la tableta se mide frente a especificaciones tales como aspecto, dureza y disponibilidad del agente fármaco como se demuestra por la velocidad de disolución y la uniformidad de contenido.
En la Patente estadounidense No. 4.513.006 se describe una variedad de ésteres clorosulfato y sulfamato de 2,3:4,5-bis-O-(1-metiletiliden)-β-D-fructopiranosa, su actividad anticonvulsivante en mamíferos y, por tanto, su utilidad en el tratamiento de la epilepsia. Más específicamente, el compuesto sulfamato de 2,3:4,5-bis-O-(1-metiletilideno)-β-D-fructopiranosa, en adelante citado como topiramato
, está actualmente disponible comercialmente como producto en tabletas en concentraciones de 25, 50, 100 y 200 mg, como terapia complementaria para tratamiento de adultos con ataques epilépticos parciales (Tabletas de TOPAMAX® (topiramato)). El topiramato se puede preparar siguiendo los procedimientos descritos en la Patente estadounidense Nos. 4.513.006 y 5.387.700 y, preferiblemente, por el procedimiento descrito en los Ejemplos 1 a 3 de la Patente estadounidense No. 5.387.700. Se cree que la exposición a la humedad y al calor hace que se degrade el agente activo de topiramato en la forma de dosificación sólida. La degradación de tabletas de topiramato se detecta fácilmente por los cambios en el aspecto físico (decoloración del color de la tableta volviéndose parda o negra) y por la formación de iones sulfato que se pueden detectar fácilmente por técnicas convencionales conocidas por cualquier especialista en el área (por ejemplo, por cromatografía de líquidos de alta presión).
Para mantener la calidad de la tableta, las tabletas de topiramato se han envasado en frascos de polietileno de alta densidad (HDPE) que contienen un desecante y envases en blister que llevan un desecante. El ensayo de estabilidad en función del tiempo ha demostrado que las tabletas en tales envases se han conservado a diversas temperaturas, humedad y condiciones de iluminación. Los envases en blister, sin embargo, ofrecen las ventajas sobre los frascos de HDPE utilizados como envase comercial actual y son, por tanto, un formato de envase preferido para tabletas de topiramato. Los envases en blister compaginan la estabilidad y características comerciales de frascos de HDPE con un menor coste de empaquetado, mayor ligereza de peso y un almacenado más convenientemente; además, ofrecen un acceso rápido, una más fácil respuesta a dosis unidad y mejor protección física para el producto. Los envases en blister son especialmente ventajosos para envasar tabletas sensibles a la humedad tales como las de topiramato debido a que cada cavidad de tableta queda como un recipiente primario en contacto directo con la tableta, encerrando inherentemente un mínimo de aire y humedad asociada.
La estabilidad de la tableta en un envase en blister, por lo tanto, resulta entonces función de las características físicas de los materiales utilizados en el envase en blister que afectan a la permeabilidad al vapor de humedad y a la capacidad de proteger al producto encerrado frente a luz y humedad. Aunque hay otros factores que afectan la estabilidad de la tableta, tales como contenido de humedad de la tableta y el propio entorno del envase, los fabricantes y empaquetadores han puesto el punto de mira sobre el potenciamiento del comportamiento en la estabilidad de los envases en blister proporcionando cavidades para materiales adicionales tales como desecantes además de cavidades de las tabletas. Por ejemplo, la patente EP 0466068 A describe un envase en blister donde cada cavidad de tableta está conectada con una cavidad de desecante. De manera similar, la Patente FR 2593152 A describe un envase en blister donde hay varias cavidades de tabletas conectadas con una cavidad de desecante. Dado que se puede acceder a la cavidad de desecante con igual facilidad que a la de tableta en los envases en blister descritos en estas referencias, estos envases presentan un riesgo potencial de seguridad. Reconociendo esto, la Patente FR 2660634 A describe un envase en blister donde el acceso a la cavidad de desecante queda reducido por proporcionar una lámina adicional que debe retirarse para abrir la cavidad de desecante. Las Patentes estadounidenses números 3.780.856 y 3.835.995 describen, cada una de ellas, envases en blister con secciones desprendibles que permiten el acceso únicamente a las cavidades de formas de dosificación oral. Además, la Patente EP 0779872 B1 describe una cavidad de forma de dosificación oral para tabletas de topiramato conectadas con una cavidad de desecante donde la cavidad de desecante está reforzada y no se puede abrir fácilmente. En resumen, las siguientes referencias describen envases en blister que contienen un desecante y los intentos de preservar la seguridad del consumidor por prevenir el acceso a la cavidad de desecante.
Descripción de la invención
Un objeto de la presente invención es proporcionar un procedimiento para envasado en blister de tabletas de topiramato desecadas.
La presente invención se refiere a un procedimiento para fabricación de un envase en blister que contiene tabletas de topiramato que comprende las etapas de:
En un modo de realización de la presente invención, las tabletas de topiramato se secan por un método seleccionado del grupo que consiste en secado con microondas, secado al vacío, secado por aire caliente, secado por rayos infra-rojos, secado empleando aire muy seco ya sea estática o dinámicamente y secado por colocación de un desecante en un tambor de almacenamiento de producto a granel durante un período de tiempo.
En un modo de realización de la invención, la lámina recipiente es una lámina seleccionada del grupo que consiste en una capa de metal simple, capas de metal múltiples, capa de plástico simple, capas de plástico múltiples, y un combinado de capa de metal y capa de plástico, y la lámina de cubierta es una lámina seleccionada del grupo que consiste en una capa de metal simple, capas de metal múltiples, capa combinada de metal y plástico, capa combinada de metal y papel y un combinado de capa de metal, de plástico y de papel.
La capa de lámina de metal es, preferiblemente, hoja de aluminio. La capa de lámina de plástico se selecciona preferiblemente del grupo que consiste en poli cloruro de vinilo (PVC), polidicloruro de vinilo (PVDC), poli cloruro de vinilideno, polietileno de elevada densidad (HDPE), polietileno de baja densidad (LDPE), polipropileno (PP), copolímero...
Reivindicaciones:
1. Un procedimiento para la producción de un envase en blister (burbuja) para contener tabletas de topiramato que comprende las etapas de:
(a) secado de una pluralidad de tabletas de topiramato hasta un contenido de agua libre de entre aproximadamente 0,4% a aproximadamente 1,4%;
(b) colocación de las tabletas de topiramato secadas de la etapa (a) en una lámina recipiente que tiene una pluralidad de cavidades; y
(c) sellado de una lámina de cubierta a la lámina recipiente (b) para formar el envase en blister, siempre que las tabletas de topiramato secadas tengan un contenido en agua libre de menos de aproximadamente 1,4% en el momento en que la lámina de cubierta se sella a la lámina recipiente y donde el envase en blister no contiene desecante.
2. El procedimiento según la reivindicación 1 donde la lámina recipiente es una lámina seleccionada del grupo que consiste en una capa de metal simple, capas de metal múltiples, una capa de plástico simple, capas de plástico múltiples y una capa combinada de metal y plástico.
3. El procedimiento según la reivindicación 2, donde la lámina de cubierta es una lámina seleccionada del grupo que consiste en una capa de metal simple, capas de metal múltiples, capa combinada de metal y capa de papel, y una capa combinada de metal, plástico y papel.
4. El procedimiento según la reivindicación 3, donde la lámina recipiente es una capa combinada de metal y plástico y la lámina de cubierta es una capa de metal.
5. El procedimiento según la reivindicación 4 donde la lámina recipiente es una capa combinada de metal y plástico de orto-poliamida/hoja de aluminio/policloruro de aluminio y la lámina de cubierta es una capa sencilla de hoja de aluminio.
6. El procedimiento según la reivindicación 5 donde la lámina recipiente es una lámina de 25 μm de orto-poliamida/ 45 μm de hoja de aluminio/60 μm de policloruro de vinilo y la lámina de cubierta es una lámina de hoja de aluminio de 20 μm.
7. El procedimiento según la reivindicación 1 donde las tabletas de topiramato se secan hasta un contenido de agua libre de entre aproximadamente 0,7% a aproximadamente 1,2%.
8. El procedimiento según la reivindicación 7 donde las tabletas de topiramato se secan hasta un contenido de agua libre entre aproximadamente 0,8% y aproximadamente 1,0%.
9. El procedimiento según la reivindicación 1 donde las tabletas de topiramato se secan por un método seleccionado del grupo que consiste en secado con micro-ondas, secado al vacío, secado con aire caliente, secado con rayos infra-rojos, secado utilizando aire muy seco ya estática o dinámicamente, y secado por colocación de un desecante en un tambor de almacenado de producto a granel durante un período de tiempo.
10. El procedimiento según la reivindicación 9 donde las tabletas de topiramato se secan utilizando aire caliente en un recubridor a una temperatura de aproximadamente 60ºC a aproximadamente 70ºC.
11. Un envase en blister fabricado por el procedimiento de la reivindicación 10.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Formulación de vitamina D de liberación modificada estabilizada y método de administración de la misma, del 22 de Julio de 2020, de EirGen Pharma Ltd: Una formulacion oral de liberacion controlada de un compuesto de vitamina D que comprende uno o ambos de 25- hidroxivitamina D2 y 25-hidroxivitamina D3, la formulacion […]
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composiciones y métodos para tratar el virus de la hepatitis C, del 15 de Julio de 2020, de Gilead Pharmasset LLC: Una composición farmacéutica que comprende: a) de aproximadamente el 25% a aproximadamente el 35% p/p de GS-7977 cristalino que tiene la estructura **(Ver […]
Preparación para el control del peso corporal a base de quitosano y celulosa, del 1 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Una composición oral sólida que contiene una combinación de quitosano de hongos o levaduras, celulosa amorfa en polvo y opcionalmente excipientes.
Granulados secos de polvos de sílice mesoporosa, del 1 de Julio de 2020, de FORMAC PHARMACEUTICALS N.V: Un granulado seco que comprende desde el 50% al 100% p/p de sílice mesoporosa ordenada que tiene una organización bidimensional hexagonalmente […]