Composición y métodos para determinar la resistencia a inhibidores de la entrada de virus usando ensayos de virus recombinantes.
Un método para determinar si una población de VIH es resistente a un inhibidor de entrada de VIH,
quecomprende:
(a) generar una curva log-sigmoidea de inhibición que comprende puntos de datos que miden la entradade la población de VIH en una célula en presencia de concentraciones variables del inhibidor de entrada de VIHque muestra un porcentaje de inhibición máxima para la población de VIH; y
(b) comparar la curva de inhibición de la etapa (a) con una curva log-sigmoidea de inhibicióncorrespondiente a una población de VIH de referencia,
en donde un descenso en el porcentaje de inhibición máxima observado para la población de VIH respecto alobservado para la población de VIH de referencia indica que el inhibidor de entrada de VIH es un inhibidor deentrada no competitivo y que el VIH es resistente al inhibidor de entrada de VIH no competitivo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/020240.
Solicitante: MONOGRAM BIOSCIENCES, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 345 OYSTER POINT BOULEVARD SOUTH SAN FRANCISCO, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: PETROPOULOS,Christos.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/16 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › VIH-1.
- C12N7/04 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › Inactivación o atenuación; Producción de partes elementales de virus.
- C12Q1/66 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una luciferasa.
- C12Q1/70 C12Q 1/00 […] › en los que intervienen virus o bacteriófagos.
PDF original: ES-2385960_T3.pdf
Fragmento de la descripción:
Composición y métodos para determinar la resistencia a inhibidores de la entrada de virus usando ensayos de virus recombinantes
2. Antecedentes
Los virus encapsulados animales se unen a la célula hospedante y entran en ella a través de la interacción de proteínas víricas de la membrana del virión (proteínas de cápsula) y proteínas de la superficie celular (receptores de virus) . El reconocimiento y la unión al receptor están mediados por la proteína de cápsula superficial. La entrada del virus es una diana atractiva para un tratamiento antiviral; se han evaluado o se están evaluando actualmente numerosos fármacos diseñados para bloquear la unión del virus o la fusión de la membrana en estudios preclínicos o clínicos (Richman, 1998; PhRMA, 1999; Stephenson, 1999) . Por ejemplo, el inhibidor de unión SCH-D, que bloquea la interacción entre proteínas de membrana víricas y CCR5 está siendo evaluado actualmente en estudios clínicos para determinar su eficacia como tratamiento antiviral (Shurman, 2004) . Otros inhibidores de entrada que están en investigación actualmente incluyen UK-427857 (Pfizer) , TNX-355 (Tanox Inc.) , AMD-070 (AnorMED) , Pro 140 (Progenics) , FP-21399 (EMD Lexigen) , BMS-488043 (Bristol-Myers Squibb) y GSK-873.140 (GlaxoSmithKline) . Un inhibidor de entrada, el T-20 (Roche/Trimeris) , ha sido aprobado para tratar la infección de VIH.
Según se vayan desarrollando estos fármacos y entren en las clínicas, serán necesarios ensayos que detecten rápida y fácilmente la emergencia de virus con una susceptibilidad reducida frente a inhibidores de entrada. En particular, se necesitan métodos para determinar si un VIH es resistente a un inhibidor de entrada, por ejemplo, SCH-C, SCH-D, UK-427857 y/o TNX-355. La presente invención cubre éstas y otras necesidades no satisfechas.
El documento WO03070985 describe un ensayo fenotípico para determinar la resistencia de virus de VIH frente a inhibidores de entrada de VIH. Se realiza una curva de inhibición log-sigmoidea, a partir de la cual se pueden obtener los valores de IC50, que son una medida de la resistencia del VIH a los compuestos evaluados.
3. Sumario
En su más amplio sentido, la invención proporciona métodos definidos en las reivindicaciones anexas.
En determinados aspectos, la invención proporciona un método para determinar si un virus de inmunodeficiencia humana (“VIH”) es resistente a un inhibidor de entrada de VIH. En un aspecto, la invención proporciona un método para determinar si un virus de inmunodeficiencia humano (“VIH”) es resistente a un inhibidor de entrada de VIH que comprende generar una curva log-sigmoidea de inhibición que comprende puntos de datos que miden la entrada del VIH a una célula en presencia de concentraciones variables del inhibidor de entrada de VIH; y comparar la curva de inhibición de la etapa (a) con una curva de inhibición log-sigmoidea de inhibición para un VIH de referencia. En determinadas realizaciones, la curva correspondiente al virus de referencia en el mismo tiempo o cerca de la curva log-sigmoidea del VIH. En determinadas realizaciones, la curva del virus de referencia puede ser una curva estándar conocida para el virus de referencia. Una disminución del porcentaje de inhibición máximo observado para el VIH respecto al observado para el VIH de referencia indica que el VIH es resistente al inhibidor de entrada de VIH y que el inhibidor de entrada de VIH es un inhibidor de entrada de VIH no competitivo. En determinadas realizaciones, el inhibidor de entrada se selecciona del grupo que consiste en SCH-C, SCH-D, UK-427857 y TNX-355. En determinadas realizaciones, el VIH de referencia es HXB2, NL4-3 o SF2. En determinadas realizaciones, el VIH procede de un sujeto infectado con VIH.
En determinadas realizaciones, los puntos de datos que miden la entrada del VIH en la célula se determinan poniendo en contacto una particular vírica de VIH con la célula en presencia del inhibidor de entrada de VIH, en donde la célula expresa un receptor de superficie celular al cual se une la partícula vírica, y en donde la partícula vírica comprende: (i) un vector de expresión vírica que carece de un ácido nucleico que codifica una proteína de cápsula vírica funcional, pero que comprende un ácido nucleico indicador que produce una señal detectable cuando se introduce en la célula, y (ii) una proteína de cápsula vírica codificada por un ácido nucleico del VIH; y medir la cantidad de señal detectable producida por la célula. En determinadas realizaciones, la señal detectable es una señal fluorescente. En determinadas realizaciones, el ácido nucleico indicador codifica luciferasa. En determinadas realizaciones, la partícula vírica se produce co-transfectando en una célula (i) un ácido nucleico que codifica una proteína de cápsula vírica del VIH, y (ii) un vector de expresión vírico que carece de un ácido nucleico que codifica una proteína de cápsula, en donde el vector comprende un ácido nucleico indicador que produce una señal detectable. En determinadas realizaciones, el receptor de superficie celular es CD4. En determinadas realizaciones, la célula también expresa un receptor de quimioquina. En determinadas realizaciones, el receptor de quimioquina es CXCR4 o CCR5. En determinadas realizaciones, el ácido nucleico de VIH codifica gp160, gp120 y/o gp41.
En otros aspectos, la invención proporciona un método para determinar si una población de VIH es resistente a un inhibidor de entrada de VIH, en donde el método comprende generar una curva de inhibición log-sigmoidea que comprende puntos de datos que miden la entrada de la población de VIH en una célula en presencia de concentraciones variables del inhibidor de entrada de VIH; y comparar la curva de inhibición de la etapa (a) con una curva de inhibición log-sigmoidea para una población de VIH de referencia. Un descenso en el porcentaje de inhibición máximo observado para la población de VIH respecto al observado para la población de VIH de referencia indica que el VIH es resistente al inhibidor de entrada de VIH y que el inhibidor de entrada de VIH es un inhibidor de entrada de VIH no competitivo.
La descripción proporciona un método para determinar si un VIH es resistente a un inhibidor de entrada de VIH que comprende determinar una curva de inhibición log-sigmoidea que comprende puntos de datos para la entrada del VIH en presencia de concentraciones variables del inhibidor de entrada de VIH, en donde si la entrada del VIH no puede ser inhibida completamente por el inhibidor de entrada de VIH, el VIH es resistente al inhibidor de entrada de VIH.
La descripción proporciona un método para determinar si una población de VIH es resistente a un inhibidor de entrada de VIH, que comprende determinar una curva de inhibición log-sigmoidea que comprende puntos de datos para la entrada de la población de VIH en presencia de concentraciones variables del inhibidor de entrada de VIH, en donde si la entrada de la población de VIH no puede ser inhibida completamente por el inhibidor de entrada de VIH, la población de VIH es resistente al inhibidor de entrada de VIH.
4. Breve descripción de las figuras
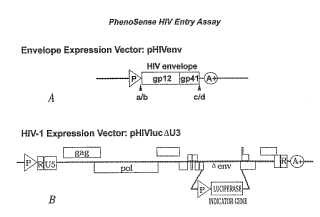
Figura 1A: Estructura de expresión de cápsula y vectores de expresión vírica.
El vector de expresión de cápsula de VIH (pHIVenv) se modifica para aceptar secuencias de cápsula que han sido amplificadas a partir de muestras de plasma del sujeto. Las designaciones a/b y c/d se refieren a sitios de endonucleasa de restricción posicionados en los extremos 5’ y 3’ de la poliproteína de cápsula de VIH-1 (gpl60) . El vector de expresión de VIH (pHIVlucLU3) codifica todas las proteínas de VIH excepto la poliproteína de cápsula. Se ha eliminado una porción del gen de cápsula para acomodar una casete de gen indicador, en este caso, luciferasa de luciérnaga que se usa para monitorizar la capacidad del virus para replicarse en presencia o ausencia de fármacos antivirales. La región 3’ U3 ha sido eliminada parcialmente para evitar la transcripción desde el 5’ LTR en células infectadas. El virus producido en este sistema se limita a una única ronda de replicación.
Figura 1B: Ensayo de entrada basado en célula La susceptibilidad a fármaco, el tropismo de co-receptor y la prueba de neutralización de virus se llevan a cabo mediante la co-transfección de una célula hospedante con pHIVenv y pHIVlucLU3. La célula hospedante produce partículas de VIH que son pseudo-tipadas con secuencias de cápsula de VIH derivadas del virus ensayado o de una muestra del sujeto. Se... [Seguir leyendo]
Reivindicaciones:
1. Un método para determinar si una población de VIH es resistente a un inhibidor de entrada de VIH, que comprende:
(a) generar una curva log-sigmoidea de inhibición que comprende puntos de datos que miden la entrada de la población de VIH en una célula en presencia de concentraciones variables del inhibidor de entrada de VIH que muestra un porcentaje de inhibición máxima para la población de VIH; y
(b) comparar la curva de inhibición de la etapa (a) con una curva log-sigmoidea de inhibición correspondiente a una población de VIH de referencia,
en donde un descenso en el porcentaje de inhibición máxima observado para la población de VIH respecto al observado para la población de VIH de referencia indica que el inhibidor de entrada de VIH es un inhibidor de entrada no competitivo y que el VIH es resistente al inhibidor de entrada de VIH no competitivo.
2. El método de la reivindicación 1, en el que el inhibidor de entrada se selecciona del grupo que consiste en SCH-C, SCH-D, UK-427857 y TNX-355.
3. El método de la reivindicación 1, en el que la población de VIH de referencia es una población de HXB2, NL4-3 o SF2.
4. El método de la reivindicación 1, en el que la población de VIH procede de un sujeto infectado con VIH.
5. El método de la reivindicación 1, en el que los puntos de datos que miden la entrada de la población de VIH en la célula se determinan:
(a) poniendo en contacto una pluralidad de partículas víricas de VIH con la célula en presencia del inhibidor de entrada de VIH, en donde la célula expresa un receptor celular superficial al cual se unen las partículas víricas, y en donde cada una de la pluralidad de partículas víricas comprende: (i) un vector de expresión vírica que carece de un ácido nucleico que codifica una proteína de cápsula vírica, pero que comprende un ácido nucleico indicador que produce una señal detectable cuando se introduce en la célula, y (ii) una proteína de cápsula vírica codificada por un ácido nucleico de la población de VIH; y
(b) midiendo la cantidad de señal detectable producida por la célula.
6. El método de la reivindicación 5, en el que cada una de la pluralidad de partículas víricas de VIH comprende la misma proteína de cápsula vírica.
7. El método de la reivindicación 5, en el que la señal detectable es una señal fluorescente.
8. El método de la reivindicación 5, en el que el ácido nucleico indicador codifica luciferasa.
9. El método de la reivindicación 5, en el que la pluralidad de partículas víricas son producidas co-transfectando en una célula (i) una pluralidad de ácidos nucleicos que contienen cada uno una proteína de cápsula vírica de la población de VIH, y (ii) un vector de expresión vírico que carece de un ácido nucleico que codifica una proteína de cápsula, en donde el vector comprende un ácido nucleico indicador que produce una señal detectable.
10. El método de la reivindicación 5, en el que el receptor celular superficial es CD4.
11. El método de la reivindicación 5, en el que la célula también expresa un receptor de quimioquina.
12. El método de la reivindicación 11, en el que el receptor de quimioquina es CXCR4 o CCR5.
13. El método de la reivindicación 11, en el que la célula expresa CXCR4 y CCR5.
14. El método de la reivindicación 5, en el que el ácido nucleico de VIH codifica gp120 o gp41.
15. Un método para determinar si una población de VIH es resistente a un inhibidor de entrada de VIH, que comprende determinar una curva log-sigmoidea de inhibición que comprende puntos de datos para la entrada de la población de VIH en presencia de concentraciones variables del inhibidor de entrada de VIH, en donde si la entrada de la población de VIH no puede ser inhibida completamente por el inhibidor de entrada de VIH, el inhibidor de VIH es un inhibidor de entrada no competitivo y la población de VIH es resistente al inhibidor de entrada de VIH no competitivo.
16. El método de la reivindicación 15, en el que el inhibidor de entrada se selecciona del grupo que consiste en SCH-C, SCH-D, UK-427857 y TNX-355.
17. El método de la reivindicación 15, en el que la población de VIH procede de un sujeto infectado con VIH.
18. El método de la reivindicación 15, en el que los puntos de datos que miden la entrada de la población de VIH en la célula se determinan:
(a) poniendo en contacto una pluralidad de partículas víricas de VIH con la célula en presencia del inhibidor de entrada de VIH, en donde la célula expresa un receptor celular superficial al cual se unen las partículas víricas, y en donde cada una de la pluralidad de partículas víricas comprende: (i) un vector de expresión vírica que carece de un ácido nucleico que codifica una proteína de cápsula vírica, pero que comprende un ácido nucleico indicador que produce una señal detectable cuando se introduce en la célula, y (ii) una proteína de cápsula vírica codificada por un ácido nucleico de la población de VIH; y (b) midiendo la cantidad de señal detectable producida por la célula.
19. El método de la reivindicación 18, en el que cada una de la pluralidad de partículas de VIH comprende la misma proteína de cápsula vírica.
20. El método de la reivindicación 18, en el que la señal detectable es una señal fluorescente.
21. El método de la reivindicación 18, en el que el ácido nucleico indicador codifica luciferasa.
22. El método de la reivindicación 18, en el que la pluralidad de partículas víricas se producen co-transfectando en una célula (i) una pluralidad de ácidos nucleicos que codifican cada uno una proteína de cápsula vírica de la población de VIH, y (ii) un vector de expresión vírico que carece de un ácido nucleico que codifica una proteína de cápsula, en donde el vector comprende un ácido nucleico indicador que produce una señal detectable.
23. El método de la reivindicación 18, en el que el receptor celular superficial es CD4.
24. El método de la reivindicación 18, en el que la célula también expresa un receptor de quimioquina.
25. El método de la reivindicación 24, en el que el receptor de quimioquina es CXCR4 o CCR5.
26. El método de la reivindicación 24, en el que la célula expresa CXCR4 y CCR5.
27. El método de la reivindicación 18, en el que el ácido nucleico de VIH codifica gp120 o gp41.
Patentes similares o relacionadas:
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Vacuna que comprende un pestivirus atenuado, del 27 de Mayo de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Un pestivirus atenuado, con al menos una mutación en la secuencia codificadora de la glicopoteína E ms y al menos otra mutación en la secuencia […]
Producción de partículas similares al virus de la gripe en plantas, del 6 de Mayo de 2020, de MEDICAGO INC.: Un ácido nucleico que comprende una región reguladora activa en una planta y un potenciador de la expresión activo en una planta, la región […]
Métodos mejorados para la inactivación del enterovirus, adsorción de adjuvante y composiciones de vacuna de dosis reducida obtenidas de los mismos, del 1 de Abril de 2020, de Serum Institute of India Private Limited: Un método para producir una composición que comprende partículas de poliovirus inactivado, caracterizado porque comprende las etapas de: a) producir […]
VIRUS VACUNAL SUS SCROFA FRENTE A LA PESTE PORCINA AFRICANA (ARMENIA/07) Y DERIVADOS DEL GENOTIPO II), del 12 de Marzo de 2020, de UNIVERSIDAD COMPLUTENSE DE MADRID (UCM): Virus vacunal sus scrofa frente a la peste porcina africana (armenia/O7) y derivados del genotipo ii) En esta invención se ha obtenido y caracterizado […]
Parvovirus atenuado vivo, del 19 de Febrero de 2020, de INTERVET INTERNATIONAL B.V: Parvovirus canino (CPV) atenuado vivo recombinante, caracterizado por que el genoma de dicho parvovirus comprende un gen de la cápside que codifica […]
Variante de la proteína ORF2 del PCV2 y partículas similares a virus compuestas por esta, del 1 de Enero de 2020, de Boehringer Ingelheim Animal Health USA Inc: Una proteína ORF2 de PCV2 que comprende o consiste en una secuencia de aminoácidos que tiene una identidad de secuencia de al menos 96 % con la […]
Cepas de virus vaccinia mutante, usos de estas y método para producirlas, del 4 de Diciembre de 2019, de TOT Shanghai R&D Center Co., Ltd: Una cepa de virus vaccinia mutante que puede replicarse de manera selectiva en células tumorales, y que ha disminuido la virulencia a células normales, en la que las secuencias […]