Composición de fosfenitoína.
Una composición farmacéutica acuosa que comprende 5,5-difenil-3-[(fosfonooxi)metil]-2,
4-imidazolidindiona o una de sus sales, y un tampón seleccionado de bicarbonato sódico, fosfato sódico, ácido bórico y glicina, en donde dicha composición tiene un pH de menos de 8,3.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2009/003563.
Solicitante: TEXCONTOR ETABLISSEMENT.
Nacionalidad solicitante: Liechtensein.
Dirección: Heiligkreuz 40 Postfach 39 9490 Vaduz LIECHTENSTEIN.
Inventor/es: TRUONG,Van Hung.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/675 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen el nitrógeno como heteroátomo de un ciclo, p. ej. fosfato de piridoxal.
- A61K9/08 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Soluciones.
PDF original: ES-2378373_T3.pdf
Fragmento de la descripción:
Composición de fosfenitoína.
Esta invención se refiere a composiciones farmacéuticas acuosas y a la aplicación de tales composiciones como agentes anticonvulsivos. En particular, la invención trata de composiciones acuosas que comprenden 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona (fosfenitoína) o una de sus sales de acuerdo con la reivindicación 1 que son estables a temperatura ambiente.
La 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona, conocida más comúnmente como fosfenitoína, es un profármaco de 5,5-difenilhidantoína. La 5,5-difenilhidantoína, denominada en la presente memoria posteriormente por su nombre trivial fenitoína, se usa comúnmente en el tratamiento y el manejo de estados convulsivos (p. ej. epilepsia y ataques). Su aplicación en el tratamiento de tales estados significa que a menudo es necesario que la fenitoína se administre parenteralmente, a menudo intravenosamente o intramuscularmente, en vez de oralmente. Sin embargo, la fenitoína es prácticamente insoluble en agua y por lo tanto tiene una baja biodisponibilidad. Por lo tanto, la fenitoína habitualmente tiene que disolverse en un medio acuoso alcalino de pH 12 para la administración. Sin embargo, el uso de tal pH alcalino puede provocar irritación.
Por otra parte, el uso de una solución acuosa no mitiga completamente los problemas asociados con la fenitoína. La baja solubilidad en agua de la fenitoína, por ejemplo, significa que tiene tendencia a precipitar durante y poco después del aporte haciendo dolorosa su administración parenteral. De hecho, siempre se ha referido que la precipitación durante el aporte intramuscular puede provocar daño a los tejidos y/o hemorragia, hematoma y necrosis en la zona de inyección. La precipitación durante y/o después de la administración también puede conducir a que se aporte una dosis menor de la pretendida (p. ej. si la fenitoína precipitada se queda en la aguja) así como a una liberación retardada de fenitoína y/o niveles en sangre de fenitoína erráticos.
Para evitar los problemas asociados con el uso de fenitoína se han desarrollado varios profármacos (documento US-A-4.260.769). Un profármaco que se ha encontrado que es particularmente útil es la fosfenitoína sódica, que es la sal disódica del éster de fosfato del derivado hidroximetílico de fenitoína. Este profármaco es vendido por Parke-Davis bajo la marca comercial Cerebyx®. Cerebyx® comprende una solución mixta disponible de 75 mg/ml de fosfenitoína sódica en agua y tampón de trometamina ajustada hasta pH 8,6 a 9,0 bien con ácido clorhídrico o bien con hidróxido sódico. Se recomienda que los viales que contienen la solución de Cerebyx® se almacenen en un refrigerador entre 2-8ºC lejos de luz y humedad. Tal almacenamiento a bajas temperaturas ayuda a prevenir la degradación de la sal disódica de fosfenitoína hasta fenitoína y otros productos de degradación tales como carbamoildifenilglicina.
El documento US-A-4.925.860 describe una investigación en la ruta de degradación de fosfenitoína hasta fenitoína y establece como hipótesis que la ruta avanza con un consumo global de hidroxilo y a través de la formación de uno o más de formaldehído, 5,5-difenil-4-imidazolidinona (DIZ), difenilglicinamida, difenilglicina y benzofenona. A la luz del consumo propuesto de hidroxilo, el documento US-A-4.925.860 recomienda la adición de un tampón, que sea capaz de prevenir la caída del pH, para influir en la estabilización.
El documento US-A-4.925.860 muestra además que la ruta de degradación cambia a medida que el pH cae y que debe mantenerse un pH alto para asegurar que la fenitoína de baja solubilidad no sea el principal producto de degradación. De acuerdo con esto, el documento US-A-4.925.860 muestra el uso de una formulación acuosa que comprende fosfenitoína y un tampón 0,05 a 0,2 M en la que el pH del sistema se mantiene entre 8,3 y 9,4.
De ahí que el intervalo de pH de 8,3 a 9,4 del documento US-A-4.925.860 y el pH de 8,6 a 9,0 de Cerebyx® pretenda asegurar que se produzcan las cantidades mínimas de fenitoína durante el almacenamiento de la solución de fosfenitoína. Por otra parte, sin embargo, pueden producirse cantidades significativas de otros productos de degradación. De hecho, el documento US-A-4.925.860 pretende específicamente optimizar el intervalo de pH de modo que el producto de degradación primario sea el compuesto que identifica como difenilglicinamida, en vez de eliminar la degradación de por sí. Así, según se muestra mediante los resultados del documento US-4.925.860, las soluciones acuosas que comprenden fosfenitoína y tampón (0,05 a 0,2 M), y que tiene un pH entre 8,3 y 9,4, tienden a sufrir degradación cuando se almacenan a temperatura ambiente. El producto de degradación principal es el compuesto identificado en el documento US-4.925.860 como difenilglicinamida, aunque a menudo también se produce formaldehído en cantidades significativas. Estos compuestos, junto con cantidades menores de fenitoína, difenilglicina, benzofenona y DIZ, pueden estar presentes en una cantidad total de hasta aproximadamente 15% en peso en una solución almacenada a temperatura ambiente o superior durante al menos 7 meses. Por lo tanto, la cantidad de fosfenitoína, y por lo tanto fenitoína, disponible para el aporte después del almacenamiento puede reducirse significativamente. Esto no sólo significa que puede aportarse finalmente a un paciente menos de la dosis recomendada de fosfenitoína, y por lo tanto fenitoína, sino también que se desconoce la cantidad exacta de fosfenitoína, y por lo tanto fenitoína, suministrada.
Los documentos WO9856422, US6133248 y Stella et al. Prodrug strategies to overcome poor water solubility. Advanced Drug Delivery Reviews. 24.08.2007 divulgan composiciones de fosfenitoína basadas en ciclodextrina. El documento US2007249563 analiza la prevención de la degradación durante la fabricación de fosfenitoína y de sus derivados.
Por lo tanto, sigue habiendo una necesidad de composiciones alternativas que comprendan fosfenitoína y en particular de composiciones que sean estables (p. ej. puedan almacenarse a temperatura ambiente sin sufrir degradación) y que puedan administrarse seguramente e indoloramente mediante la ruta parenteral. Se ha encontrado ahora sorprendentemente que una composición acuosa que comprende fosfenitoína, tampones seleccionados de bicarbonato sódico, fosfato sódico, ácido bórico, glicina y que tiene un pH de menos de 8,3 es estable durante períodos de tiempo prolongados incluso a temperatura ambiente. En particular, se ha encontrado que tales composiciones son resistentes a la degradación y producen solo pequeñas cantidades, si acaso, de fenitoína o cualquiera de los otros productos de degradación mencionados anteriormente cuando se almacenan a temperatura ambiente. Esto significa que las composiciones acuosas de la invención pueden usarse para administrar indoloramente y eficazmente una dosis conocida de fosfenitoína, y por lo tanto fenitoína, incluso después de un almacenamiento prolongado de la composición.
Así, vista desde un aspecto, la invención proporciona una composición farmacéutica acuosa que comprende 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona o una de sus sales, en donde dicha composición tiene un pH de menos de 8,3.
Vista desde un aspecto adicional, la invención proporciona un método de tratamiento de un sujeto humano o animal no humano que necesite tratamiento anticonvulsivo, comprendiendo dicho método administrar a dicho sujeto una cantidad eficaz de una composición farmacéutica acuosa que comprende 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona o una de sus sales, en el que dicha composición tiene un pH de menos de 8,3.
La 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona y sus sales para el uso de acuerdo con la invención pueden obtenerse a partir de fuentes comerciales o pueden prepararse usando procesos y procedimientos estándar bien conocidos por los expertos en la técnica. La 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona tiene la fórmula:
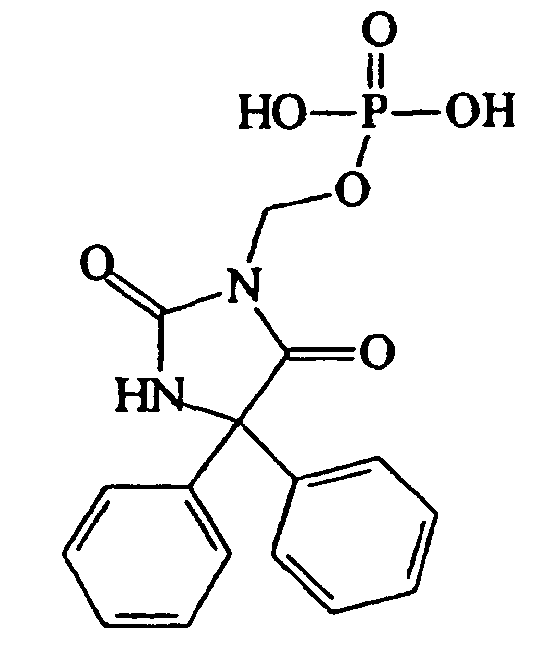
La 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona también se conoce como éster de fosfato de 3-(hidroxi- metil)-5,5-difenilhidantoína, fosfato de 2,5-dioxo-4,4-difenilimidazolidin-1-il-metilo y, según se menciona anterio rmente, fosfenitoína. El término 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona se usa en la presente memoria sinónimamente con todos estos... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica acuosa que comprende 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona o una de sus sales, y un tampón seleccionado de bicarbonato sódico, fosfato sódico, ácido bórico y glicina, en donde dicha composición tiene un pH de menos de 8,3.
2. Una composición de acuerdo con la reivindicación 1, en la que dicho pH es mayor de 7,5.
3. Una composición de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en la que dicha 5,5-difenil-3-[(fosfonooxi)metil]-2,4-imidazolidindiona está presente en la forma de su sal disódica.
4. Una composición farmacéutica acuosa de acuerdo con la reivindicación 1, para el uso en un tratamiento anticonvulsivo.
5. Una jeringa que contiene una composición farmacéutica acuosa de acuerdo con la reivindicación 1.
Patentes similares o relacionadas:
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Agente terapéutico para cáncer sólido, del 17 de Junio de 2020, de IDAC Theranostics, Inc: Un agente para uso en el tratamiento de cáncer sólido que comprende como principio activo un anticuerpo anti-CD4 que es un anticuerpo quimérico de tipo humano, un anticuerpo […]
Una terapia de combinación para un injerto estable y a largo plazo usando protocolos específicos para el agotamiento de los linfocitos T/B, del 20 de Mayo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Una dosis de células hematopoyéticas inmaduras de linfocitos T agotados, en donde dichas células hematopoyéticas inmaduras de linfocitos T agotados comprenden menos de 5 x 105 […]
Agente terapéutico para la disfunción meibomiana, del 6 de Mayo de 2020, de SANTEN PHARMACEUTICAL CO., LTD.: Una composición farmacéutica que comprende sirolimus a una concentración de 0,01 a 0,5% (p/v) como único ingrediente activo para uso en la supresión de la obstrucción de […]
Formulación de doxilamina y piridoxina y/o metabolitos o sales de estas, del 6 de Mayo de 2020, de DUCHESNAY INC.: Una forma de dosificación oral de liberación dual que comprende de 5 mg a 40 mg de doxilamina y/o una sal farmacéuticamente aceptable de esta y de 5 […]
Profármaco tenofovir éster monobencílico fosfamida, método de preparación y uso del mismo, del 6 de Mayo de 2020, de Jiangsu Tasly Diyi Pharmaceutical Co., Ltd: Un compuesto tenofovir éster monobencílico fosfamida de la fórmula general X, y el hidrato, solvato, sal farmacéuticamente aceptable del mismo o el isómero […]
Composición farmacéutica inyectable estable de antagonista del receptor de neuroquinina-1 y procedimiento para su preparación, del 29 de Abril de 2020, de PHARMATHEN S.A.: Una composición farmacéutica de liberación controlada para administración intramuscular o subcutánea que comprende Aprepitant o Fosaprepitant […]
Bisfosfonatos conjugados para el diagnóstico y la terapia de enfermedades óseas, del 22 de Abril de 2020, de SCV GmbH: Compuesto V para la complejación de isótopos metálicos, que comprende un quelante X y uno o varios vectores diana conjugados con el quelante X con la estructura -L1-R1-L2-R2-L3-R3, […]