Anticuerpo monoclonal específico para un epítopo de glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado.
Anticuerpo monoclonal específico para un epítopo único para una glicoproteína codificada por VIF inactivado,
seleccionada del grupo que consiste en gp95 o gp130, en el que el anticuerpo monoclonal reaccionaespecíficamente con o reconoce el epítopo de VIF inactivado o de glicoproteína de VIF inactivado, pero no reaccionacon ni reconoce el VIF vivo o la glicoproteína de VIF vivo, en el que dicho anticuerpo se produce a partir de la líneacelular depositada como número de la ATCC PTA-4837.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E03255660.
Solicitante: WYETH LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940 ESTADOS UNIDOS DE AMERICA.
Inventor/es: Chengjin,Michael Huang.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C07K16/10 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › de virus ARN.
- C12N15/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Preparación de células híbridas por fusión de dos o más células, p. ej. fusión de protoplastos.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- C12P21/08 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Anticuerpos monoclonales.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/569 G01N 33/00 […] › para microorganismos, p. ej. protozoarios, bacterias, virus.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
PDF original: ES-2383075_T3.pdf
Fragmento de la descripción:
Anticuerpo monoclonal específico para un epítopo de glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado.
Antecedentes de la invención
El virus de la inmunodeficiencia felina (VIF) , originariamente lentivirus linfotrópico T felino, se describió por primera vez por Pederson y col., Science, (1987) 235: 790-793 y se ha identificado en gatos domésticos y guepardos. La infección es endémica en gatos de todo el mundo. Como el VIH, el VIF es una preocupación internacional. De acuerdo con la American Association of Feline Practitioners, hasta uno de cada doce gatos puede dar positivo en un ensayo para VIF. Después de la infección, existe un periodo transitorio de fiebre, linfadenopatía y neutropenia. La mayoría de los gatos se recuperan de esta fase y parecen normales durante meses o años antes de que aparezca la inmunodeficiencia. Debido a esta manifestación de inmunodeficiencia latente, sería excesivamente peligroso utilizar una vacuna de virus vivo para el tratamiento o la prevención del VIF. Aunque se conocen anticuerpos monoclonales específicos para epítopos de antígenos o proteínas antigénicas codificadas por el VIF, es decir, los documentos US
5.177.014 y US 5.219.725, estos anticuerpos no son capaces de reconocer el VIF inactivado. Esto significa que para las vacunas de VIF comerciales actuales, todas las cuales utilizan VIF inactivado, no se conocen anticuerpos monoclonales útiles para la determinación de la cantidad de virus o de la potencia del componente de VIF inactivado en una composición de vacuna.
El documento WO94/20622 desvela un fragmento polipeptídico capaz de inducir anticuerpos neutralizantes contra el VIF, el documento WO92/15684 desvela la proteína gag p24 y la glicoproteína 160 del VIF recombinante. El documento WO90/06510 desvela anticuerpos monoclonales contra el lentivirus linfotrópico T felino.
Por lo tanto, un objeto de la presente invención es proporcionar un anticuerpo monoclonal específico para un epítopo de una glicoproteína de VIF inactivado.
Otro objeto de la presente invención es proporcionar un procedimiento para la determinación de la cantidad de un VIF inactivado.
Un objeto adicional de la presente invención es proporcionar un procedimiento para determinar la potencia de una vacuna de VIF inactivado.
Una característica de la presente invención es que el anticuerpo monoclonal de la invención es específico para el epítopo de una glicoproteína de VIF inactivado y no reconoce epítopos de glicoproteínas, proteínas o antígenos de VIF vivo.
Otros objetos y características de la invención se harán más evidentes a partir de la descripción detallada expuesta a continuación en el presente documento.
Sumario de la invención
La presente invención proporciona un anticuerpo monoclonal específico para un epítopo único para una glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado, seleccionada del grupo que consiste en gp95 o gp130, en el que el anticuerpo monoclonal reacciona específicamente con o reconoce el epítopo de VIF inactivado o la glicoproteína de VIF inactivado, pero no reacciona con ni reconoce el VIF vivo o la glicoproteína de VIF vivo, en el que dicho anticuerpo se produce a partir de la línea celular depositada como número de la ATCC PTA-4837.
La presente invención proporciona además un procedimiento para la detección de un epítopo único para una glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado en una muestra, que comprende: poner en contacto dicha muestra con un anticuerpo monoclonal específico para un epítopo único para una glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado para formar un complejo; y detectar dicho complejo.
Seleccionada del grupo que consiste en gp95 o gp130, en el que el anticuerpo monoclonal reacciona específicamente con o reconoce el epítopo de VIF inactivado o la glicoproteína de VIF inactivado, pero no reacciona con ni reconoce el VIF vivo o la glicoproteína de VIF vivo, en el que dicho anticuerpo se produce a partir de la línea celular depositada como número de la ATCC PTA-4837.
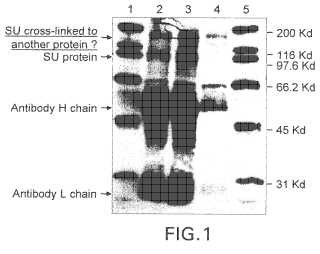
Breve descripción del dibujo La FIG. 1 es una fotografía de un análisis de inmunotransferencia de Western del anticuerpo monoclonal, AcM 1 D9, identificado como específico para un epítopo único de una glicoproteína codificada por el virus de la inmunodeficiencia felina inactivado.
La FIG 1 se describe además de la forma siguiente: Inmunoprecipitación de glicoproteínas de la envuelta del VIF con el anticuerpo monoclonal 1D9. Una reserva de virus enriquecida en VIF inactivado con formalina se biotiniló con sulfo-NHS-LC-biotina y se extrajo con Triton X-100. La inmunoprecipitación se llevó a cabo por incubación del extracto con el AcM 1 D9 o H5332. Los inmunocomplejos se recogieron sobre Proteína G inmovilizada, se lavaron y se sometieron a SDS-PAGE y transferencia de Western. Las proteínas en la transferencia se detectaron usando estreptavidina marcada con peroxidasa. Carriles 1 y 5, marcador de peso molecular biotinilado; carril 2, 20 ul de AcM 1 D9 usado para la inmunoprecipitación; carril 3, 100 ul de 1 D9 usado para la inmunoprecipitación; carril 4, 100 ul de un anticuerpo monoclonal irrelevante, H5332, usado en la inmunoprecipitación. Las cadenas H (50 Kd) y L (25 Kd) de los anticuerpos y alguna BSA (67 Kd) no se tiñeron específicamente por la estreptavidina marcada con peroxidasa.
Descripción detallada de la invención La glicoproteína de la envuelta del virus de la inmunodeficiencia felina (VIF) está implicada en interacciones de receptores con células, y esta interacción determina la susceptibilidad de las células a dicho virus. La glicoproteína de la envuelta del VIF también está implicada en la penetración del virus y en la formación de sincitios, y es la diana primaria para respuestas inmunes humorales y celulares. (Bendinelli, M., y col., Clinical Microbiology Review, (1995)
8: 87-112) . Dicha glicoproteína de la envuelta consiste en dos componentes que están unidos no covalentemente en el virión, la proteína de superficie (SU) , que está fuertemente glicosilada y tiene un peso molecular aparente de 95.000-100.000, y la proteína transmembrana (TM) , que está menos glicosilada y tiene un peso molecular aparente de 35.000-40.000. (Pacino, G. y col., Virology, (1995) 206: 796-806) . Diversos estudios han sugerido que la proteína de la envuelta del VIF es capaz de inducir inmunidad protectora frente al VIF en gatos. Por lo tanto, un ensayo inmunoabsorbente ligado a enzimas (ELISA) que mide la cantidad relativa o pureza de la proteína de la envuelta del VIF sería más útil para determinar la potencia de una vacuna para el VIF. Sin embargo, todas las vacunas para el VIF disponibles en el mercado en la actualidad utilizan virus muerto o inactivado, y los anticuerpos monoclonales que se sabe que reaccionan con o reconocen el VIF o la glicoproteína del VIF no reaccionan con ni reconocen el VIF
o la glicoproteína del VIF inactivado. Se propone que la inactivación de dicho virus puede alterar la conformación de la proteína de la envuelta del VIF.
Sorprendentemente, ahora se ha descubierto que el anticuerpo monoclonal, denominado AcM 1 D9, reconoce específicamente sólo el VIF inactivado y no reconoce el VIF vivo. Además, los experimentos de ELISA e inmunoprecipitación demuestran que el anticuerpo monoclonal de la invención reacciona específicamente con el componente de proteína de superficie de la glicoproteína de la envuelta del VIF.
La expresión anticuerpo monoclonal, como se usa en la memoria descriptiva y en las reivindicaciones, designa un anticuerpo producido a partir de una sola célula productora de anticuerpo que se ha clonado para producir una línea celular productora de anticuerpo. El término epítopo designa una secuencia de aminoácidos específica, secuencia de aminoácidos modificada o estructura secundaria o terciaria de proteína que es reconocida por un anticuerpo. La expresión virus inactivado designa un virus "no vivo" o "muerto".
El anticuerpo monoclonal de la invención puede prepararse usando técnicas convencionales conocidas en la materia. Por ejemplo, pueden inmunizarse ratones con un virus inactivado parcialmente purificado tal como VIF-Shiz, VIF-Petaluma o similar, preferentemente VIF-Shiz; después se exploran extracciones de sangre de la cola de ratón para determinar la respuesta de anticuerpos y se seleccionan... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo monoclonal específico para un epítopo único para una glicoproteína codificada por VIF inactivado, seleccionada del grupo que consiste en gp95 o gp130, en el que el anticuerpo monoclonal reacciona específicamente con o reconoce el epítopo de VIF inactivado o de glicoproteína de VIF inactivado, pero no reacciona con ni reconoce el VIF vivo o la glicoproteína de VIF vivo, en el que dicho anticuerpo se produce a partir de la línea celular depositada como número de la ATCC PTA-4837.
2. Anticuerpo monoclonal de acuerdo con la reivindicación 1, en el que el VIF inactivado es VIF-Shiz o VIF-Petaluma.
3. Anticuerpo monoclonal de acuerdo con la reivindicación 1, en el que dicha glicoproteína es gp95.
4. Anticuerpo monoclonal de acuerdo con la reivindicación 2, en el que dicho VIF es VIF-Shiz.
5. Anticuerpo monoclonal de acuerdo con cualquiera de las reivindicaciones anteriores, en el que dicho VIF se ha inactivado por tratamiento con formalina.
6. Un procedimiento para la detección de un epítopo único para una glicoproteína codificada por VIF inactivado en una muestra, que comprende: poner en contacto dicha muestra con un anticuerpo monoclonal de acuerdo con una cualquiera de las reivindicaciones 1-5 específico para un epítopo único para una glicoproteína codificada por VIF inactivado para formar un complejo; y detectar dicho complejo.
7. Un procedimiento para determinar la cantidad de un VIF inactivado en una muestra, que comprende: poner en contacto dicha muestra con un anticuerpo monoclonal de acuerdo con la reivindicación 1 para formar un complejo; y detectar dicho complejo.
8. Un procedimiento para determinar la potencia de un VIF inactivado en una muestra, que comprende: poner en contacto dicha muestra con un monoclonal de acuerdo con la reivindicación 1 para formar un complejo; y detectar dicho complejo.
9. El procedimiento de acuerdo con la reivindicación 7 u 8, en el que el anticuerpo monoclonal es un anticuerpo monoclonal como se define en cualquiera de las reivindicaciones 1 a 5.
10. Un procedimiento para la preparación de anticuerpos monoclonales de acuerdo con la reivindicación 1, que comprende inmunizar a un ratón con un VIF inactivado parcialmente purificado, explorar el huésped para una alta respuesta de anticuerpos específicos de VIF, fusionar esplenocitos de dicho huésped con una línea celular de mieloma adecuada para generar células de hibridoma, explorar dichas células de hibridoma para una reactividad específica con VIF inactivado, y después seleccionar un clon estable, cultivar dicho clon estable y recoger los anticuerpos monoclonales deseados.
11. El procedimiento de acuerdo con la reivindicación 10, en el que el VIF inactivado es VIF-Shiz o VIF-Petaluma.
12. El procedimiento de acuerdo con la reivindicación 10 u 11, en el que dicho VIF es VIF-Shiz.
13. El procedimiento de acuerdo con cualquiera de las reivindicaciones 10 a 12, en el que dicho VIF ha sido inactivado por tratamiento con formalina.
14. La línea celular depositada en la Colección Americana de Cultivos Tipo con el Nº de Acceso PTA-4837.
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Bebidas energéticas y otras ayudas nutricionales derivadas de licores a base de agave, del 1 de Julio de 2020, de Roar Holding, LLC: Una composición que comprende compuestos inhibidores de monoamino oxidasa (MAO), cuya composición se prepara mediante la eliminación de etanol de una bebida […]
Evaluación asistida del pronóstico en la enfermedad inflamatoria, del 24 de Junio de 2020, de KINGS COLLEGE LONDON: Un método in vitro de recopilación de información útil para predecir el resultado clínico en un sujeto, en donde el sujeto tiene o se sospecha que tiene una enfermedad […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Marcadores celulares para el diagnóstico de la enfermedad de Alzheimer y para la progresión de la enfermedad de Alzheimer, del 17 de Junio de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un método para el diagnóstico de la probabilidad de la enfermedad de Alzheimer (EA) en un individuo examinado, que comprende: (i) medir los […]
Biomarcadores de TB, del 22 de Abril de 2020, de United Kingdom Research and Innovation: Un método para el diagnóstico de TB en un sujeto, comprendiendo el método: (a) proporcionar una muestra de dicho sujeto, siendo dicha muestra seleccionada […]
Procedimiento para detectar bacterias coliformes contenidas en la leche, del 15 de Abril de 2020, de ASAHI KASEI KABUSHIKI KAISHA: Procedimiento para lisar bacterias coliformes contenidas en la leche, que comprende la etapa de mezclar un agente de lisis que contiene lisozima, un surfactante aniónico […]