Animales transgénicos que comprenden un sistema inmunitario humanizado.
Un animal transgénico no humano capaz de producir TCR humano con un repertorio de TCRs sustancial,
quecomprende:
loci del receptor de células T endógeno inactivados que son loci del receptor de cadena α y β; y
transgenes contenidos en su genoma compuesto de loci del receptor de células T humano que son loci del receptorde cadena α y β;
en el que dichos loci del receptor de células T humano no están reordenados.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2001/049413.
Solicitante: ALTOR BIOSCIENCE CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2810 NORTH COMMERCE PARKWAY MIRAMAR, FLORIDA 33025 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WONG, HING, C., WEIDANZ, JON, A., BELMONT,HEATHER J, WITTMAN,VAUGHAN P.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
PDF original: ES-2389251_T3.pdf
Fragmento de la descripción:
Animales transgénicos que comprenden un sistema inmunitario humanizado
Campo de la invención
La presente invención se refiere a animales transgénicos no humanos capaces de producir receptores de células T (TCRs) humanos funcionales, moléculas heterólogas del Complejo Mayor de Histocompatibilidad (MHC) y moléculas correceptoras, así como a métodos y transgenes para producir los animales transgénicos. Los animales y proteínas heterólogas producidos son útiles para una variedad de aplicaciones, incluyendo el desarrollo de nuevos compuestos terapéuticos y vacunas.
Antecedentes de la invención
La industria biofarmacéutica se ha construido sobre el éxito del desarrollo de agentes proteicos como compuestos terapéuticos, por ejemplo para tratar enfermedades en seres humanos y animales. El desarrollo de compuestos biofarmacéuticos ha estado conducido por el uso de tecnología de ADN recombinante o ingeniería genética para clonar y expresar las proteínas de interés y manipular mediante ingeniería su fabricación a escala comercial. El campo ha evolucionado hasta el punto en el que se reconoce y acepta que las proteínas producidas para uso en seres humanos deberían contener tanta más secuencia humana como sea posible para asegurarse que el compuesto terapéutico proteico será menos probable que provoque una respuesta de anticuerpo en el paciente tratado. Esto ha conducido a una serie de desarrollos para producir proteínas más completamente humanas.
El sistema de respuesta inmunitaria humano es un sistema de defensa muy complejo y eficiente frente a organismos invasores. Recientemente, ha habido un aumento de interés en el uso de componentes del sistema inmunitario del propio cuerpo como agentes terapéuticos para modular o inducir un ataque inmunitario en un estado de enfermedad,
o para inhibir un ataque en un trastorno autoinmunitario. Las moléculas terapéuticas que imitan a componentes del sistema inmunitario nativos se integrarían en los mecanismos de defensa naturales del cuerpo y de este modo proporcionarían un método eficiente de tratamiento para tales enfermedades. Como resultado de tales esfuerzos, se ha desarrollado recientemente un número de productos de anticuerpos, y se han aprobado como compuestos terapéuticos para uso humano. Muchos de estos se desarrollaron originalmente como anticuerpos monoclonales murinos; sin embargo, los anticuerpos murinos provocan generalmente una respuesta de anticuerpo anti-ratón de humano (HAMA) en la que el sistema inmunitario del paciente produce anticuerpos frente al anticuerpo terapéutico. En respuesta a tales efectos, se desarrollaron métodos para crear anticuerpos quiméricos o anticuerpos “humanizados”, en los que las regiones constantes murinas o las regiones de armazón del anticuerpo se sustituyeron por secuencias humanas. Otro enfoque ha sido crear animales transgénicos en los que los genes de los anticuerpos murinos se han suprimido o inactivado y se han sustituido por genes de anticuerpos humanos (Lonberg y Kay, patente US 5.877.397, Kucherlapati et al. US 6.150.584 A, Abgenix Inc. documento WO 98/24893 A2) . Estos animales transgénicos son capaces de producir anticuerpos humanos en respuesta a la vacunación.
Las células T son las células efectoras primarias implicadas en la respuesta celular. Al igual que los anticuerpos se han desarrollado como compuestos terapéuticos, (TCRs) , los receptores sobre la superficie de las células T, que les dan su especificidad, tienen ventajas únicas como plataforma para desarrollar compuestos terapéuticos. Aunque los anticuerpos están limitados para el reconocimiento de patógenos en la sangre y espacios extracelulares, o para dianas proteicas sobre la superficie celular, los TCRs reconocen antígenos presentados por moléculas de MHC sobre las superficies de las células (incluyendo antígenos derivados de proteínas intracelulares) . Dependiendo del subtipo de células T que reconocen el antígeno presentado y se activan, los TCRs y los TCRs que poseen células T participan en el control de diversas respuestas inmunitarias. Por ejemplo, las células T auxiliares están implicadas en la regulación de la respuesta inmunitaria humoral a través de la inducción de la diferenciación de células B en células que segregan anticuerpos. Además, las células T auxiliares activadas inician respuestas inmunitarias mediadas por células mediante células T citotóxicas. De este modo, los TCRs reconocen específicamente dianas que no son vistas normalmente por anticuerpos, y también disparan a las células T que poseen para iniciar una amplia variedad de respuestas inmunitarias.
Una célula T reconoce un antígeno presentado sobre las superficies de las células por medio de los TCRs expresados sobre su superficie celular. Los TCRs son heterodímeros enlazados mediante disulfuro, consistiendo la mayoría en glucoproteínas de cadenas ! y ∀. Las células T usan mecanismos de recombinación para generar diversidad en sus moléculas receptoras similares a aquellos mecanismos para generar diversidad de anticuerpos que operan en células B (Janeway y Travers, Immunobiology 1997) . Similar a los genes inmunoglobulínicos, los genes de TCR están compuestos de segmentos que se reordenan durante el desarrollo de las células T. Los polipéptidos de TCR consisten en regiones variables, constantes, transmembránicas y citoplásmicas. Mientras que la región transmembránica ancla la proteína, y la región intracelular participa en la señalización cuando el receptor está ocupado, la región variable es responsable del reconocimiento específico de un antígeno, y la región constante mantiene la superficie de unión de la región variable. La cadena ! de TCR contiene regiones variables codificadas por segmentos variables (V) y de unión (J) solamente, mientras que la cadena ∀ contiene segmentos de diversidad
(D) adicionales.
Los segmentos V, D y J de las cadenas de PCR están presentes en múltiples copias en ADN de la línea germinal. La diversidad del repertorio de células T y la capacidad para reconocer diversos antígenos se genera a través de un proceso de recombinación al azar que da como resultado la unión de un miembro de cada familia de segmentos para generar una única molécula que codifica una única cadena ! o ∀ de TCR. Aunque este proceso de reordenamiento se produce en ambos alelos en la célula T, la exclusión alélica da como resultado sólo un TCR expresado por célula T (Janeway y Travers, Immunobiology, 1997) .
Un TCR reconoce un antígeno peptídico presentado sobre las superficies de células presentadoras de antígenos en el contexto de moléculas auto- (MHC) . Dos tipos diferentes de moléculas del MHC reconocidas por TCRs están implicados en la presentación de antígenos. Las moléculas del MHC de clase I y las moléculas del MHC de clase II. Los subconjuntos de células T maduras se definen por las moléculas correceptoras que expresan. Estos correceptores actúan conjuntamente con los TCRs en el reconocimiento del complejo de MHC-antígeno y la activación de la célula T. Las células T auxiliares maduras reconocen antígeno en el contexto de moléculas del MHC clase II, y se distinguen por tener el correceptor CD4. Las células T citotóxicas reconocen antígeno en el contexto de determinantes del MHC clase I, y se distinguen por tener el correceptor CD8.
Debido a la especificidad de los TCRs y su capacidad para reconocer diversas amenazas e iniciar una respuesta inmunitaria natural, actualmente los TCRs se están evaluando para uso como una plataforma para desarrollar compuestos terapéuticos. En un ejemplo, los TCRs humanos se conjugan químicamente a un fármaco contra el cáncer, a fin de usar la especificidad del TCR para guiar y suministrar el fármaco a células que el TCR puede reconocer. En otro ejemplo, el gen de TCR se fusiona genéticamente (o se conjuga químicamente) a una proteína biológicamente activa (por ejemplo citocina, quimiocina o linfocina) , y de este modo suministra o dirige el agente activo hacia el sitio de acción por medio de la especificidad de TCR. En un tercer ejemplo, los TCRs están enlazados a un anticuerpo específico para un tipo celular, de manera que el anticuerpo puede reclutar una célula efectora y dirigir o guiar a la célula efectora hacia la vecindad de la célula diana, que el TCR reconoce. En un ejemplo adicional, se ha desarrollado una estirpe celular de hibridoma de célula T murina que carece de cadenas de TCR endógenas, que expresa las regiones variables ! y ∀ y la región constante ∀... [Seguir leyendo]
Reivindicaciones:
1. Un animal transgénico no humano capaz de producir TCR humano con un repertorio de TCRs sustancial, que comprende:
loci del receptor de células T endógeno inactivados que son loci del receptor de cadena ! y ∀; y
transgenes contenidos en su genoma compuesto de loci del receptor de células T humano que son loci del receptor de cadena ! y ∀;
en el que dichos loci del receptor de células T humano no están reordenados.
2. El animal transgénico no humano de la reivindicación 1, en el que dichos loci del receptor de células T humano están compuestos, en enlazamiento operable, de una pluralidad de genes V del receptor de células T humano, y genes D y/o J y C.
3. El animal transgénico no humano de una de las reivindicaciones 1 ó 2, en el que dicho animal es capaz de reordenamiento VDJC productivo y expresar receptores de células T humanos.
4. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-3, en el que dichos transgenes sufren reordenamiento VDJC productivo en linfocitos de dicho animal transgénico no humano, y en el que las células T expresan cantidades detectables de TCR transgénico en respuesta a la estimulación antigénica.
5. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-4, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a un antígeno, y en el que los receptores de células T comprenden un receptor de células T humano.
6. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-5, en el que un receptor de células T humano producido está compuesto de cadenas ! y ∀ humanas.
7. El animal transgénico no humano de una cualquiera de las reivindicaciones anteriores, que comprende además:
transgenes contenidos en su genoma compùesto de genes HLA humanos de loci de MHC humanos.
8. El animal transgénico no humano de la reivindicación 7, en el que dichos loci de MHC contienen todos los genes HLA humanos.
9. El animal transgénico no humano de la reivindicación 7, en el que dichos loci de MHC contienen una porción de los genes HLA humanos.
10. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-9, en el que dichos genes HLA humanos son MHC clase I y MHC clase II.
11. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-10, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a un antígeno presentado por receptores de MHC clase I humanos, y/o que reaccionan frente a un antígeno presentado por receptores de MHC clase II humanos.
12. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-11, en el que dichos genes HLA humanos son MHC clase I.
13. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-12, en el que dichos genes HLA humanos son HLA-A2.
14. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-13, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a un antígeno presentado por receptores de MHC clase I humanos.
15. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-11, en el que dichos genes HLA humanos son MHC clase II.
16. El animal transgénico no humano de la reivindicación 15, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a un antígeno presentado por receptores de MHC clase II humanos.
17. El animal transgénico no humano de una cualquiera de las reivindicaciones 7-16, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta
inmunitaria una población de células T que reaccionan frente a un antígeno, y en el que los receptores de células T comprenden cadenas ! y ∀ humanas.
18. Un animal transgénico no humano de una cualquiera de las reivindicaciones anteriores, que comprende además genes contenidos en su genoma un correceptor humano.
19. El animal transgénico no humano de la reivindicación 18, en el que dichos genes codifican un correceptor CD8 y/o un correceptor CD4.
20. El animal transgénico no humano de la reivindicación 18 o reivindicación 19, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente al antígeno, y en el que los receptores de células T comprenden receptores de células T humanos y moléculas correceptoras.
21. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-20, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a antígeno presentado por receptores de MHC clase I humanos, y/o que reaccionan frente a un antígeno presentado por receptores de MHC clase II humanos.
22. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-21, en el que dicho correceptor es un correceptor CD8.
23. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-22, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente al antígeno y en el que las células T expresan sobre su superficie celular receptores de células T humanos y moléculas correceptoras CD8.
24. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-23, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a antígeno presentado por receptores de MHC clase I humanos.
25. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-21, en el que dicho correceptor es un correceptor CD4.
26. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-21 y 26, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente al antígeno y en el que las células T expresan sobre su superficie celular receptores de células T humanos y moléculas correceptoras CD4.
27. El animal transgénico no humano de una cualquiera de las reivindicaciones 18-21, 25 y 26, en el que dicho animal transgénico no humano produce una respuesta inmunitaria frente a un antígeno, comprendiendo dicha respuesta inmunitaria una población de células T que reaccionan frente a antígeno presentado por receptores de MHC clase II humanos.
28. El animal transgénico no humano de una cualquiera de las reivindicaciones anteriores, en el que dicho animal es cualquier animal que se puede manipular transgénicamente.
29. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es un ratón.
30. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es una rata.
31. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es un primate.
32. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es un chimpancé.
33. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es una cabra.
34. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es un cerdo.
35. El animal transgénico no humano de una cualquiera de las reivindicaciones 1-28, en el que dicho animal es un pez zebra.
36. Un método para producir un animal transgénico no humano según la reivindicación 1, que comprende las etapas de:
inactivar loci de receptores de células T endógenos que son loci de receptores de célula T de cadena ! y ∀ en un embrión no humano o una célula madre embriónica no humana;
insertar transgenes que contienen loci de receptores de células T humanos activos que son loci de receptores de cadenas ! y ∀ en dicho embrión no humano o célula madre embriónica no humana;
producir un animal transgénico a partir de dicho embrión no humano o célula madre embriónica no humana que contiene el transgén humano activo, en el que el animal es capaz de producir células T que expresan receptores de células T humanos; y
reproducir el animal transgénico según sea necesario para producir el animal transgénico de la reivindicación
1.
37. Un método para producir un animal transgénico no humano según la reivindicación 1, que comprende las etapas de:
inactivar loci de receptores de células T endógenos en un embrión no humano o célula madre embriónica no 15 humana, en el que dichos loci son loci de receptores de células T ! o de receptores de células T ∀;
producir un animal transgénico a partir de dicho embrión no humano o célula madre embriónica no humana que contiene loci activados, en el que el animal es incapaz de expresar dichos loci endógenos;
cruzar un animal transgénico producido que tiene loci de receptores de células T ! endógenos inactivados con un animal transgénico producido que tiene loci de receptores de células T ∀ endógenos inactivados;
seleccionar la progenie que tiene los loci tanto de los receptores de células T ! como de los receptores de células T ∀ endógenos inactivados;
insertar trasngenes que contienen loci de receptores de células T humanos activos en un embrión no humano
o célula madre embriónica no humana, en el que dichos loci de receptores de células T humanos son loci de receptores de células T ! o de receptores de células T ∀ humanos;
producir un animal transgénico a partir de dicho embrión no humano o célula madre embriónica no humana que contiene el transgén humano activo;
cruzar un producto transgénico animal que tiene transgenes de receptores de células T ! humanos activos con un animal transgénico producido que tiene transgenes de receptores de células T ∀ humanos activos;
seleccionar la progenie que tiene los transgenes tanto de los receptores de células T ! como de los 30 receptores de células T ∀ humanos activos, en el que el animal es capaz de producir células T que expresan receptores de células T humanos;
cruzar un animal transgénico producido que tiene loci tanto de los receptores de células T ! como de los receptores de células T ∀ endógenos inactivados con un animal transgénico producido que tiene transgenes tanto de receptores de células T ! como de receptores de células T ∀ humanos activos;
seleccionar la progenie que tiene loci de receptores de células T ! y de receptores de células T ∀ endógenos inactivados y que contiene transgenes de receptores de células T ! y de receptores de células T ∀ humanos activos; y
reproducir el animal transgénico según sea necesario para producir el animal transgénico de la reivindicación
1.
38. El método de una cualquiera de las reivindicacione.
3. 37, en el que dichos loci de receptores de células T endógenos se inactivan mediante una limitación funcional de los loci.
39. El método de una cualquiera de las reivindicacione.
3. 37, en el que dichos loci de receptores de células T endógenos se inactivan suprimiendo los genes del segmento J a partir de dichos loci.
40. El método de una cualquiera de las reivindicacione.
3. 37, en el que dichos loci de receptores de células T 45 endógenos se inactivan suprimiendo los genes del segmento D de dichos loci.
41.
3. 37, en el que dichos loci de receptores de células T endógenos se inactivan suprimiendo los genes del segmento C de dichos loci.
42.
3. 37, en el que dichos loci de receptores de células T humanos están no reordenados.
43.
3. 37, en el que dichos transgenes que contienen los loci de
receptores de células T humanos comprenden, en enlazamiento operable, una pluralidad de genes V y genes D y/o 5 J y C de receptores de células T humanos.
44. Un método para producir un animal transgénico no humano según la reivindicación 1, capaz además de producir moléculas heterólogas de MHC, que comprende las etapas de:
cruzar un animal transgénico que expresa receptores de clls T humanos producidos mediante el método de la reivindicación 36 con un animal transgénico que contiene loci de MHC humano y que expresa moléculas de 10 MHC humano;
seleccionar la descendencia de animales transgénicos que expresan receptores de células T humanos y moléculas heterólogas de MHC; y
reproducir el animal transgénico según sea necesario para producir el animal transgénico de la reivindicación 1, capaz además de producir moléculas heterólogas de MHC.
45. El método de la reivindicación 44, en el que dichos loci de MHC contienen todos los genes HLA humanos.
46. El método de la reivindicación 44, en el que dichos loci de MHC contienen una porción de los genes HLA humanos.
47.
4. 46, en el que dichos genes HLA humanos son MHC clase I y MHC clase II.
48. El método de una cualquiera de las reivindicacione.
4. 47, en el que dichos genes HLA humanos son MHC clase I.
49. El método de una cualquiera de las reivindicacione.
4. 47, en el que dichos genes HLA humanos son MHC clase II.
50. Un método para producir un animal transgénico no humano según la reivindicación 1, capaz además de producir 25 moléculas heterólogas de MHC, y moléculas de correceptores heterólogos, que comprende las etapas de:
cruzar un animal transgénico que expresa receptores de células T humanos y moléculas heterólogas de MHC producidos mediante el método de la reivindicación 44 con un animal transgénico que contiene genes de correceptor heterólogo;
seleccionar progenie de los animales transgénicos que expresan receptores de células T humanos, 30 moléculas heterólogas de MHC, y moléculas de correceptores heterólogos; y
reproducir el animal transgénico según sea necesario para producir el animal transgénico de la reivindicación 1, capaz además de producir moléculas heterólogas de MHC y moléculas de correceptores heterólogos.
51. El método de la reivindicación 50, en el que dicho correceptor heterólogo es un correceptor CD8 y un correceptor CD4.
52. El método de la reivindicación 50, en el que dicho correceptor heterólogo es un correceptor CD8.
53. El método de la reivindicación 50, en el que dicho correceptor heterólogo es un correceptor CD4.
54. Un método para generar una línea celular inmortal capaz de producir receptores de células T humanos, que comprende las etapas de: producir un animal transgénico capaz de producir receptores de células T humanos mediante el método de la 40 reivindicación 37; inducir una respuesta inmunitaria en dicho animal;
aislar una célula T que expresa receptores de células T humanos; y fusionar la célula T aislada con una estirpe celular inmortalizante para generar una estirpe celular inmortal capaz de producir receptores de células T humanos.
45 55. El método de la reivindicación 54, en el que dicha célula T aislada expresa TCR específico para un antígeno particular de interés.
56. El método de la reivindicación 54 o reivindicación 55, en el que dicha célula T aislada expresa TCR capaz de reaccionar con un complejo péptido/MHC de interés.
57.
5. 56, en el que dicha estirpe celular inmortalizante es una estirpe celular de mieloma.
58. El animal transgénico no humano de la reivindicación 1, que contiene además en su genoma transgenes que comprenden, en enlazamiento operable, una pluralidad de genes V y sus genes D y/o J y C de receptores de células T humanos.
59. El animal transgénico no humano de la reivindicación 1, en el que los transgenes contenidos en su genoma están contenidos en la línea germinal.
Patentes similares o relacionadas:
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Estimulación de la vía wnt en la reprogramación de células somáticas, del 20 de Mayo de 2020, de WHITEHEAD INSTITUTE FOR BIOMEDICAL RESEARCH: Un método de reprogramación de una célula somática de mamífero, que comprende: (a) poner en contacto la célula somática de mamífero con un activador de la vía Wnt seleccionado […]
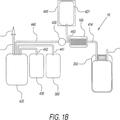 Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Ceramidasa y diferenciación celular, del 22 de Abril de 2020, de MOUNT SINAI SCHOOL OF MEDICINE: Un método in vitro para mejorar el fenotipo de una población de condrocitos, dicho método comprende: seleccionar una población de condrocitos de mamífero que […]
Medios de perfusión, del 1 de Abril de 2020, de Coherus Biosciences, Inc: Un método para la fabricación de una proteína que comprende la etapa de producir la proteína mediante el cultivo celular por perfusión de células […]
Andamios de biomatriz para la dispersión a escala industrial, del 11 de Marzo de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un metodo para producir un andamio de biomatriz a partir de tejido biologico seleccionado del grupo que comprende: pancreas, arbol biliar y duodeno para la […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en hepatocitos, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en hepatocitos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un medio […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en neuronas, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en neuronas, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un […]