PROCEDIMIENTO DE RESOLUCIÓN PARA EL ÁCIDO (R)-(-)-2-HIDROXI-2-(2-CLOROFENIL)ACÉTICO.
El procedimiento para la preparación de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético de la Fórmula (I) caracterizado porque el ácido 2-hidroxi-2-(2-clorofenil)acético racémico se resuelve con una amina sustituida de la fórmula general (II) - donde R 1 significa grupo hidroximetilo o grupo carbonilo,
R 2 significa grupo fenilo, grupo nitrofenilo o un grupo alquilo C1-C4 sustituido con un grupo amino, R 3 significa grupo hidroxilo o átomo de hidrógeno
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/HU2002/000054.
Solicitante: SANOFI-AVENTIS.
Nacionalidad solicitante: Francia.
Dirección: 174, AVENUE DE FRANCE 75013 PARIS FRANCIA.
Inventor/es: DOMBRADY, ZSOLT, GAJARY, ANTAL, CSATARINE NAGY, MARIANNA, FOGASSY, ELEMER, BALINT,Jozsef , SUBA,Charles.
Fecha de Publicación: .
Fecha Solicitud PCT: 14 de Junio de 2002.
Clasificación Internacional de Patentes:
- C07C215/36 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 215/00 Compuestos que contienen grupos amino e hidroxi unidos a la misma estructura carbonada. › Ari-1 amino-2 propanodioles-1,3.
- C07C229/26 C07C […] › C07C 229/00 Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › con más de un grupo amino unido a la estructura carbonada, p. ej. lisina.
- C07C51/02 C07C […] › C07C 51/00 Preparación de ácidos carboxílicos o sus sales, haluros o anhídridos. › a partir de sales de ácidos carboxílicos.
- C07C51/41B
Clasificación PCT:
- C07C215/10 C07C 215/00 […] › con un grupo amino y al menos dos grupos hidroxi unidos a la estructura carbonada.
- C07C229/26 C07C 229/00 […] › con más de un grupo amino unido a la estructura carbonada, p. ej. lisina.
- C07C51/02 C07C 51/00 […] › a partir de sales de ácidos carboxílicos.
- C07C51/41 C07C 51/00 […] › Preparación de sales de ácidos carboxílicos por conversión de estos ácidos o sus sales en sales que tienen la misma parte de ácido carboxílico (preparación de jabones C11D).
Clasificación antigua:
- C07C215/10 C07C 215/00 […] › con un grupo amino y al menos dos grupos hidroxi unidos a la estructura carbonada.
- C07C229/26 C07C 229/00 […] › con más de un grupo amino unido a la estructura carbonada, p. ej. lisina.
- C07C51/02 C07C 51/00 […] › a partir de sales de ácidos carboxílicos.
- C07C51/41 C07C 51/00 […] › Preparación de sales de ácidos carboxílicos por conversión de estos ácidos o sus sales en sales que tienen la misma parte de ácido carboxílico (preparación de jabones C11D).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
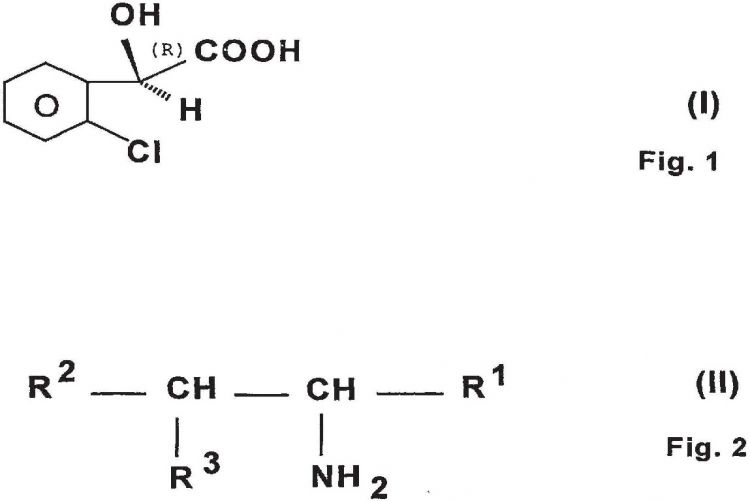
Fragmento de la descripción:
El objeto de la presente invención es un nuevo procedimiento de resolución del ácido 2-hidroxi-2-(2clorofenil)-acético racémico que hace posible la preparación de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético de la fórmula (I).
El compuesto ópticamente activo de la fórmula (I) es uno de los materiales de partida del conocido compuesto antiagregante de trombocito ópticamente activo clopidogrel (Plavix®) (documento WO-99/18110).
El ácido 2-hidroxi-2-(2-clorofenil)acético racémico puede obtenerse mediante diferentes procedimientos /Chem. Ber. 37 S. 3173 (1904), J. Am. Chem. Soc. 55 p 2593 (1933), Chem. Ber. 92 S 1739 (1959)/. Se conocen diversos procedimientos para la preparación del compuesto ópticamente activo de la fórmula (I) a partir de la literatura (Chirality 7 (8) p 652-76 (1995), Bull. Soc. Chim. Fr. (1973) 12, Pt 2, 3330), aunque tienen desventajas desde el punto de vista industrial porque o usan agentes de resolución caros (alcaloides) o aplicaban procedimientos microbiológicos que necesitan grandes volúmenes y su productividad es baja. (documentos EP-A-610048, EP-A449648, EP-A-527553). J. of Med. Chemistry 17 (1) p 34-41 (1974) describe la posibilidad de resolución del ácido 2hidroxi-2-(2-clorofenil)-acético mediante efedrina. Se tenía la intención de encontrar un procedimiento químico más ventajoso que los conocidos que de un procedimiento técnicamente más sencillo y barato para la preparación del compuesto de fórmula (I).
Inesperadamente se encontró que los compuestos de la fórmula general (II) forman una sal pobremente soluble con solo un enantiómero o ácido 2-hidroxi-2-(2-clorofenil)acético racémico, y así uno de los enantiómeros puede eliminarse de forma selectiva de la mezcla de reacción del procedimiento de resolución.
Según la invención, el compuesto de la fórmula (I) se da a partir de su sal diastereomérica sólida formada con un compuesto de la fórmula general (II) o se da a partir de las aguas madres del procedimiento de resolución y opcionalmente su pureza óptica se aumenta por recristalización selectiva.
El procedimiento según la invención puede llevarse a cabo preferiblemente en un disolvente orgánico, por ejemplo en metanol o una mezcla de agua y un disolvente orgánico, por ejemplo en una mezcla de agua - acetato de etilo o agua - metanol o acetato de isopropilo -metanol - agua.
Como un compuesto de la fórmula general (II), son aplicables lo más preferiblemente el (1S,2S)-(+)-1-fenil2-amino-1,3-propanodiol, (1R,2r)-treo-(-)-1-(4-nitrofenil)-2-amino-1,3-propanodiol o la L-(+)-lisina. /Núm. Cat. de Aldrich. L-(+)-lisina: 16971-4 (2000-1); (1S, 2S)-(+)-1-fenil-2-amino-1,3-propanodiol: 18654-6(2000-1); (1R, 2R)-treo(-)-1-(4-nitrofenil)-2-amino-1,3-propanodiol: A 7070-4 (2000-1)/.
Los compuestos de la fórmula general (II) se usan generalmente en una relación equimolar considerada al ácido racémico.
El procedimiento de resolución se lleva a cabo preferiblemente entre 10ºC y 30ºC. La pureza óptica del compuesto en bruto de la fórmula (I) así obtenido es 84-98%. El compuesto de la fórmula (I) en casi el 100% de pureza óptica puede recibirse por una recristalización del compuesto en bruto de la fórmula (I) a 40-100ºC usando tolueno o acetato de isopropilo como disolvente. El disolvente se usa entre 1,5-10 unidades volumétricas, preferiblemente 6-8 unidades volumétricas dependiendo de una unidad de masa del compuesto a recristalizar.
Otro objeto de la presente invención son sales del compuesto de la fórmula (I) formadas con compuestos de la fórmula general (II).
La eficacia de este procedimiento inventado se aumenta por la descomposición de la sal diastereomérica formada a partir del ácido (S)-(+)-2-hidroxi-2-(2-clorofenil)acético y de un compuesto de la fórmula general (I), el (S)(+)-isómero se racemiza y se resuelve de nuevo según la presente invención.
El procedimiento de racemización es un objeto adicional de la presente invención.
Así, el compuesto racémico de partida puede transformarse en el enantiómero deseado casi en toda la extensión.
La racemización puede llevarse a cabo en presencia de una base, preferiblemente puede usarse hidróxido sódico o hidróxido de potasio acuoso. El uso de una pequeña cantidad de disolvente aprótico en el medio acuoso acelera el procedimiento de racemización. Los disolventes apróticos preferidos son dimetilsulfóxido, sulfolano, dimetilformamida, hexametilfosfotriamida o la N-metil-pirrolidona. La racemización se hace preferiblemente al punto de ebullición de la mezcla de reacción en presencia de 0,1 - 0,5 unidades volumétricas de disolvente aprótico.
Más detalles de la presente invención se muestran en los siguientes ejemplos, sin limitar las reivindicaciones a su contenido.
Ejemplo 1
Resolución de ácido 2-hidroxi-2-(2-clorofenil)-acético racémico mediante (1S,2S)-(+)-1-fenil-2-amino-1,3propanodiol
(El compuesto de la fórmula general (II) - en donde R1 es un grupo hidroximetilo, R2 es un grupo fenilo, R3 es un grupo hidroxi)
Se disolvió ácido 2-hidroxi-2-(2-clorofenil)acético racémico (20,0 g, 107 mmoles) en 60 cm3 de acetato de etilo saturado con agua y se añadió al mismo (1S,2S)-(+)-1-fenil-2-amino-1,3-propanodiol (18,0 g, 107,5 mmoles), y después la mezcla se sembró mediante una sal formada a partir de (S)-(+)-2-hidroxi-2-(2-clorofenil)acetato y (1S,2S)-(+)-1-fenil 2-amino-1,3-propanodiol a temperatura ambiente.
La mezcla se agitó durante 3 horas a temperatura ambiente, la sustancia precipitada se filtró y se lavó con acetato de etilo y se secó: se recibieron 30,7 g de sustancia cristalina blanca. Esta sustancia se disolvió en una mezcla de 50 cm3 de agua y 15 cm3 de ácido clorhídrico al 37% y se extrajo con metil-terc-butil-éter. El extracto se secó en sulfato sódico y el disolvente se evaporó: se obtuvieron 15,3 g de mezcla enantiomérica rica en ácido (S)(+)-2-hidroxi-2-(2-clorofenil)acético ([α]D20 = +38º (c = 4, alcohol metílico/, la pureza óptica es 24%) que se puede racemizar según el Ejemplo 4 y reciclarse en el procedimiento.
Las aguas madres obtenidas de la resolución se concentraron, disolvieron en la mezcla de 15 cm3 de agua y 4,0 cm3 de ácido clorhídrico al 37% y se extrajeron con metil-terc-butil-éter. Los extractos combinados se secaron en sulfato sódico y se concentraron: se obtuvieron 4,3 g de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético ([α]D20 = 132,2º (c = 4, alcohol metílico) con pureza óptica de 84,2%. Este producto se recristalizó a partir de tolueno, se filtró a 60ºC, se lavó con tolueno. Después de secar se obtuvieron 3,62 g (19,4 mmoles, 18,1%) de ácido R-(-)-2-hidroxi2-(2-clorofenil)acético ([α]D20 =-157º (c = 4, alcohol metílico).
Ejemplo 2
Resolución de ácido 2-hidroxi-2-(2-clorofenil)acético racémico mediante (1R,2R)-(-)-treo-1-(4-nitrofenil)-2amino-1,3-propanodiol) (compuesto de la fórmula general (II) en donde R1 es un grupo hidroximetilo, R2 es un grupo p-nitrofenilo, R3 es un grupo hidroxi)
Se disolvió ácido 2-hidroxi-2-(2-clorofenil)acético racémico (20,0 g, 107 mmoles) en una mezcla de 120 g de acetato de isopropilo, 16 cm3 de metanol y 2 cm3 de agua.
Se añadieron 22,8 g (107 mmoles) de (1R,2R)-(-)-treo-1-(4-nitrofenil)-2-amino-1,3-propanodiol al mismo durante el ligero calentamiento para ayudar a la disolución. A temperatura ambiente la mezcla se sembró con sal de (1R,2R)-(-)-treo-1-(4-nitrofenil)-2-amino-1,3-propanodiol formado con ácido R-(-)-2-hidroxi-2-(2-clorofenil)acético. La mezcla de reacción se agitó durante 3 horas a temperatura ambiente y la sustancia precipitada se filtró, se lavó y se secó, se obtuvieron 13,6 g de sustancia cristalina, que es la sal del diol anterior y el ácido (R)-(-)-2-hidroxi-2-(2clorofenil)acético.
Esta sal se disolvió en 20 cm3 de agua y la disolución se aciduló mediante 5,7 cm3 de ácido clorhídrico concentrado y se extrajo con metil-terc-butil-éter, los extractos se combinaron, se secaron, se concentraron y se obtuvieron 5,84 g (31,3 mmoles) de ácido (R)-(-)-2-hidroxi-(2-clorofenil)acético en bruto ([α]D20 = -151º (c = 4, alcohol metílico), su pureza óptica es 96%.
Este ácido en bruto se recristalizó a partir de 41 cm3 de tolueno a 60ºC y el producto se secó. El peso de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético es 5,6 g (30,0 mmoles). El rendimiento es 28%. ([α]D20...
Reivindicaciones:
1. El procedimiento para la preparación de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético de la Fórmula (I)
**(Ver fórmula)**
5 caracterizado porque el ácido 2-hidroxi-2-(2-clorofenil)acético racémico se resuelve con una amina sustituida de la fórmula general (II) - donde R1 significa grupo hidroximetilo o grupo carbonilo, R2 significa grupo fenilo, grupo nitrofenilo o un grupo alquilo C1-C4 sustituido con un grupo amino, R3 significa grupo hidroxilo o átomo de hidrógeno.
2. El procedimiento según la reivindicación 1, caracterizado porque el (1S,2S)-(+)-1-fenil-2-amino-1,310 propanodiol cubierto por la fórmula general (II) se usa como agente de resolución.
3. El procedimiento según la reivindicación 1, caracterizado porque el (1R,2R)-treo-(-)-1-(4-nitrofenil)-2amino-1,3-propanodiol cubierto por la fórmula general (II) se usa como agente de resolución.
4. El procedimiento según la reivindicación 1, caracterizada porque la L-(+)-lisina cubierta por la fórmula general (II) se usa como agente de resolución.
7. El procedimiento según la reivindicación 6, caracterizado porque la cristalización selectiva se lleva a cabo en tolueno o en acetato de isopropilo. 8. El procedimiento según la reivindicación 6, caracterizado porque el compuesto de alta pureza óptica de 25 la fórmula (I) obtenido por cristalización selectiva se separa del disolvente a una temperatura entre +40º y +100 ºC. 9. El procedimiento según la reivindicación 1, caracterizado porque el ácido (S)-(+)-2-hidroxi-2-(2clorofenil)acético obtenido por resolución se racemiza y después de devuelve al procedimiento de resolución. 10. El procedimiento según la reivindicación 9, caracterizado porque la racemización se lleva a cabo con un hidróxido de metal alcalino, ventajosamente con hidróxido sódico. 30 11. El procedimiento según la reivindicación 9, caracterizado porque la racemización se lleva a cabo en agua en presencia de una pequeña cantidad de disolvente aprótico, ventajosamente en presencia de dimetilsulfóxido, sulfolano, dimetilformamida, triamida de ácido hexametilfosfórico o N-metil-pirrolidona. 12. Sal de (1S,2S)-(+)-1-fenil-2-amino-1,3-propanodiol de ácido (S)-(+)-2-hidroxi-2-(2-clorofenil)acético. 13. Sal de (1R,2R)-(-)-treo-1-(4-nitrofenil)-2-amino-1,3-propanodiol de ácido (R)-(-)-2-hidroxi-2-(235 clorofenil)acético. 14. Sal de ácido (R)-(-)-2-hidroxi-2-(2-clorofenil)acético-L-(+)-lisina. 15 5. El procedimiento según la reivindicación 1, caracterizada porque la sal del ácido 2-hidroxi-2-(2clorofenil)acético racémico y un compuesto de la fórmula general (II) - donde el significado de R1, R2 o R3 es como se da anteriormente - se forma en un disolvente inorgánico o en la mezcla de agua y uno o más disolventes orgánicos, y la sal separada debido a su diferente solubilidad del par de sales diastereoméricas se obtiene de la mezcla de reacción y el compuesto de la fórmula (I) se obtiene de la sal o de la lejía madre de la resolución.
20 6. El procedimiento según la reivindicación 1, caracterizado porque la pureza óptica del compuesto en bruto de la fórmula (I) obtenido por resolución se aumenta por cristalización selectiva.
Patentes similares o relacionadas:
Fenilacetato de L-ornitina y métodos de elaboración del mismo, del 1 de Abril de 2020, de Ocera Therapeutics, Inc: Una composición que comprende una forma cristalina de fenilacetato de L-ornitina, en donde dicha forma cristalina muestra un patrón de difracción de rayos […]
Métodos de fabricación de fenilacetato de L-ornitina, del 13 de Marzo de 2019, de Ocera Therapeutics, Inc: Un proceso de fabricación de sal de fenilacetato de L-ornitina que comprende: preparar una solución de sal de fenilacetato mezclando un ácido fenil acético y una base […]
Reactivos de transfección que contienen amina y métodos para prepararlos y usarlos, del 28 de Febrero de 2019, de LIFE TECHNOLOGIES CORPORATION: Compuesto 87 o sus sales farmacéuticamente aceptables:**Fórmula**
Sal de lisina de ácido 15-hidroxi-8(Z),11(Z),13(E)-eicosatrienoico, del 27 de Febrero de 2019, de DS Biopharma Limited: Una sal de lisina de ácido 15-hidroxi-8(Z),11(Z),13(E)-eicosatrienoico (15-HETrE).
Procedimiento de preparación de una sal de ácido acetilsalicílico y de un aminoácido básico, del 19 de Noviembre de 2018, de Unither Pharmaceuticals: Procedimiento de preparación de una sal de ácido acetilsalicílico y de un aminoácido básico, que comprende la mezcla en un reactor de una solución de […]
Fase cristalina de (3S,3S'') 4,4''-disulfanodiilbis(ácido 3-aminobutano 1-sulfónico) con L-lisina, del 3 de Enero de 2018, de Quantum Genomics: Una forma cristalina de (3S,3S') 4,4'-disulfanodiilbis (ácido 3-aminobutano 1-sulfónico) con L-lisina ABSD.
Fenilacetato de l-ornitina y métodos para elaborar el mismo, del 27 de Septiembre de 2017, de Ocera Therapeutics, Inc: Una composición que comprende una forma cristalina de fenilacetato de L-ornitina, donde dicha forma cristalina exhibe un patrón de difracción en polvo de rayos-X que […]
Derivados deuterados de catecolamina y medicamentos que comprenden dichos compuestos, del 18 de Mayo de 2016, de RATIOPHARM GMBH: Ácido L-2-amino-2,3-dideutero-3-(3,4-dihidroxifenil)propiónico y sus estereoisómeros, enantiómeros o diastereómeros en forma ópticamente pura así como sus […]