PROTEÍNA QUIMÉRICA.
Una proteína quimérica que comprende: 1) un primer polipéptido que posee actividad de modificación de la matriz por separación de componentes de la matriz extracelular que inhiben el crecimiento y desarrollo neuronal y que se selecciona de enzimas de digestión de la matriz;
y 2) un segundo polipéptido que posee actividad de factor neurotrófico para células neurales, no presentándose conjuntamente en la naturaleza dicho primer y segundo polipéptido y estando unidos conjuntamente en dicha proteína quimérica.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/026214.
Solicitante: ACORDA THERAPEUTICS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 15 SKYLINE DRIVE HAWTHORNE, NY 10532 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GRUSKIN, ELLIOTT, A., GARGI,Roy, CHOJNICKI,Eric,Theodore.
Fecha de Publicación: .
Fecha Solicitud PCT: 14 de Agosto de 2003.
Clasificación PCT:
- C12P21/06 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
Clasificación antigua:
- C12P21/06 C12P 21/00 […] › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2366333_T3.pdf
Fragmento de la descripción:
ANTECEDENTES
Campo Técnico La presente publicación se refiere a una proteína quimérica que contiene al menos dos dominios funcionales. La proteína se codifica por un gen recombinante que contiene, al menos, un dominio que codifica un primer polipéptido que posee actividad de modificación de matriz por separación de componentes de la matriz extracelular que inhiben el crecimiento y desarrollo neuronal y que se selecciona de enzimas de digestión de la matriz, y al menos otro dominio que codifica un segundo polipéptido que posee actividad de factor neurotrófico en células neuronales. Los compuestos de esta publicación se pueden usar para favorecer la reparación de daño neuronal causado por enfermedad o trauma físico.
Descripción de la Técnica Relacionada
La capacidad de las neuronas para extender las neuritas es de importancia fundamental en el establecimiento de conexiones neuronales durante el desarrollo. Se requiere también durante la regeneración para restablecer conexiones destruidas como resultado de una lesión.
Un área que se ha determinado que es de importancia en la reparación y regeneración de tejido celular, incluyendo tejido neural, es la matriz extracelular. Durante aproximadamente las dos últimas décadas, el conocimiento básico de la adhesión y migración celular en matrices extracelulares (ECMs) a nivel molecular se ha extendido rápidamente. La acción de enzimas y otros polipéptidos que degradan componentes de la matriz extracelular y membranas basales puede facilitar los casos de reparación neural por una variedad de mecanismos que incluyen la liberación de citoquinas unidas y aumentando la permeabilidad de la matriz, aumentando con ello la movilidad de moléculas mediadoras, factores de crecimiento y agentes quimiotácticos, así como las células implicadas en el proceso de curación. Por ejemplo, la patente de U.S. No. 5.997.863 describe el uso de glicosaminoglicanos para manipular la proliferación celular y estimular la cicatrización de heridas. Aunque se pueden usar proteínas, especialmente enzimas, para separar los componentes de la matriz extracelular inhibidores de la regeneración, su uso solamente puede no ser suficiente para llevar a cabo la reparación de un sistema nervioso dañado.
Un número de moléculas y de regiones específicas de ellas se han implicado en la capacidad para favorecer el brote de neuritas de una célula neuronal, un proceso llamado también brote neurítico. Este proceso es fundamental en el desarrollo y regeneración neural, especialmente después de que el daño físico o enfermedad ha dañado las células neuronales. Las neuritas se alargan profusamente durante el desarrollo del sistema nervioso central y periférico de todas las especies animales (Cajal, Degeneración y regeneración en el sistema nervioso, Oxford University Press, London (1928)). Este fenómeno corresponde a los axones y dendritas. Sin embargo, en adultos, el rebrote de axones y dendritas en el sistema nervioso central se pierde cada vez más con el progreso evolutivo. Se sabe que diversos polipéptidos, especialmente moléculas de adhesión celular (CAMs), favorecen el crecimiento de células neurales. Aunque los primeros esfuerzos en este área de investigación se concentraron sobre la fibronectina (FN), proteína de matriz extracelular favorecedora de la adhesión, se ha descubierto también que otros péptidos favorecen el crecimiento neural. Por ejemplo, la patente de U.S. No. 5.792.743 describe nuevos polipéptidos y métodos para favorecer el crecimiento neural en el sistema nervioso central de un mamífero administrando una molécula soluble de adhesión celular neural, un fragmento suyo, o un producto de fusión-Fc suyo. La patente de U.S. No. 6.313.265 describe polipéptidos sintéticos que contienen las regiones farmacológicamente activas de CAMs que se pueden usar para favorecer la reparación y regeneración nerviosa tanto en daños de nervios periféricos como lesiones del sistema nervioso central (CNS).
Aunque útiles, el uso de proteínas regeneradoras solamente puede no ser suficiente para llevar a cabo la reparación 45 de un sistema nervioso dañado.
Las proteínas quiméricas se conocen en la técnica como proteínas derivadas de fuentes genéticamente diferentes. Se sintetizan normalmente usando técnicas de DNA recombinante. Por ejemplo, la patente de U.S. No. 6.326.166 describe proteínas quiméricas de unión a DNA y métodos para su fabricación y uso, y la patente de U.S. No.
6.248.562 describe proteínas quiméricas que contienen polipéptidos antigénicos derivados de cepas de Borrelia que causan la enfermedad de Lyme.
El documento WO 95/13091 describe una proteína quimérica que comprende actividad enzimática que altera la ECM y un resto de unión a la ECM.
El documento EP 0704532 describe una proteína quimérica que tiene un polipéptido modificador de la matriz y un factor regulador celular glicoproteico.
SUMARIO
De acuerdo con la presente publicación, se describe una proteína quimérica que contiene al menos dos dominios funcionales. Los dominios funcionales codifican polipéptidos que no se encuentran conjuntamente en la naturaleza, pero ambos favorecen la regeneración y reparación de tejido neural dañado.
En una realización, el primer dominio funcional es para un polipéptido, que es una enzima de digestión de la matriz, que posee actividad de modificación de la matriz por separación de componentes de la matriz extracelular que inhiben el crecimiento y desarrollo neural. El segundo dominio funcional es para un polipéptido que se sabe que posee actividad de factor neurotrófico para las células.
La publicación se extiende a métodos de favorecer y aumentar la regeneración neural in vivo utilizando proteínas quiméricas que combinan dos o más dominios que codifican para dos o más polipéptidos terapéuticos, y a composiciones farmacéuticas que se pueden usar para alcanzar los objetivos de tales métodos. Más específicamente, las proteínas quiméricas de la presente publicación se pueden formular en una composición que se puede liberar en un sitio neural, como por administración parenteral.
El término “Chasa” o “CHasa” cuando se usa en el presente documento es una abreviatura de “condroitinasa”.
BREVE DESCRIPCION DE LAS FIGURAS
La Fig. 1 es un gel de agarosa que representa el fragmento clonado de Chasa AC de Flavobacterium Heparinum. La Fig. 2 muestra la expresión de condroitinasa AC en el vector Pet 15b. La Fig. 3 muestra la expresión proteica de Chasa AC. La Fig. 4 es un gel zimográfico que muestra la actividad de Chasa AC recombionante. La Fig. 5 es un gel de agarosa que representa el fragmento clonado de Chasa B de Flavobacterium Heparinum. La Fig. 6 muestra la expresión de condroitinasa B en el vector Pet 15b. La Fig. 7 muestra la purificación de Chasa B usando columna de Ni-NTA y pasada sobre gel de SDS-PAGE al 10%. La Fig. 8 es un gel zimográfico que muestra la actividad de Chasa B recombinante. La Fig. 9 es un gel de agarosa que representa el fragmento clonado de Chasa ABC de Proteus Vulgaris. La Fig. 10 es un gel de agarosa que representa la expresión de condroitinasa AC en PCDNA4HisMax, un vector de
expresión en mamíferos.
La Fig. 11 indica la técnica de transferencia de Western que muestra extractos de células transfectadas CHO-K con Chasa AC. La Fig. 12 es un gel de agarosa que representa la expresión de condroitinasa B en PCDNA4HisMax, un vector de
expresión en mamíferos.
La Fig. 13 indica la técnica de transferencia de Western que muestra extractos de células transfectadas CHO-K con Chasa B. La Fig. 14 representa un gel proteico de proteína L1-Fc humana purificada. La Fig. 15 indica los resultados de un ensayo de brote que muestra actividad de L1-Fc humana favoreciendo brote
neurítico.
DESCRIPCION DETALLADA DE LAS REALIZACIONES PREFERIDAS
La presente publicación se refiere a proteínas quiméricas que combinan polipéptidos que no se encuentran conjuntamente en la naturaleza. Las proteínas quiméricas son una combinación de uno o más polipéptidos capaces de modificar la matriz extracelular como se ha descrito anteriormente, con al menos otro polipéptido que posee actividad de factor neurotrófico para células neurales.
Cuando se usan en el presente documento, los términos “proteína”, “polipéptido”, y “péptido” se usan de modo... [Seguir leyendo]
Reivindicaciones:
1. Una proteína quimérica que comprende:
1) un primer polipéptido que posee actividad de modificación de la matriz por separación de componentes de la
matriz extracelular que inhiben el crecimiento y desarrollo neuronal y que se selecciona de enzimas de digestión
de la matriz; y
2) un segundo polipéptido que posee actividad de factor neurotrófico para células neurales,
no presentándose conjuntamente en la naturaleza dicho primer y segundo polipéptido y estando unidos conjuntamente en dicha proteína quimérica.
2. La proteína quimérica de la reivindicación 1 donde el primer polipéptido se selecciona del grupo consistente en condroitinasas, hialuronidasas, y metaloproteinasas de matriz.
3. La proteína quimérica de la reivindicación 2 donde la condroitinasa se selecciona del grupo consistente en condroitinasa ABC exoliasa, condroitinasa ABC endoliasa, condroitinasa AC, y condroitinasa B.
4. La proteína quimérica de la reivindicación 2 donde la condroitinasa se selecciona del grupo consistente en condroitinasa ABC I, condroitinasa ABC II, condroitinasa AC, y condroitinasa B.
5. La proteína quimérica de la reivindicación 4 donde la condroitinasa es condroitinasa ABC I.
6. La proteína quimérica de la reivindicación 2 donde la metaloproteinasa de matriz se selecciona del grupo consistente en MMP-9, MMP-2, y pepsina.
7. La proteína quimérica de la reivindicación 1 donde el segundo polipéptido que posee actividad de factor neurotrófico se selecciona del grupo consistente en NGF, BDNF, NT-3, IGF, EGF, VEGF, FGF, PDGF, y TGF y .
8. La proteína quimérica de una cualquiera de las reivindicaciones precedentes donde el primer polipéptido está unido al segundo polipéptido por una ligadura peptídica.
9. La proteína quimérica de la reivindicación 8 donde la ligadura peptídica es una parte Fc de una inmunoglobulina.
10. Una composición farmacéutica que comprende una proteína quimérica, como se reivindica en una cualquiera de las reivindicaciones precedentes, en combinación con un vehículo farmacéuticamente aceptable.
11. La proteína quimérica de una cualquiera de las reivindicaciones 1 a 9 para usar en terapia.
12. Uso de la proteína quimérica de una cualquiera de las reivindicaciones 1 a 9 para la fabricación de un medicamento para aumentar la reparación y regeneración del sistema nervioso mediante la administración de la proteína quimérica a células dañadas del sistema nervioso.
Patentes similares o relacionadas:
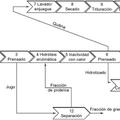 Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
 Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Uso de tripeptidil peptidasas tolerantes a la prolina en composiciones de aditivo para piensos, del 26 de Febrero de 2020, de Dupont Nutrition Biosciences ApS: Un método para preparar una composición de aditivo para piensos que comprende: mezclar al menos una tripeptidil peptidasa tolerante a la prolina que tiene […]
Enzimas específicas de sitio y métodos de uso, del 19 de Febrero de 2020, de Poseida Therapeutics, Inc: Un polipéptido que comprende al menos una secuencia de aminoácidos que tiene la secuencia de LSTEQVVAIASX1X2GGKQALEAVKAQLLVLRAAPYE (SEQ ID NO: 1), en donde […]
Composiciones para unir módulos de dedos de cinc, del 15 de Enero de 2020, de Sangamo Therapeutics, Inc: Una proteína de dedos de cinc de múltiples dedos que se une específicamente a un sitio diana, comprendiendo la proteína de dedos de cinc de […]
Concentrado de proteínas de granos que contienen almidón: composición, método de fabricación y usos del mismo, del 1 de Enero de 2020, de THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF AGRICULTURE: Un proceso para producir un concentrado de proteinas a partir de un grano o semilla oleaginosa que contiene almidon, el proceso comprende: (i) moler el […]
 Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
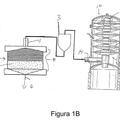 Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]
Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]