MÉTODOS Y COMPOSICIONES PARA REDUCIR LA NEURODEGENERACIÓN EN ESCLEROSIS LATERAL AMIOTRÓFICA.
Una composición que comprende una solución acuosa transparente que comprende:
(a) un primer material seleccionado entre ácido ursodesoxicólico o una sal sódica del ácido ursodesoxicólico (UDCA); (b) un carbohidrato seleccionado entre el grupo compuesto por un producto soluble acuoso de la conversión del almidón o un polisacárido soluble acuoso no de almidón; (c) agua, donde el primer material y el carbohidrato ambos permanecen en solución para cualquier subconjunto del intervalo de valores de pH obtenibles en un sistema acuoso suficiente para que una formulación farmacéutica permanezca en solución desde la preparación, hasta la administración, y hasta la absorción en el cuerpo; para su uso en el tratamiento de al menos un síntoma de la esclerosis lateral amiotrófica
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/039089.
Solicitante: YOO, SEO HONG.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 537 SPENCER DRIVE WYCKOFF, NEW JERSEY 07481 ESTADOS UNIDOS DE AMERICA.
Inventor/es: YOO, SEO HONG.
Fecha de Publicación: .
Fecha Solicitud PCT: 31 de Octubre de 2005.
Clasificación PCT:
- A61K31/575 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › sustituidos en posición 17 beta por una cadena de al menos tres átomos de carbono, p. ej. colano, colestano, ergosterol, sitosterol.
- A61K47/36 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61P25/16 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Medicamentos contra el Parkinson.
- A61P25/28 A61P 25/00 […] › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2358089_T3.pdf




Fragmento de la descripción:
La presente descripción se refiere a composiciones y métodos para mejorar o tratar al menos un síntoma de un proceso o enfermedad neurodegenerativa.
En cualquier momento dado, tantos como 30.000 americanos padecen esclerosis lateral amiotrófica (ALS), que casi siempre es fatal. La ALS, también conocida como enfermedad de Lou Gehrig, es una enfermedad neurodegenerativa progresiva que ataca a las neuronas motoras del cerebro y la médula espinal y provoca debilidad y atrofia muscular. Los síntomas tempranos incluyen pérdida de destreza y el modo de andar. Según progresa la enfermedad, los pacientes llegan a quedar paralizados y requieren asistencia para respirar. La esperanza de vida de pacientes con ALS habitualmente es de 3 a 5 años después del diagnóstico siendo la causa principal de muerta la pérdida de función respiratoria.
La etiología de la ALS está sólo parcialmente comprendida. Los casos familiares (hereditarios) componente sólo aproximadamente el 5-10% de todos los pacientes con ALS. Dentro de este subconjunto de pacientes con ALS, uno de cada cinco porta el único defecto genético identificado hasta la fecha, una mutación en el gen SODI. El alelo mutante conduce a la producción de una proteína que se cree que es tóxica para las neuronas motoras. La mayoría de los casos, es decir, el 90-95% restante, surge aparentemente de forma espontánea y sin un patrón identificable. Por tanto, parece que la ALS es capaz de atacar a cualquiera en cualquier momento. Las terapias eficaces son escasas o inexistentes.
El lector puede informarse adicionalmente en cuando al estado de la técnica por referencia a los siguientes documentos: WO 01/56547 A (YOO, SEO, HONG) 9 de agosto de 2001 (09-08-2001), WO 00/04875 A (YOO, SEO, HONG) 3 de febrero de 2000 (03-02-2000), WO 2004/012686 A (NITROMED, INC; GARVEY, DAVID, S; IYENGAR, RADHA) 12 de febrero de 2004 (12-02-2004), KEENE C DIRK ET AL: "A bile acid protects against motor and cognitive deficits and reduces striatal degeneration in the 3-nitropropionic acid model of Huntington's disease" EXPERIMENTAL NEUROLOGY, vol. 171, nº 2, octubre de 2001 (10-2001), páginas 351-360, XP0023750471SSN: 0014-4886, RODRIGUES CECILIA M P ET AL: "Bilirubin and amiloid-beta peptide induce cytochrome c release through mitochondrial membrane permeabilization" MOLECULAR MEDICINE (NEW YORK), vol. 6, nº 11, noviembre de 2000 (200011), páginas 936-946, XP009064467 ISSN: 1076-1551. Puede encontrarse un análisis detallada de la importancia de estas descripciones en el archivo de seguimiento.
Por consiguiente, la presente invención proporciona una composición que comprende una solución acuosa se caracterizan en las reivindicaciones dependientes.
En realizaciones que contienen tanto polisacárido soluble no de almidón como producto de conversión del almidón de elevado peso molecular, las cantidades de cada uno son tales que cuando se combinan juntos en la composición, son suficientes para permitir que el componente UDCA, el producto de conversión del almidón de elevado peso molecular, el polisacárido soluble no de almidón y el compuesto farmacéutico, si lo hay, permanezcan en solución a cualquier pH dentro de un intervalo de pH seleccionado.
En algunas realizaciones de la descripción, se proporciona una composición de terapia de combinación que puede aumentar la intensidad de respuesta a o la eficacia de un agente farmacéutico. Más específicamente, la administración de una composición de la descripción que comprende un UDCA y riluzol a un sujeto que padece un trastorno neurodegenerativo puede tener más de un efecto aditivo de la administración de cada compuesto solo.
Algunas realizaciones ejemplares específicas de la descripción pueden comprenderse por referencia, en parte, a la siguiente descripción y los dibujos adjuntos, en los que:
la FIGURA 1A es la esperanza de vida y su resultado se muestra como el porcentaje de supervivencia en el tiempo cuando el animal muere;
la FIGURA 1B es un ensayo de rotarod (rodillo giratorio) y su resultado se muestra como el tiempo que permanecieron sobre el rodillo antes de caerse todas las semanas hasta la muerte;
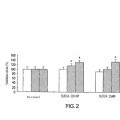
la FIGURA 2 es una gráfico de barras que muestra los resultados de un ensayo de viabilidad celular con células de tipo silvestre, células A4V, y células G93A en el que las células no se trataron (panel de la izquierda) o se incubaron con 200 nM de UDCA solubilizado en solución de la descripción (panel central), o 20 M de UDCA solubilizado en solución de la descripción (panel de la derecha);
la FIGURA 3 es un gráfico de barras que muestra los resultados de un ensayo de viabilidad celular con células de tipo silvestre, células A4V, y células G93A en el que las células no se trataron (panel de la izquierda) o se incubaron con S-nitrosoglutatión 500 M (GSNO; panel central), o GSNO 500 M seguido de una solución de UDCA 20 M de la descripción;
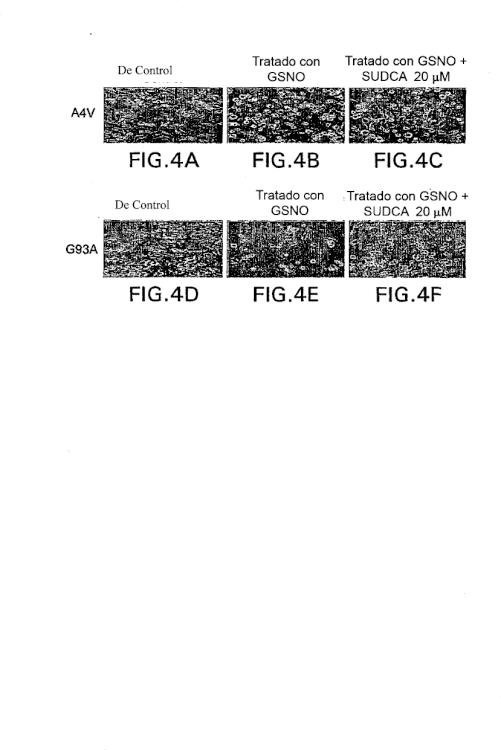
la FIGURA 4A es una micrografía que muestra células A4V no tratadas (células de control);
la FIGURA 4B es una micrografía que muestra células A4V incubadas con S-nitrosoglutatión 500 M (GSNO);
la FIGURA 4C es una micrografía que muestra células A4V incubadas con GSNO 500 M y después, incubadas en sucesión con 20 M de UDCA solubilizado en solución de la descripción;
la FIGURA 4D es una micrografía que muestra células G93A no tratadas;
la FIGURA 4E es una micrografía que muestra células G93A incubadas con GSNO 500 M; y
la FIGURA 4F es una micrografía que muestra células G93A incubadas con GSNO 500 M y después, incubadas en sucesión con 20 M de UDCA solubilizado en solución de la descripción.
Aproximadamente el 85-90% de los pacientes con ALS de aparición en el adulto no tienen historia familiar de la enfermedad. Esta incidencia aparentemente aleatoria o fortuita ha conducido a algunos facultativos a identificar estos casos como ALS esporádica (SALS). Por el contrario, la ALS puede heredarse como una afección dominante autonómica en aproximadamente el 10-15% de los pacientes. Estos casos se han identificado como ALS familiar (FALS). En aproximadamente un quinto de los casos de FALS, el gen mutante es una enzima citoplasmática, la Cu/Zn superóxido dismutasa-1 (SOD). Se han identificado más de 90 mutaciones en la Cu/Zn SOD y están extendidas a lo largo de más de 30 sitios. Estas mutaciones pueden dar lugar a una nueva función adversa que conduce a FALS en oposición a la simple alteración de una función normal del producto génico. Por ejemplo, en experimentos con ratones transgénicos que sobre-expresan una Cu/Zn SOD humana mutante (A4V, G93A, G85R, G37R), no había correlación entre las pérdidas de actividad de SODI y la aparición o gravedad de la enfermedad.
Los síntomas y la patología de pacientes con FALS con mutaciones en SODI se parecen mucho a los de pacientes con SALS. El progreso clínico y las alteraciones patológicas en las neuronas motoras de ratones que expresan SODI mutante también son sorprendentemente similares a las encontradas en pacientes con SALS, lo que sugiere que los mecanismos de neurodegeneración para SALS y FALS pueden compartir componentes comunes. Las mitocondrias desempeñan una tarea central en muchas vías metabólicas y apoptóticas que regulan la vida y la muerte de las células. Las mitocondrias también son el sitio de inicio de la cascada apoptótica intrínseca, que puede activarse por la liberación de factores pro-apoptóticos que pueden actuar de un modo dependiente de caspasa o independiente de caspasa. La disfunción mitocondrial puede estar directamente implicada en la patogénesis de la ALS.
La disfunción mitocondrial causa muerte de las neuronas motoras predisponiéndolas a excitotoxicidad mediada por calcio, aumentando la generación de especies de oxígeno reactivas, y/o iniciando la vía apoptótica intrínseca. La disfunción mitocondrial puede provocar liberaciones cuantales de factores pro-apoptóticos, tales como citocromo c, el factor inductor de la apoptosis (AIF), y endoG, desde mitocondrias individuales, quizá en respuesta a toxicidad mediada por calcio local, por ejemplo, en sinapsis de excitación. Esta toxicidad local podría inducir la muerte de compartimientos subcelulares, por ejemplo, las ramificaciones dendríticas o axonales. Este tipo de degeneración compartimental subcelular podría ser insuficiente para inducir que la célula muera inmediatamente, pero podría... [Seguir leyendo]
Reivindicaciones:
1. Una composición que comprende una solución acuosa transparente que comprende:
(a) un primer material seleccionado entre ácido ursodesoxicólico o una sal sódica del ácido ursodesoxicólico (UDCA);
(b) un carbohidrato seleccionado entre el grupo compuesto por un producto soluble acuoso de la conversión del almidón o un polisacárido soluble acuoso no de almidón;
(c) agua, donde el primer material y el carbohidrato ambos permanecen en solución para cualquier subconjunto del intervalo de valores de pH obtenibles en un sistema acuoso suficiente para que una formulación farmacéutica permanezca en solución desde la preparación, hasta la administración, y hasta la absorción en el cuerpo;
para su uso en el tratamiento de al menos un síntoma de la esclerosis lateral amiotrófica.
2. La composición de acuerdo con la reivindicación 1, en le que la esclerosis lateral amiotrófica es esclerosis lateral amiotrófica avanzada.
3. La composición de acuerdo con la reivindicación 1, en la que el síntoma se selecciona entre el grupo compuesto por duración de la vida acortada y parálisis.
4. La composición de acuerdo con la reivindicación 1, en la que el sujeto es un mamífero.
5. La composición de acuerdo con la reivindicación 1, en la que el sujeto es un ser humano.
6. La composición de acuerdo con la reivindicación 1, en la que el primer material está presente en una cantidad terapéuticamente activa.
7. La composición de acuerdo con la reivindicación 1, en la que el producto soluble acuoso de la conversión del almidón se selecciona entre el grupo compuesto por maltodextrina, dextrina, glucosa líquida, jarabe de maíz sólido, y almidón soluble.
8. La composición de acuerdo con la reivindicación 1, en la que el intervalo de pH seleccionado está entre aproximadamente 1 y aproximadamente 10 inclusive.
9. La composición de acuerdo con la reivindicación 1, en la que el producto soluble acuoso de la conversión del almidón es maltodextrina.
10. La composición de acuerdo con la reivindicación 1, en la que el polisacárido soluble acuoso no de almidón se seleccionan entre el grupo compuesto por dextrano, goma guar, pectina, fibra soluble no digerible.
11. La composición de acuerdo con una de las reivindicaciones precedentes que comprende adicionalmente:
(d) una cantidad farmacéuticamente eficaz de un compuesto farmacéutico seleccionado entre los siguientes:
el compuesto farmacéutico se selecciona entre el grupo compuesto por pasiniazida, benztiazida, prednisolona, mentol, mebhidrolina, naftalenosulfonato, triclormetiazida, oxitetraciclina, sulfato de arcaína, eritromicina, glutatión, trioxsaleno, nilhidrina HCl, desmetildiazepam, tonzilamina HCl, valproato Na, aminofenazona, sulfametizol, droperidol, 2tiouracilo, ácido quinurénico, ácido fusídico, leucovorina Ca, sulfato de esparteína, amigdalina, pramoxina HCl, furosemida, dinitolmida, budesonida, flopropiona, fluorometolona, anti-inflamatorio), N-formil-metionilfenilalanina, tiopental Na, lansoprazol, tosilato de bretilio, cefamandol Na, oxibendazol, cicloleucilglicina, dantroleno Na, tetroquinona, piperazina, esculina, etisterona, dimetadiona, griseofulvina, acetaminosalol, isoguvacina HCl, putrescina diHCl, emetina HCl, sulfanilamida, mimosina, acetilcolina, mesilato de pralidoxima, lisil-triptofanil-lisina, hecogenina, acetato de prednisolona, albendazol, hidroclorotiazida, demeclociclina HCl, nitrofurazona, dicloxacilina Na, alfa-tocoferol, tetraciclina HCl, fenofibrato, probenecid, tretinoína, acetaminofeno, hidrastinina HCl, acetato de d[-Arg-2]quiotorfina, NMDA, cefmetazol Na, ribavirina, bencil-L-serina, picrotoxina, oxetazina, sulfatiazol, triclormetina, nabumetona, cloranfenicol, riluzol, ginseng y su extracto, glicirricina y ácido glicirrícico, derivados de carboquinona, coenzima Q10, creatina, factor de crecimiento-1 tipo insulina, minociclina, mecamserina, xaliproden, gabapentina, dextrometorfano, talampanel, IL-1, TR500, procisteína, factor neurotrófico derivado de cerebro, baclofeno, tizanidina, benzodiazepinas, glicopirrolato, atropina, quinina, fenitoína y morfina
que disminuye la muerte de neuronas motoras, y donde el primer material, el carbohidrato, y la cantidad farmacéuticamente eficaz del compuesto farmacéutico permanecen todos en solución pata todos los valores de pH de la solución dentro de un intervalo seleccionado de valores de pH.
12. La composición de acuerdo con la reivindicación 11, en la que el primer material está presente en una cantidad neuroprotectora.
Patentes similares o relacionadas:
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Matrices de microagujas obtenidas mediante disolución y colada que contienen un principio activo, del 29 de Julio de 2020, de Corium, Inc: Un método para formar una matriz de microprotusiones, que comprende: (a) dispensar en un molde que tiene una matriz de cavidades correspondientes al negativo […]
Potenciador de la conservación, del 29 de Julio de 2020, de DSM IP ASSETS B.V.: Una composición tópica que comprende fitantriol y eritrulosa.
 Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Administración intravascular de composiciones de nanopartículas y usos de las mismas, del 29 de Julio de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden rapamicina y albúmina para su uso en un procedimiento para inhibir la remodelación […]
Reducción de tejido adiposo, del 22 de Julio de 2020, de Dobak, John, Daniel: Una formulacion farmaceutica inyectable que comprende: (i) polidocanol en una cantidad del 0,5 % p/v al 2,0 % p/v; e (ii) un alcohol C3-C6 en una cantidad del […]