MÉTODO PARA PURIFICACIÓN DE 225AC A PARTIR DE DIANAS MARCADAS CON 226RA IRRADIADAS.
Método para purificar 225Ac a partir de dianas de 226Ra irradiadas dispuestas sobre un soporte,
que comprende las siguientes etapas: 5 a) efectuar al menos un tratamiento de lixiviación de las dianas de 226Ra para lixiviar esencialmente la totalidad de 225Ac y 226Ra con ácido nítrico o clorhídrico en condiciones de reflujo; b) eliminar HCI si el disolvente en la etapa a) es ácido clorhídrico y disolver de nuevo el material resultante en ácido nítrico; 10 c) concentrar los extractos que contienen 225Ac y 226Ra; d) separar 225Ac de 226Ra y otros isótopos de Ra por medio de al menos una primera cromatografía de extracción con un material soporte sólido que tiene un primer sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general I en al menos un compuesto de acuerdo con la fórmula general II, **(Ver fórmula)**Fórmula I **(Ver fórmula)**Fórmula II en donde en la fórmula I: R1, R2 son independientemente octilo, n-octilo, fenilo o fenilo sustituido con alquilo de C1 a C3; R3, R4 son independientemente propilo, isopropilo, butilo o isobutilo; en donde en la fórmula II: R5, R6 y R7 son independientemente alquilo de C2 -C5, en particular, butilo o isobutilo; e) eluir 225Ac que es retenido en el soporte sólido de la fase estacionaria con ácido nítrico o clorhídrico, mientras se hace pasar a su través 226Ra; 10 f) separar 225Ac de 210Po y 210Pb por medio de al menos una segunda cromatografía de extracción con un material soporte sólido que tiene un segundo sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general III en al menos un compuesto de la fórmula general IV, **(Ver fórmula)**Fórmula III R10 ºº OH Fórmula IV en donde en la fórmula III: R8 y R9 son independientemente H, alquilo de C1 &8211; C6 o t-butilo; y en donde en la fórmula IV: R10 es alquilo de C4 a C12; 25 g) utilizar HCI 2M como fase móvil; y h) recuperar 225Ac del flujo pasante, mientras que 210Po y 210Pb son retenidos en el soporte sólido
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/001424.
Solicitante: ACTINIUM PHARMACEUTICALS INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: KOLL CORPORATE CENTER 25 B HANOVER ROAD FLORHAM PARK, NJ 07932 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KABAI,EVA, HENKELMANN,RICHARD, TURLER,ANDREAS, HUENGES,ERNST, MORENO BERMUDEZ,JOSUE,MANUEL.
Fecha de Publicación: .
Fecha Solicitud PCT: 19 de Febrero de 2007.
Fecha Concesión Europea: 14 de Julio de 2010.
Clasificación Internacional de Patentes:
- C22B60/02H
- G21G1/00R
- G21G4/08 FISICA. › G21 FISICA NUCLEAR; TECNICA NUCLEAR. › G21G CONVERSION DE ELEMENTOS QUIMICOS; FUENTES RADIACTIVAS. › G21G 4/00 Fuentes radiactivas. › especialmente adaptadas a las aplicaciones médicas (radioterapia por empleo de fuentes radiactivas A61N 5/10).
Clasificación PCT:
- C01F17/00 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01F COMPUESTOS DE BERILIO, MAGNESIO, ALUMINIO, CALCIO, ESTRONCIO, BARIO, RADIO, TORIO O COMPUESTOS DE LOS METALES DE LAS TIERRAS RARAS (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; sulfuros o polisulfuros de magnesio, calcio, estroncio o bario C01B 17/42; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base C01B 37/00; compuestos que tienen propiedades de tamices moleculares y de cambiadores de base, p. ej. zeolitas cristalinas, C01B 39/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › Compuestos de los metales de tierras raras.
- C22B60/02 C […] › C22 METALURGIA; ALEACIONES FERROSAS O NO FERROSAS; TRATAMIENTO DE ALEACIONES O METALES NO FERROSOS. › C22B PRODUCCION O AFINADO DE METALES (fabricación de polvos metálicos o sus suspensiones B22F 9/00; producción de metales por electrólisis o electroforesis C25 ); PRETRATAMIENTO DE MATERIAS PRIMAS. › C22B 60/00 Obtención de metales que tienen un número atómico mayor o igual que 87, p. ej. metales radiactivos. › Obtención de torio, uranio u otros actínidos.
- G21G4/08 G21G 4/00 […] › especialmente adaptadas a las aplicaciones médicas (radioterapia por empleo de fuentes radiactivas A61N 5/10).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
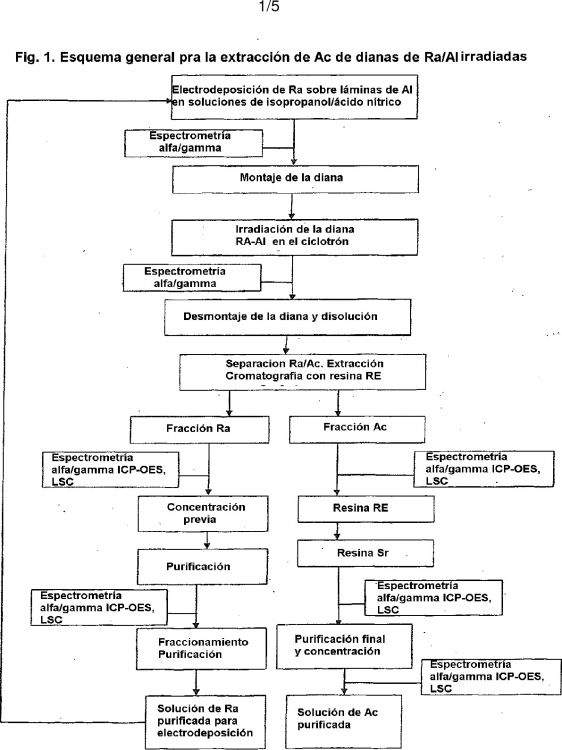
Fragmento de la descripción:
La presente invención se refiere a un método para la purificación de 225Ac a partir de dianas marcadas con 226Ra irradiadas dispuestas sobre un soporte de acuerdo con las reivindicaciones 1 a 3. Además, la invención se refiere a una composición de radionucleidos que contiene 225Ac de acuerdo con la reivindicación 21.
En particular, el radionucleido 225Ac puede utilizarse con éxito en medicina nuclear – en casos de anticuerpos específicos de tumores – en diversas pruebas clínicas para el tratamiento del cáncer, particularmente en forma de su nucleido hijo 213Bi.
Ya en 1993, se dieron por primera vez los criterios para la selección de radionucleidos para inmunoterapia con emisores º y emisores º (GEERLINGS, M.W. (1993): Int. J. Biol. Markers, 8, 180-186: "Radionuclides for radioimmunotherapy: criteria for selection") de donde surgió debido a la diferencia de energía que la radiactividad de los emisores º que ha de aplicarse puede ser más de 1000 veces inferior a la de los emisores º, si se pretende conseguir un efecto comparable.
Por otra parte, en la bibliografía anterior, los radionucleidos 225Ac que emiten rayos º y su isótopo hijo 213Bi parecían ser muy prometedores para radioinmunoterapia junto con el conjugado de anticuerpos, en principio utilizable, sin embargo relativamente poco disponible o inestable, que produce los emisores º: 221At, 255Fm, 212Bi/212Pb,
224Ra, 233Ra.
Uno de los estudios esenciales para el fundamento de una radioinmunoterapia con emisores º está descrito en GEERLINGS, M.W., KASPERSEN, F.M., APOSTOLIDIS; C. y VAN DER HOUT, R. (1993): Nuclear Medicine Communications 14, 121-125, "The feasibility of 225Ac as a source of º-particles in radioimmunotherapy". En dicho texto se describe que 225Ac producido a partir de 229Th y el isótopo hijo de 225Ac, es decir 213Bi, es adecuado como isótopo para la radioinmunoterapia con emisores de partículas º. Como indicaciones se describe en particular el tratamiento de cáncer y el tratamiento de micrometástasis de tumores malignos utilizando anticuerpos monoclonales específicos de tumores, como portadores de los emisores de partículas º.
Un estudio adicional de KASPERSEN, F.M., BOS, E., DOORNMALEN, A.V., GEERLINGS, M.W., APOSTOLIDIS, C. y MOLINET, R. (1995): Nuclear Medicine Communications, 16, 468-476: "Cytotoxicity of 213Bi-and 225Ac -immunoconjugates" confirma y cuantifica el efecto citotóxico de 213Bi y 225Ac con ensayos in vitro que utilizan la línea celular tumoral epidermoide humana A431.
Por otra parte, se sugiere la utilización de 213Bi para el tratamiento de enfermedades malignas del sistema sanguíneo.
Además, en KASPERSEN et al. 1995 puede encontrarse un procedimiento por el cual pueden unirse químicamente anticuerpos a un agente quelante adecuado para 213Bi y 225Ac. Se ha demostrado que, por ejemplo, el p-isotiocianatobencildietilentriamina-pentaacetato (bencil-DTPA) es particularmente adecuado.
Otro agente quelante, a saber el ciclohexil-DTPA ha sido descrito, por ejemplo, por NIKULA, T.K., McDEVITT, M.R., FINN, R.D., WU, C., KOZAK, R.W., GARMESTANI, K, BRECHBIEL, M.W., CURCIO, M.J.,. PIPPIN, C.G., TIFFANY-JONES, L., GEERLINGS, M.W., Sr., APOSTOLIDIS, C., MOLINET, R., GEERLINGS, M.W., Jr., GANSOW, O.A. Y SCHEINBERG, D.A. (1999): J. Nucl. Med. 40, 166-176: Alpha-Emitting Bismuth Cyclohexylbenzyl DTPA Constructs of Recombinant Humanized AntiCD33 Antibodies: Pharmacokinetics, Bioactivity, Toxicity and Chemistry".
Una revisión general sobre la química de agentes quelantes puede encontrarse, por ejemplo, en HASSFJELL, S. y BRECHBIEL, W. (2001): Chem. Rev., 101, 2019-2036: "The Development of the º-Particle Emitting Radionuclides 212Bi and 213Bi and Their Decay Chain Related Radionuclides, For Therapeutic Applications”.
Mientras tanto, se encuentran en diversas fases de pruebas clínicas varios procedimientos radioinmunoterapéuticos con 225Ac y 213Bi para el tratamiento del cáncer.
La importancia médico-clínica de la presente invención puede observarse, por ejemplo, en dos prometedores procesos terapéuticos:
Por un lado, JURCIC, J.G., LARSON, S.M., SGOUROS, G., McDEVITT, M.R., FINN, R.D., DIVGI, C. R. Áse, M.B., HAMACHER, K.A., DANGSHE,M., HUMM, J.L., BRECHBIEL, M. W., MOLINET, R., SCHEINBERG, D.A. (2002) en Blood, 100, 12331239 describen un éxito significativo en el tratamiento de pacientes con leucemia mielógena aguda (AML) y leucemia mielógena crónica (CML) utilizando 213Bi, que está unido a HuM195, una formulación de un anticuerpo monoclonal anti-CD33, que se desarrolló para la medicina humana. Este fue el primer estudio demostrativo en el que se trató un ser humano con una radioinmunoterapia sistémica que comprende un emisor de partículas º, que son transportadas a una diana celular específica de tumores.
Por otro lado, HUBER, R., SEIDL, C., SCHMID, E., SEIDENSCHWANG, S., BECKER, K. F., SCHUMACHER, C., APOSTOLIDIS, C., NIKULA, T., KREMMER, E., SCHWAIGER, M. y SENEKOWITSCH-SCHMIDTKE, R. (2003): Clinical Cancer Research (Suppl.) 9, 1s-6s: "Locoregional º-Radioimmunotherapy of Intraperitoneal Tumor Cell Dissemination Using a Tumor-specific Monoclonal Antibody" describen la eficacia terapéutica de 213Bi-d9MAB – con baja toxicidad para la médula ósea – y la posible aplicación de una terapia locorregional a pacientes con carcinoma gástrico, que expresa d9-E-Cadherina.
Más resultados de estudios y aspectos parciales de este tema se muestran en la tesis doctoral de Roswitha HUBER, en la Facultad de Medicina Veterinaria dependiente de la Universidad Ludwig-Maximilians de Munich, 18 de julio, 2003: "Bewertung der lokoregionalen Radioimmuntherapie disseminierter Tumorzellen des diffusen Magenkarzinoms mit einem 213Bi gekoppelten tumorspezifischen Antikdrper im Mausmodell" (Evaluación de una radioinmunoterapia locorregional de células tumorales diseminadas del carcinoma gástrico difuso con un anticuerpo específico del tumor unido a 213Bi en el modelo de ratón).
Esta tesis comenzó en la Clínica y Policlínica de Medicina Nuclear de la Universidad Técnica de Munich, el Hospital universitario “Klinikum rechts der Isar”, decano: Prof. Dr. M. Schwaiger. La tesis se realizó bajo la supervisión del Prof. Dr. Med. Dr. Phil. Reingard Senekowitsch-Schmidtke y fue presentada en la Facultad de Veterinaria por el Prof. Dr. Med. Vet. K. Tempel, Instituto de Farmacología, Toxicología y Farmacia de la Facultad de Medicina Veterinaria de la Universidad Ludwig-Maximilians de Munich, director: Prof. Dr. Med. Vet. R. Schulz.
Según HUBER 2003, cada año sólo 18 de cada 100.000 alemanes enferman de carcinoma gástrico. En Japón, llegan a estar afectados 126 de cada 100.000 personas. Esto significa aproximadamente 156.000 casos al año sólo en Japón. Tanto allí como en China, Taiwan y Corea, el carcinoma gástrico es una de las causas más frecuentes de muerte como consecuencia de un tumor. Cuando se diagnostica una carcinomatosis peritoneal, la consecuencia de la expansión difusa de células tumorales en la cavidad abdominal, la esperanza de vida de un paciente es actualmente de alrededor de 12 meses. Incluso con carcinoma gástrico extirpable, es decir con carcinoma que no se ha diseminado y con resultados de diagnóstico negativos con relación a los ganglios linfáticos, el índice de supervivencia de tres años sin progresión es sólo de aproximadamente el 45%.
Hasta ahora la aplicación de agentes citostáticos incluidos en la quimioterapia parece ser el camino terapéutico más prometedor.
Sin embargo, los efectos secundarios varían desde inmunosupresión, coagulopatía, anoxia metabólica, mucositis e hiperuricemia hasta el peligro de tumores secundarios inducidos por los agentes citostáticos. Particularmente afectado en este caso es el tejido muy proliferante, como la médula ósea y el epitelio del tracto gastrointestinal, así como la mucosa bucal.
En contraste, la radioinmunoterapia utiliza estructuras proteínicas localizadas en la membrana, que son expresadas por líneas de células tumorales con el fin de unirse a sustancias activas citotóxicas por medio de un vehículo. Normalmente, una sobreexpresión de la molécula de unión en la célula tumoral es fundamental para una radioinmunoterapia. La molécula diana para los anticuerpos asociados al tumor se expresa también por tanto en un menor grado en las células fisiológicas del organismo. Esto implica que cualquier agente terapéutico...
Reivindicaciones:
Reivindicaciones
1. Método para purificar 225Ac a partir de dianas de 226Ra irradiadas dispuestas sobre un soporte, que comprende las siguientes etapas:
5 a) efectuar al menos un tratamiento de lixiviación de las dianas de 226Ra para lixiviar esencialmente la totalidad de 225Ac y 226Ra con ácido nítrico o clorhídrico en condiciones de reflujo;
b) eliminar HCI si el disolvente en la etapa a) es ácido clorhídrico y disolver de nuevo el material resultante en ácido nítrico; 10 c) concentrar los extractos que contienen 225Ac y 226Ra;
d) separar 225Ac de 226Ra y otros isótopos de Ra por medio de al menos una primera cromatografía de extracción con un material soporte sólido que tiene un primer sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general I en al menos un compuesto de acuerdo con la fórmula general II,
**(Ver fórmula)**
Fórmula I
**(Ver fórmula)**
Fórmula II
en donde en la fórmula I:
R1, R2 son independientemente octilo, n-octilo, fenilo o fenilo sustituido con alquilo de C1 a C3; R3, R4 son independientemente propilo, isopropilo, butilo o isobutilo; en donde en la fórmula II: R5, R6 y R7 son independientemente alquilo de C2 -C5, en particular, butilo o isobutilo; e) eluir 225Ac que es retenido en el soporte sólido de la fase estacionaria
con ácido nítrico o clorhídrico, mientras se hace pasar a su través 226Ra;
10 f) separar 225Ac de 210Po y 210Pb por medio de al menos una segunda cromatografía de extracción con un material soporte sólido que tiene un segundo sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general III en al menos un compuesto de la fórmula general IV,
**(Ver fórmula)**
Fórmula III R10 ºº OH Fórmula IV
en donde en la fórmula III: R8 y R9 son independientemente H, alquilo de C1 – C6 o t-butilo; y en donde en la fórmula IV: R10 es alquilo de C4 a C12;
25 g) utilizar HCI 2M como fase móvil; y h) recuperar 225Ac del flujo pasante, mientras que 210Po y 210Pb son retenidos en el soporte sólido.
2. El método para purificar 225Ac a partir de dianas de 226Ra irradiadas dis30 puestas sobre un soporte, que comprende las siguientes etapas:
a) efectuar al menos un tratamiento de lixiviación de las dianas de 226Ra para lixiviar esencialmente la totalidad de 225Ac y 226Ra con ácido nítrico o clorhídrico en condiciones de reflujo; b) eliminar HCI si el disolvente en la etapa a) es ácido clorhídrico y di5 solver de nuevo el material resultante en ácido nítrico; c) concentrar los extractos que contienen 225Ac y 226Ra; d) separar 225Ac de 226Ra y otros isótopos de Ra por medio de al menos una primera cromatografía de extracción con un material soporte sólido que tiene un primer sistema de extracción revestido sobre él, que 10 comprende al menos un compuesto de acuerdo con la fórmula general IA,**(Ver fórmula)**
Fórmula IA
en donde en la fórmula IA: R1a, R2a, R3a, R4a son independientemente octilo o 2-etilhexilo; e) eluir 225Ac que es retenido en el soporte sólido de la fase estacionaria
con ácido nítrico en un intervalo de concentración de 0,3 M a 0,01 M 20 o ácido clorhídrico 1 M a 0,05 M, mientras se hace pasar a su través 226Ra;
f) separar 225Ac de 210Po y 210Pb por medio de al menos una segunda cromatografía de extracción con un material de soporte sólido que tiene un segundo sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general III en al menos un compuesto de acuerdo con la fórmula general IV,
**(Ver fórmula)**
Fórmula III R10 ºº OH Fórmula IV
en donde en la fórmula III: R8 y R9 son independientemente H, alquilo de C1 -C6 o t-butilo; y en la fórmula IV: R10 es alquilo de C4 a C12; g) utilizar HCI 2M como fase móvil; y h) recuperar 226Ac del flujo pasante, mientras 210Po y 210Pb son retenidos
en el soporte sólido.
3. Método para purificar 225Ac a partir de dianas de 226Ra irradiadas dispuestas sobre un soporte, que comprende las siguientes etapas:
a) efectuar al menos un tratamiento de lixiviación de las dianas de 226Ra para lixiviar esencialmente la totalidad de 225Ac y 226Ra con ácido nítrico o clorhídrico en condiciones de reflujo;
b) eliminar HCI si el disolvente en la etapa a) es ácido clorhídrico y di
solver de nuevo el material resultante en ácido nítrico; c) concentrar los extractos que contienen 225Ac y 226Ra; d) separar 225Ac de 226Ra y otros isótopos de Ra por medio de al menos
una primera cromatografía de extracción con un material soporte sólido que tiene un primer sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general IB,
**(Ver fórmula)**
Fórmula IB e) eluir 225Ac que es retenido en el soporte sólido de la fase estacionaria 5 con ácido nítrico que tiene una concentración inferior a aproximadamente 0,1 M y superior a aproximadamente 0,02 M, mientras se hace pasar a su través 226Ra; f) separar 225Ac de 210Po y 210Pb por medio de al menos una segunda cromatografía de extracción con un material soporte sólido que tiene 10 un segundo sistema de extracción revestido sobre él, que comprende al menos un compuesto de acuerdo con la fórmula general III en al menos un compuesto de acuerdo con la fórmula general IV,**(Ver fórmula)**
15 Fórmula III R10 ºº OH Fórmula IV
en donde en la fórmula III: 20 R8 y R9 son independientemente H, alquilo de C1 -C6 o t-butilo; y en donde en la fórmula IV:
R10 es alquilo de C4 a C12;
g) utilizar HCI 2M como fase móvil; y
h) recuperar 226Ac del flujo pasante, mientras 210Po y 210Pb son retenidos
en el soporte sólido.
4. Método de acuerdo con las reivindicaciones 1 a 3, en el que el soporte se selecciona del grupo que consiste en metales, en particular aluminio o aleaciones de aluminio, aluminio pasivado, aluminio anodizado, aluminio revestido con un elemento del grupo del platino; metales preciosos, en particular elementos del grupo del platino; y sus mezclas.
5. Método de acuerdo con las reivindicaciones 1 a 4, en el que el ácido nítrico de la etapa a) tiene un intervalo de concentración de aproximadamente 0,001 M a 2 M, preferiblemente alrededor de 0,1 M y el ácido clorhídrico tiene un intervalo de concentración de 0,001 M a 2 M, y/o dichos ácidos se utilizan a temperaturas elevadas, en particular de aproximadamente 30 a 90ºC.
6. Método de acuerdo con las reivindicaciones 1 a 5, en el que se reúnen los extractos del tratamiento de lixiviación.
7. Método de acuerdo con las reivindicaciones 1 a 6, en el que en la etapa c) se alcanza una concentración final de 1,5 M a 10 M de ácido nítrico.
8. Método de acuerdo con la reivindicación 1, en el que el primer sistema de extracción es óxido de octil(fenil)-N,N-diisobutilcarbamoilfosfina [CMPO] en fosfato de tributilo [TBP].
9. Método de acuerdo con las reivindicaciones 1 a 3, en el que el segundo sistema de extracción es un éter corona de acuerdo con la fórmula V:
Fórmula V en 1-octanol.
10. Método de acuerdo con la reivindicación 9, en el que el segundo sistema de extracción es 4,4'-bis(t-butilciclohexano)-18-corona-6 en 1-octanol.
11. Método de acuerdo con la reivindicación 9, en el que el segundo sistema de extracción es 4,5'-bis(t-butilciclohexano)-18-corona-6 en 1-octanol.
12. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que la primera cromatografía de extracción de la etapa d) se repite varias veces, con el fin de eliminar las cantidades trazas de isótopos de Ra, dependiendo de la pureza deseada del 225Ac.
13. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que se repite varias veces la segunda cromatografía de extracción de la etapa f), dependiendo de la pureza deseada del 225Ac.
14. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que se recupera el 226Ra del flujo pasante de la etapa e).
15. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que 210Po se eluye a partir del soporte sólido de la segunda cromatografía de extracción en la etapa h) por medio de ácido nítrico concentrado o ácido clorhídrico concentrado, y 210Pb se eluye con ácido clorhídrico concentrado o solución de EDTA.
16. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que cada etapa o fracción de purificación se comprueba por medio de espectroscopia º y/o º (gamma).
**(Ver fórmula)**
17. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que se evaporan las fracciones respectivas que contienen: a) 225Ac; o 5 b) Isótopos de Ra; o
c) 210Po; y 210Pb
d) hasta obtener residuos húmedos o secos y se vuelven a disolver, si es necesario.
10 18. Método de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que se separan las impurezas orgánicas, preferiblemente haciéndolas pasar por una resina que contiene un polímero de éster acrílico no iónico.
19. Composición de radionucleidos que contiene 225Ac farmacéuticamente aceptable obtenible por un método de acuerdo con al menos una de las reivindicaciones 1 a 18.
Patentes similares o relacionadas:
 Sistema de elución de radioisótopos de autoalineación, del 28 de Agosto de 2019, de Curium US LLC: Un sistema de elución de radioisótopos , incluyendo:
un protector auxiliar ;
una tapa protectora que incluye un asa (80, […]
Sistema de elución de radioisótopos de autoalineación, del 28 de Agosto de 2019, de Curium US LLC: Un sistema de elución de radioisótopos , incluyendo:
un protector auxiliar ;
una tapa protectora que incluye un asa (80, […]
Método y aparato para la producción de plomo 212 para un uso médico, del 26 de Septiembre de 2018, de Orano Med: Metodo de produccion de plomo 212 de calidad medica, que comprende: - la produccion de plomo 212 por desintegracion de radio 224 en un generador que contiene […]
Sistemas para generación, preparación, transporte y administración de productos radiofarmacéuticos integrados, del 11 de Abril de 2018, de BAYER HEALTHCARE LLC: Un sistema de manipulación de fluidos peligrosos , que comprende: una estación de acoplamiento , que comprende: una bomba (1012, […]
Generador de radioisótopos, del 29 de Marzo de 2017, de GE HEALTHCARE LIMITED: Un generador de radioisótopos, que comprende: un recipiente exterior en el que hay situado un recipiente blindado , comprendiendo dicho recipiente […]
Generador de radionucleido con molécula para la funcionalización de un soporte, la unión de un radionucleido al soporte y generador de radionucleidos para la producción del radionucleido, así como procedimiento de producción, del 1 de Marzo de 2017, de ITM Isotopen Technologies München AG: Generador de radionucleidos Ge-68/Ga-68, que comprende: - una molécula con por lo menos un grupo funcional para la unión de un nucleido padre radiactivo y un grupo molecular, […]
Sistema de elución de radioisótopos de autoalineación, del 7 de Diciembre de 2016, de Mallinckrodt Nuclear Medicine LLC: Un sistema de elución de radioisótopos , incluyendo: un protector auxiliar ; una tapa protectora que incluye un asa , donde la tapa protectora […]
Sistema de elución de radioisótopos de autoalineación, del 20 de Julio de 2016, de Mallinckrodt Nuclear Medicine LLC: Un sistema de elución de radioisótopos incluyendo un generador de radioisótopos y un conjunto protector antirradiación , donde el generador de radioisótopos […]
 Sistema y método radiofarmacéutico utilizando etiquetas de identificación por radiofrecuencia, del 22 de Febrero de 2016, de Mallinckrodt LLC: Un sistema radiofarmacéutico para generar radioisótopos por elución, y que comprende un generador de radioisótopos que tiene una aguja de entrada y una aguja de […]
Sistema y método radiofarmacéutico utilizando etiquetas de identificación por radiofrecuencia, del 22 de Febrero de 2016, de Mallinckrodt LLC: Un sistema radiofarmacéutico para generar radioisótopos por elución, y que comprende un generador de radioisótopos que tiene una aguja de entrada y una aguja de […]