IMPLANTES DE GESTIÓN DE FLUJO DE FLUIDOS DE RESISTENCIA A OCLUSIÓN MEJORADA.
Un implante de gestión de flujo de fluidos que comprende: a) un catéter de drenaje antimicrobiano o elución de fármaco,
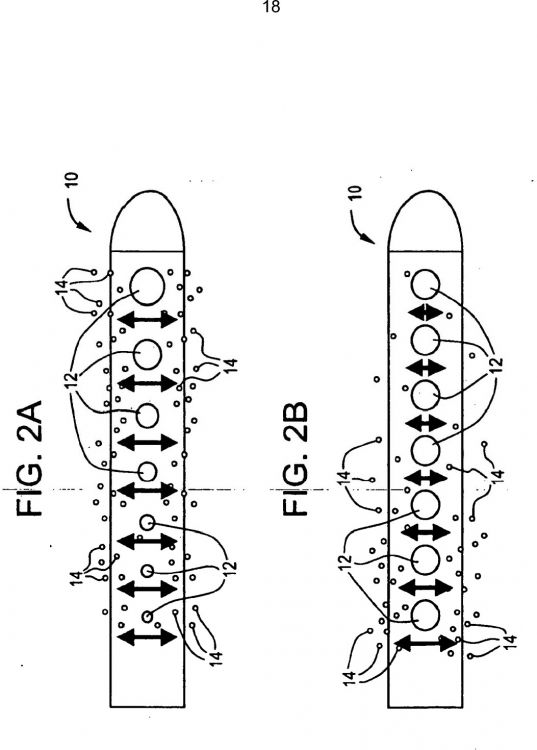
que comprende un extremo proximal y uno distal; caracterizado por que b) un agente antimicrobiano o un fármaco que evita o minimiza el crecimiento del tejido se recubre sobre dicho catéter o se impregna en dicho catéter; y c) una punta de potenciación de distribución de flujo (10) se proporciona en el extremo distal del catéter, en el que la punta de potenciación de distribución de flujo (10) comprende un extremo distal que está sellado y una pluralidad de aperturas de entrada (12) localizadas entre los extremos distal y proximal de la punta (10) y las aperturas de entrada (12) aumentan progresivamente en el área de sección transversal desde la apertura de entrada más próxima a la apertura de entrada más distal
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05256107.
Solicitante: CODMAN & SHURTLEFF INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 325 PARAMOUNT DRIVE RAYNHAM, MASSACHUSETTS 02767 ESTADOS UNIDOS DE AMERICA.
Inventor/es: Dextradeur,Alan , Mauge,Christophe.
Fecha de Publicación: .
Fecha Solicitud PCT: 29 de Septiembre de 2005.
Clasificación Internacional de Patentes:
- A61L29/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 29/00 Materiales para catéteres o para su revestimiento (forma o estructura de los catéteres A61M 25/00). › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
- A61L31/16 A61L […] › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
Clasificación PCT:
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
1. Campo de la Invención
La presente invención se refiere a dispositivos de gestión de flujo de fluidos y, en particular, a derivaciones de hidrocefalia que contienen un antibiótico y/o fármaco para minimizar el riesgo de bloqueo u obstrucción dentro del catéter, mientras que mejoran la protección frente a la colonización de bacterias gram positivas y/o la proliferación de tejidos cuando los dispositivos se combinan con puntas de potenciación de flujo de fluido uniforme.
2. Técnica Relacionada
La hidrocefalia es una afección neurológica que está provocada por la acumulación anormal de líquido cefalorraquídeo (CSF) dentro de los ventrículos o cavidades del cerebro. El CSF es un fluido transparente, incoloro, que se produce principalmente por el plexo coroideo, y rodea el cerebro y la médula espinal. El CSF circula constantemente a través del sistema ventricular del cerebro y finalmente se absorbe en el torrente circulatorio. El CSF ayuda en la protección del cerebro y la médula espinal. Debido a que el CSF mantiene el cerebro y la médula espinal flotando, actúa como un cojín protector o “absorbedor de choque” para evitar lesiones en el sistema nervioso central.
La hidrocefalia, que afecta a niños y adultos, surge cuando el drenaje normal de CSF en el cerebro se bloquea de alguna manera. Dicho bloqueo puede estar provocado por numerosos factores incluyendo, por ejemplo, predisposición genética, hemorragia intraventricular o intracraneal, infecciones, tales como meningitis, traumatismo craneal o similares. El bloqueo del flujo de CSF, en consecuencia, crea un desequilibrio entre la cantidad de CSF producido por el plexo coroideo y la velocidad a la que el CSF se absorbe en el torrente circulatorio, aumentando de esta manera la presión en el cerebro, lo que provoca que los ventrículos se dilaten.
Algunos de estos problemas pueden tratarse por retrolavado, que es un proceso que usa el CSF presente en el sistema de derivación para retirar la materia obstructora. Este proceso puede ser ineficaz, sin embargo, debido al pequeño tamaño de los poros del catéter ventricular y debido a la pequeña cantidad de líquido de lavado disponible en el sistema de derivación. Otros sistemas de derivación se han diseñado para incluir un mecanismo para el lavado del sistema de derivación. Por ejemplo, algunos sistemas de derivación incluyen un dispositivo de bombeo dentro del sistema, que provoca que el fluido en el sistema fluya con una presión y velocidad considerables, lavando de esta manera el sistema. Como con el proceso de retrolavado, usar un mecanismo de inclusión para lavar el sistema de derivación puede fallar para retirar la obstrucción debido a factores tales como el tamaño de los poros y el grado de extensión al que los poros se han atascado.
Los catéteres ventriculares ocluidos pueden repararse también por cauterización del catéter, para retirar el tejido bloqueado, reabriendo de esta manera los poros existentes que han quedado ocluidos. Como alternativa, pueden crearse nuevos poros en el catéter. Estas reparaciones, sin embargo, pueden ser incapaces de retirar las obstrucciones del catéter ventricular, dependiendo de la localización de los poros atascados. Adicionalmente, la extensión del crecimiento del tejido hacia el interior de y alrededor del catéter puede impedir también la creación de poros adicionales, por ejemplo en situaciones donde el crecimiento de tejido cubre una parte sustancial del catéter ventricular. Otra desventaja de crear nuevas aperturas para reparar un catéter ventricular ocluido es que este método falla a la hora de prevenir o reducir el riesgo de obstrucciones repetidas.
Debido a que los intentos de lavado o reparación de un catéter ventricular bloqueado a menudo son vanos e ineficaces, la oclusión se trata más a menudo sustituyendo el catéter. Aunque esto puede conseguirse simplemente retirando el catéter obstruido del ventrículo, el crecimiento del plexo coloideo y otros tejidos alrededor del catéter y hacia los poros puede impedir la retirada y sustitución del catéter. Debe tenerse cuidado de evitar el daño al plexo coloideo, que puede provocar lesión grave al paciente, tal como por ejemplo hemorragia. Estos procedimientos no sólo suponen un riesgo significativo de lesión para el paciente, también pueden ser muy costosos, especialmente cuando la obstrucción de derivación es un problema recurrente.
El documento US 4.917.686, describe dispositivos médicos implantados (tales como catéteres, válvulas, piezas moldeadas, etc. e incluye derivaciones de hidrocefalia y catéteres venosos centrales) que se han tratado con agentes antimicrobianos para combatir el problema de colonización de bacterias,
particularmente en las superficies interiores del dispositivo.
El documento US 2003/0216710, describe un catéter que tiene uno o más orificios de entrada a lo largo de la longitud del catéter, con lo que las áreas de sección transversal de los orificios de entrada sucesivos disminuyen, ocurriendo en primer lugar la disminución en el orificio de entrada inmediatamente después del orificio de entrada más próximo. Dicho diseño supone alterar el flujo de entrada típico del fluido hacia el catéter, de manera que un volumen desproporcionadamente de alto de fluido no entra más en el orificio de entrada más próximo. La disminución en el flujo de entrada en la entrada más próxima da como resultado una menor deposición de residuos dentro del catéter en esta posición.
Lin et al., en “Computational and Experimental Study of Proximal Flow Ventricular Catheters”, (J. Neurosurgery 99: 426-431, 2003), describen y demuestran que la geometría del orificio de drenaje, de hecho, es un factor para conseguir patrones de flujo uniformes dentro de los catéteres ventriculares. La Figura 2 de Lin demuestra drásticamente la mejora en la distribución de flujo cuando se modifica la geometría del orificio del catéter. El problema abordado por Lin se refiere a agentes de obstrucción tales como coágulos sanguíneos, agrupaciones celulares y tejido normal como causa de oclusión del catéter en su extremo proximal. No se mencionan dispositivos médicos implantables antimicrobianos o basados en fármacos, tales como catéteres o derivaciones, en un intento de aliviar la oclusión del lumen del catéter provocada por la formación de biopelícula a través de colonización bacteriana u oclusión mediante proliferación del tejido.
Por consiguiente, existe una necesidad de implantes de gestión de flujo de fluidos, tal como derivaciones y sistemas de derivación de catéter que minimizan o eliminan el riesgo de bloqueo u obstrucción en el implante, y reducen la posibilidad de biopelícula bacteriana u oclusión de tejidos dentro de los lúmenes y superficies internas de los implantes.
El documento WO2004/073768 describe una derivación de gestión de flujo de fluido, que comprende un catéter de drenaje de elución de fármaco.
El documento EP-A-1364628 describe un recubrimiento de elución de fármaco que puede aplicarse a un amplio intervalo de dispositivos médicos, incluyendo derivaciones para hidrocefalia.
El documento US-A-2004/0054351 describe un catéter de inyección para el suministro uniforme de un medicamento. El catéter tiene una punta de potenciación de la distribución de flujo que tiene aperturas de salida que aumentan progresivamente en el área de la sección transversal, desde la apertura de salida más proximal a la apertura de salida más distal.
El documento US-A-4950232 describe un catéter para un drenaje de líquido cefalorraquídeo que tiene una punta de drenaje en la que los orificios están protegidos frente a la oclusión en un surco, permitiendo un flujo de fluido sin alteraciones.
El documento US-B-6533763 describe catéteres mejorados para la retirada y/o suministro de fluidos a un paciente, en particular para hemodiálisis. El catéter puede tener aperturas de salida que aumentan progresivamente en el área de sección transversal desde la apertura de entrada más proximal a la apertura de entrada más distal.
El documento WO94/07549 describe un catéter para el suministro de fármaco a vasos sanguíneos remotos. El catéter puede tener aperturas de salida que aumentan progresivamente en el área de la sección transversal desde la apertura de entrada más proximal a la apertura de entrada más distal.
La presente invención proporciona un implante de gestión de flujo de fluido que comprende: (a) un catéter de drenaje de elución de fármaco o antimicrobiano...
Reivindicaciones:
1. Un implante de gestión de flujo de fluidos que comprende: a) un catéter de drenaje antimicrobiano o elución de fármaco, que comprende un extremo proximal y uno distal; caracterizado por que
b) un agente antimicrobiano o un fármaco que evita o minimiza el crecimiento del tejido se recubre sobre dicho catéter o se impregna en dicho catéter; y
c) una punta de potenciación de distribución de flujo (10) se proporciona en el extremo distal del catéter, en el que la punta de potenciación de distribución de flujo (10) comprende un extremo distal que está sellado y una pluralidad de aperturas de entrada (12) localizadas entre los extremos distal y proximal de la punta (10) y las aperturas de entrada (12) aumentan progresivamente en el área de sección transversal desde la apertura de entrada más próxima a la apertura de entrada más distal.
2. El implante de la reivindicación 1, en el que el implante es una derivación.
3. El implante de la reivindicación 2, en el que el implante es una derivación de hidrocefalia.
4. El implante de la reivindicación 1, en el que el catéter está recubierto o impregnado con agentes antimicrobianos seleccionados entre el grupo que consiste en tetraciclinas, rifamicinas, macrólidos, penicilinas, cefalosporinas, otros antibióticos de beta-lactama, aminoglucósidos, cloramfenicol, sulfonamidas, glucopéptidos, quinolonas, ácido fusídico, trimetroprim, metronidazol, clindamicinas, mupirocina, polienos, azoles, inhibidores de betalactama y mezcla de los mismos.
5. El implante de la reivindicación 4, en el que el agente antimicrobiano se selecciona entre el grupo que consiste en isminociclina, rifampina, eritromicina, nafcilina, cefazolina, imipenem, aztreonam, gentamicina, sulfametoxazol, vancomicina, ciprofloxacina, trimetoprim, metronidazol, clindamicina, teicoplanina, mupirocina, azitromicina, claritromicina, ofloxacina, lomefloxacina,
norfloxacina, ácido nalidíxico, esparfloxacina, pefloxacina, amifloxacina, enoxacina, fleroxacina, temafloxacina, tosufloxacina, clinafloxacina, sulbactama, ácido clavulánico, anfotericina B, fluconazol, itraconazol, cetoconazol, nistatina y mezclas de los mismos.
6. El implante de la reivindicación 4, en el que el agente antimicrobiano se selecciona entre el grupo que consiste en rifampina, clorhidrato de clindamicina y mezclas de los mismos.
7. El implante de la reivindicación 1, en el que el fármaco recubierto o impregnado en el catéter de elución del fármaco comprende un fármaco seleccionado entre el grupo que consiste en alcaloides de la vinca, paclitaxel, epidipodofilotoxinas, antraciclinas, mitoxantrona, bleomicinas, plicamicina (mitramicina) y mitomicina, enzimas; agentes antiplaquetarios; agentes de alquilación antiproliferativos/antimitóticos; antimetabolitos antiproliferativos/antimitóticos; complejos de coordinación de platino; hormonas; anticoagulantes; agentes fibrinolíticos; esteroides anti-inflamatorios, agentes no esteroideos; derivados de para-aminofenol; ácidos indol e indeno acéticos, ácidos heteroaril acéticos, ácidos micofenólicos, ácidos enólicos, nabumetona, compuestos de oro; inmunosupresores; sirolimus (rapamicina), azatioprina, mofetil micofenolato); agentes angiogénicos: factor de crecimiento endotelial vascular (VEGF), factor de crecimiento de fibroblastos (FGF); bloqueadores del receptor de angiotensina; donadores de óxido nítrico; oligonucleótidos antisentido y combinaciones de los mismos; inhibidores del ciclo celular, inhibidores de mTOR, e inhibidores de quinasa de transducción de señal del receptor del factor de crecimiento; retenoides; inhibidores de ciclina/CDK; inhibidores de reductasa de co-enzima HMG (estatinas); inhibidores de proteasas y mezclas de los mismos.
8. El implante de la reivindicación 7, en el que el fármaco comprende paclitaxel.
9. El implante de la reivindicación 7, en el que el fármaco comprende una combinación de sirolimus y ácido micofenólico.
10. El implante de la reivindicación 7, en el que el fármaco comprende sirolimus.
Patentes similares o relacionadas:
Endoprótesis híbrida helicoidal, del 22 de Julio de 2020, de MEDINOL LTD.: Componente de endoprótesis principal para formar una endoprótesis, que comprende: una sola tira que tiene una pluralidad de arrollamientos […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composición de fármaco y revestimiento asociado, del 1 de Julio de 2020, de W.L. GORE & ASSOCIATES, INC.: Un producto sanitario para administrar un agente terapéutico a un tejido, y el producto tiene una capa de revestimiento aplicada en una superficie del producto, y la capa […]
Método de preparación de un artículo elastomérico antimicrobiano, del 20 de Mayo de 2020, de ALLEGIANCE CORPORATION: Un método de preparación de un artículo elastomérico antimicrobiano, que comprende: recubrir un artículo elastomérico con una composición de recubrimiento antimicrobiano […]
Formulación de Mesna y su uso, del 29 de Abril de 2020, de AuXin Surgery SA: Un dispositivo para administrar una formulación de Mesna a tejidos y/u órganos, que comprende una primera cámara que comprende el Mesna en forma sólida, una segunda cámara […]
Nuevos dispositivo médico y composición para ingeniería tisular basados en A-PRP, máquinas y procesos de fabricación, del 18 de Marzo de 2020, de Regen Lab SA: Una composición que comprende al menos un ácido hialurónico de bajo peso molecular y al menos un ácido hialurónico de alto peso molecular caracterizada por que: […]
Emulsiones de copolímero de politetrafluoroetileno, del 12 de Febrero de 2020, de W.L. GORE & ASSOCIATES, INC.: Un método de preparación de una emulsión de agua en disolvente que comprende un copolímero de tetrafluoroetileno disuelto en un disolvente orgánico miscible […]
Método de fabricación de dispositivos médicos antitrombogénicos, del 12 de Febrero de 2020, de Covidien LP (100.0%): Un metodo para proporcionar un dispositivo medico, en donde el dispositivo medico comprende: un cuerpo tubular expandible que comprende una pluralidad de […]