CONTROL DE GLUCOSA EN SANGRE EN EL TRATAMIENTO DE DIABETES USANDO INSULINA ADMINISTRADA POR VÍA PULMONAR EN COMBINACIÓN CON INSULINA BASAL.
El uso de una composición de insulina en la fabricación de un medicamento para uso en el tratamiento de un paciente con un trastorno relacionado con la insulina en donde la composición comprende dicetopiperazina e insulina,
es adecuado para la administración por vía pulmonar y se utiliza en combinación con una insulina basal acción prolongada
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08075731.
Solicitante: MANNKIND CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 28903 NORTH AVENUE PAINE VALENCIA, CA 91355 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BOSS, ANDERS, CHEATHAM,WAYMAN,WENDELL.
Fecha de Publicación: .
Fecha Solicitud PCT: 31 de Marzo de 2006.
Fecha Concesión Europea: 16 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K38/28 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Insulinas.
Clasificación PCT:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2362220_T3.pdf




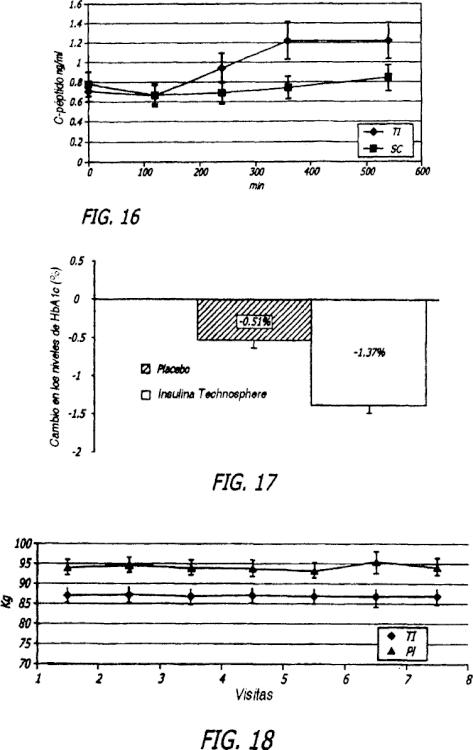
Fragmento de la descripción:
Control de glucosa en sangre en el tratamiento de diabetes usando insulina administrada por vía pulmonar en combinación con insulina basal.
Esta aplicación reivindica prioridad en virtud de 35 USC
Campo de la invención
La presente invención se refiere a métodos de tratamiento de la diabetes y un control más eficaz de la glucosa en sangre. En concreto, el método de la presente invención proporciona un control superior de los niveles de glucosa postprandial y reduce el riesgo de hipoglucemia postprandial tardía al imitar la cinética de respuesta de la insulina de un individuo no diabético.
Antecedentes de la invención
La diabetes mellitus afecta actualmente al menos 200 millones de personas en todo el mundo. La diabetes tipo 1 representa alrededor del 10% de este número, y se origina por la destrucción autoinmune de las células beta secretoras de insulina en los islotes de Langerhans en el páncreas. La supervivencia depende de múltiples inyecciones diarias de insulina. La diabetes tipo 2 representa el restante 90% de los individuos afectados, y la tasa de prevalencia va en aumento. La diabetes tipo 2 está a menudo, pero no siempre, asociada con la obesidad, y aunque anteriormente denominada diabetes de aparición tardía o diabetes del adulto, es cada vez más manifiesta en los individuos más jóvenes. Es causada por una combinación de resistencia a la insulina y la secreción inadecuada de insulina
En un individuo normal no estresado, el nivel de glucosa basal tenderá a seguir siendo el mismo de día en día debido a un mecanismo intrínseco de retrocontrol. Cualquier tendencia a aumentar de la concentración de glucosa plasmática se ve compensada por un aumento en la secreción de insulina y una supresión de la secreción de glucagón, que regulan la producción hepática de glucosa (gluconeogénesis y liberación de las reservas de glucógeno) y la captación de glucosa del tejido para mantener la concentración de glucosa plasmática constante. Si el individuo gana peso o se vuelve resistente a la insulina por cualquier otra razón, los niveles de glucosa sanguínea aumentan, resultando un aumento de la secreción de insulina para compensar la resistencia a la insulina. Por tanto, la glucosa y los niveles de insulina son modulados para minimizar los cambios en estas concentraciones, mientras que la producción normal y la utilización de glucosa se mantienen relativamente.
Han sido identificadas cinco fases diferentes en la secreción de insulina: (1) secreción de insulina basal en la cual la insulina se libera en el estado postabsortivo; (2) fase cefálica en la que la secreción de insulina es desencadenada por la vista, el olfato y el sabor de la comida, antes que cualquier nutriente sea absorbido por el intestino, mediado por la inervación del páncreas; (3) primera fase de secreción de insulina en la que hay una liberación inicial de golpe de la misma en los 5-10 minutos después de que la célula β se expone a un rápido aumento de la glucosa, u otros secretagogos; (4) segunda fase de secreción de insulina en la que los niveles de insulina aumentan de manera más gradual y se relacionan con el grado y la duración del estímulo y (5) una tercera fase de secreción de insulina que sólo se ha descrito in vitro. Durante estas etapas, la insulina es secretada, como muchas otras hormonas, de manera pulsátil, resultando unas concentraciones oscilatorias en la sangre. Estas oscilaciones incluyen pulsos rápidos (ocurren cada 8-15 minutos) superpuestos a oscilaciones más lentas (ocurren cada 80-120 minutos) que están relacionadas con fluctuaciones de la concentración de glucosa en la sangre.
La secreción de insulina puede ser inducida por otros sustratos energéticos, además de glucosa (aminoácidos en particular), así como por hormonas y fármacos. Cabe destacar que la respuesta de la insulina observada después de la ingestión de alimentos no se puede explicar exclusivamente por el aumento en los niveles de glucosa en la sangre, sino también depende de otros factores tales como la presencia de ácidos grasos libres y otros secretagogos en la comida, la activación neural de la fase cefálica y las hormonas gastrointestinales.
Cuando a un individuo se le da una sobrecarga de glucosa por vía intravenosa, hay una respuesta bifásica de la insulina que incluye un aumento rápido con un pico, un punto más bajo entre picos y un posterior aumento de fase más lenta. Esta respuesta bifásica sólo se ve cuando aumenta la concentración de glucosa rápidamente, como después de un bolo de glucosa o infusión de glucosa. Un aumento más lento en la administración de glucosa, lo que se ve en condiciones fisiológicas, induce a un aumento más gradual en la secreción de insulina sin la bien definida respuesta bifásica vista en la respuesta a un bolo o infusión de glucosa.
El modelo de la primera fase de la respuesta de la insulina bajo condiciones fisiológicas normales ha demostrado que, después de una comida, aumenta la concentración de glucosa de manera más gradual (Cmax se alcanza en aproximadamente 20 minutos) a la observada con inyecciones en bolo intravenoso de glucosa (Cmax se alcanza en aproximadamente 3-10 minutos).
Las células β pancreáticas sanas generan una respuesta temprana a la exposición de glucosa de las comidas que rápidamente eleva la insulina en suero, tanto en la circulación portal como en la periférica. Por el contrario, las células β defectuosas, que tienen una primera fase de respuesta alterada de insulina, generan una respuesta lenta a la exposición de la glucosa de las comidas.
Cada vez más, la evidencia indica que una respuesta temprana y relativamente rápida de la insulina después de la ingesta de glucosa juega un papel crítico en el mantenimiento de la homeostasis de la glucosa postprandial. Un aumento temprano de la concentración de insulina puede limitar la salida inicial de glucosa, principalmente a través de la inhibición de la producción de glucosa endógena. Por lo tanto la inducción de una respuesta rápida de insulina en una persona diabética se espera que produzca una mejora en la homeostasis de glucosa en sangre.
En un individuo normal, una comida induce la secreción de una liberación de insulina, generando un pico relativamente rápido en la concentración sérica de insulina, que luego se descompone con relativa rapidez (ver Figura 1). Esta fase de respuesta temprana de insulina es responsable del cierre de la liberación de glucosa desde el hígado. Los mecanismos homeostáticos entonces adaptan la secreción de insulina (y los niveles séricos de insulina) a la carga de glucosa. Esto es observado como una ligera disminución de niveles de insulina sérica modestamente elevados que vuelven a niveles basales y es cínética de segunda fase.
Los diabéticos tipo 2 presentan típicamente un retraso en la respuesta a los aumentos en los niveles de glucosa en la sangre. Mientras que los individuos normales por lo general comienzan a liberar insulina dentro de los 2-3 minutos después del consumo de alimentos, los diabéticos tipo 2 no pueden secretar insulina endógena hasta que la glucosa en sangre empieza a subir, y luego con la cinética de la fase segunda, que es un lento ascenso hacia una larga meseta en concentración. Como resultado, la producción de glucosa endógena no se apaga y continúa después del consumo y el paciente experimenta hiperglucemia (niveles elevados de glucosa en la sangre).
La pérdida de secreción de insulina inducida por la toma de alimentos es una de las primeras alteraciones de la función de células β. Si bien los factores genéticos juegan un papel importante, algunas alteraciones en la secreción de insulina parecen ser adquiridas y pueden ser al menos parcialmente reversibles mediante el control óptimo de la glucosa. El control óptimo de la glucosa a través de la terapia con insulina después de una comida puede llevar a una mejora significativa en la secreción de insulina inducida por glucosa de forma natural que requiere tanto la capacidad de respuesta del tejido normal a la insulina administrada como un brusco aumento en las concentraciones séricas de insulina. Por lo tanto, el reto en... [Seguir leyendo]
Reivindicaciones:
1. El uso de una composición de insulina en la fabricación de un medicamento para uso en el tratamiento de un paciente con un trastorno relacionado con la insulina en donde la composición comprende dicetopiperazina e insulina, es adecuado para la administración por vía pulmonar y se utiliza en combinación con una insulina basal acción prolongada.
2. El uso según la reivindicación 1 en donde la composición de la insulina se administra próxima al comienzo de las comidas.
3. El uso según la reivindicación 1 en donde la dicetopiperazina es fumaril dicetopiperazina.
4. El uso según la reivindicación 1 en donde la composición de la insulina es administrada por inhalación en forma de polvo seco.
5. El uso según la reivindicación 4 en donde la composición de insulina es administrada desde aproximadamente 10 minutos antes de comenzar una comida a unos 30 minutos después del comienzo de una comida.
6. El uso según la reivindicación 1 en donde el trastornos relacionado con la insulina es la diabetes mellitus.
7. El uso según la reivindicación 6 en donde el trastorno relacionado con la insulina es la diabetes mellitus tipo 2 o diabetes mellitus tipo 1.
8. El uso según la reivindicación 1 en donde la hipoglucemia postprandial tardía clínicamente relevante se reduce.
9. El uso según la reivindicación 1 en donde el aumento de peso se reduce.
10. El uso según la reivindicación 1 en donde las salidas de glucosa postprandial son menores que las salidas de glucosa postprandial que resultan de una dosis de insulina administrada por vía subcutánea proporcionando una exposición a la insulina prácticamente similar y en donde la salida de glucosa media es al menos un 25% inferior que para la administración subcutánea.
11. El uso según la reivindicación 10 en donde las salidas de glucosa postprandial son reducidas respecto a las producidas por el tratamiento con una dosis subcutánea apropiada de insulina sola.
12. El uso según la reivindicación 10 en donde la frecuencia de episodios de hipoglucemia postprandial tardía clínicamente relevante es reducido en comparación con el tratamiento con una dosis subcutánea apropiada de insulina sola.
13. El uso de una composición de la insulina en la fabricación de un medicamento para uso en el tratamiento de un paciente con un trastorno relacionado con la insulina cuya composición comprende una dicetopiperazina e insulina, es adecuado para la administración por vía pulmonar reduciendo las salidas de glucosa postprandial en un paciente con un trastorno relacionado con la insulina, y en donde la exposición a la insulina total del paciente (INS-AUC0-y,
14. El uso según la reivindicación 13 en donde el riesgo de hipoglucemia postprandial tardía no se incrementa.
15. El uso según la reivindicación 13 en donde la dicetopiperazina es fumaril dicetopiperazina.
16. El uso según la reivindicación 13 en donde la composición de insulina es administrada por inhalación en forma de polvo seco.
17. El uso de una composición de insulina en la fabricación de un medicamento para uso en el tratamiento de un paciente con un trastorno relacionado con la insulina en donde la composición comprende dicetopiperazina e insulina, y es adecuada para la administración por vía pulmonar y se utiliza en combinación con un medicamento oral para la diabetes.
Patentes similares o relacionadas:
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Formulaciones de inulina y de acetato de inulina, del 5 de Junio de 2020, de SOUTH DAKOTA STATE UNIVERSITY (100.0%): Una composición que comprende micropartículas o nanopartículas de acetato de inulina (InAc) y una molécula de carga, en la que la molécula de carga está encapsulada […]
Terapia para la diabetes, del 13 de Mayo de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un inhibidor de DPP-4, que es linagliptina, para uso terapéutico por administración subcutánea.
Formulaciones farmacéuticas estabilizadas de análogos de insulina y/o derivados de insulina, del 29 de Abril de 2020, de SANOFI: Una formulación farmacéutica que comprende (a) al menos un análogo y/o derivado de insulina, en donde dicho análogo de insulina se selecciona del grupo que […]
Dispositivo, composición y método para el diagnóstico basado en tejidos, del 29 de Abril de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un dispositivo para licuar al menos parcialmente un tejido de un sujeto vivo, que comprende: un depósito que se configura para acoplar operativamente […]
Dispositivo tragable para la administración de fármacos, del 22 de Abril de 2020, de Rani Therapeutics, LLC: Un dispositivo ingerible para la administración de un agente terapéutico hacia el interior de una pared luminal del tubo gastrointestinal de un paciente, […]
Sistemas a base de conjugados para la administración controlada de fármacos, del 18 de Marzo de 2020, de Smartcells, Inc: Un conjugado que comprende una molécula de insulina conjugada a dos o más ligandos de sacáridos, en el que los dos o más ligandos son cada uno aminoetiltrimanosa (AETM) y en […]