COMPOSICIONES PARA PRODUCIR, INCREMENTAR Y MANTENER LAS RESPUESTAS INMUNES CONTRA EPÍTOPOS RESTRINGIDOS DE MHC DE CLASE I, CON FINES PROFILÁCTICOS O TERAPÉUTICOS.
El uso de una composición de entrada que se administra directamente al sistema linfático de un mamífero,
comprendiendo dicha composición de entrada un plásmido no replicante que codifica un inmunógeno y que comprende además un inmunopotenciador, comprendiendo el inmunógeno un antígeno o su fragmento inmunógeno; y una composición de amplificación que se administra directamente al sistema linfático del mamífero, comprendiendo dicha composición de amplificación un péptido de amplificación, en el que el péptido corresponde a un epítopo de dicho antígeno, en el que la composición de entrada y la composición de amplificación no son iguales, y en el que la composición de entrada se administra al menos dos veces, en un curso de uno hasta aproximadamente siete días o como una infusión continua que tiene una duración de entre aproximadamente 8 horas hasta aproximadamente 7 días para la fabricación de un medicamento de combinación de inmunización para la profilaxis o la terapia de enfermedades infecciosas o neoplásicas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/019546.
Solicitante: MANNKIND CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 28903 NORTH AVENUE PAINE VALENCIA, CALIFORNIA 91355 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BOT,ADRIAN,ION, SMITH,KENT,ANDREW, LIU,XIPING.
Fecha de Publicación: .
Fecha Solicitud PCT: 17 de Junio de 2004.
Fecha Concesión Europea: 4 de Agosto de 2010.
Clasificación Internacional de Patentes:
- A61K39/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/00D6
Clasificación PCT:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- A61P37/00 A61P […] › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
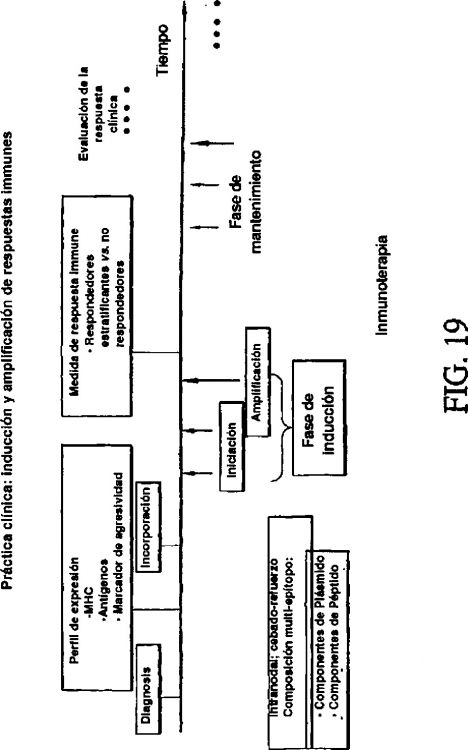
Fragmento de la descripción:
Composiciones para producir, incrementar y mantener las respuestas inmunes contra epítopos restringidos de MHC de clase I, con fines profilácticos o terapéuticos.
Antecedentes de la invención
La invención descrita en este documento se refiere a composiciones para inducir una respuesta inmune restringida al MHC (acrónimo para el inglés "major histocompatibility complex"; complejo mayor de histocompatibilidad) clase I y controlar la naturaleza y la magnitud de la respuesta, promoviendo una intervención inmunológica eficaz en procesos patógenos. Más particularmente, se refiere a composiciones inmunógenas, su naturaleza y el orden, la temporización y la ruta de administración por las que se usan con eficacia.
Descripción de la técnica relacionada
Precognición del Complejo Mayor de Histocompatibilidad y Linfocitos T Diana
Los linfocitos T (células T) son células inmunes específicas de antígeno que funcionan en respuesta a señales específicas de antígeno. Los linfocitos B y los anticuerpos que producen son también entidades específicas de antígeno. Sin embargo, a diferencia de los linfocitos B, los linfocitos T no responden a los antígenos que se encuentran en forma libre o soluble. Para que un linfocito T responda a un antígeno se requiere que el antígeno esté ligado a un complejo de presentación conocido como el complejo mayor de histocompatibilidad (MHC).
Las proteínas del MHC proporcionan los medios por los cuales los linfocitos T diferencian a las células naturales o "propias" de las células ajenas. Las moléculas MHC son una categoría de receptores inmunes que presentan epítopos peptídicos potenciales que son controlados posteriormente por los linfocitos T. Hay dos tipos de MHC, MHC clase I y MHC clase II. Los linfocitos T CD4+ se relacionan con las proteínas del MHC clase II y predominantemente tienen un fenotipo de ayudante mientras que los linfocitos T CD8+ se relacionan con las proteínas de MHC clase I y predominantemente tienen un fenotipo citolítico, pero cada uno de ellos también puede mostrar funciones reguladoras, particularmente depresivas. Ambos MHC son proteínas transmembrana estando la mayor parte de su estructura en la superficie externa de la célula. Además, ambas clases de MHC tienen un sitio de unión de péptido en sus partes externas. Es en este sitio en el que los pequeños fragmentos de proteínas, naturales o ajenos, se unen y se presentan al ambiente extracelular.
Las células llamadas células presentadoras de antígenos (APC, por sus siglas en inglés "antigen presenting cells") muestran antígenos frente a los linfocitos T usando el MHC. Los linfocitos T pueden reconocer a un antígeno, si está presentado en el MHC. Este requerimiento se llama restricción del MHC. Si no se muestra un antígeno por un MHC reconocible, el linfocito T no reconocerá y no actuará en la señal del antígeno. Los linfocitos T específicos para el péptido unido a MHC reconocible se unen a estos complejos de MHC-péptido y proceden en las siguientes etapas de la respuesta inmune.
Los péptidos correspondientes a epítopos restringidos nominales a MHC clase I o clase II están entre las formas más simples de antígeno que pueden administrarse para la inducción, amplificación u otra manipulación de la respuesta de los linfocitos T. A pesar de que se ha demostrado que los epítopos peptídicos son eficaces in vitro en la re-estimulación de líneas de linfocitos T cebadas in vivo, clones, o hibridomas de linfocitos T, su eficacia in vivo es muy limitada. Esto es debido a dos factores principales:
Resumen de la invención
La solicitud de patente internacional WO 01/30382 A1 se refiere a métodos para inducir y/o realzar las respuestas inmunes respecto a antígenos de tumores administrando el antígeno del tumor o el ácido nucleico que lo codifica directamente en un sitio linfático. El ejemplo de este documento de la técnica anterior describe un método para inducir una respuesta inmune que comprende administrar a un sitio linfático en un mono, una primera composición que comprende un vector ALVAC que codifica gp100 seguido de una inyección de refuerzo de un péptido gp100 modificado después de 14 días. La referencia describe que el vector ALVAC usado es un vector basado en el virus de la viruela del canario atenuado.
La solicitud de patente internacional WO 98/58956 A2 se refiere a métodos para inducir respuestas inmunes contra antígenos usando un virus para cebar la inmunización y péptidos de antígeno combinados con un adyuvante para la inmunización reforzadora. La solicitud de patente internacional WO 03/011331 A se refiere a un método para inducir una respuesta CTL específica pero universal a una pluralidad de epítopos, en la que se usan constructos de poliepítopo en la fase de cebado de un régimen de vacunación, pero en la que se usan inmunógenos que codifican o comprenden los epítopos individualmente para la fase de refuerzo.
Las realizaciones de la presente invención incluyen composiciones para la manipulación, y en particular para la inducción, entrada y/o amplificación de la respuesta inmune a los epítopos restringidos de MHC clase I y a su uso para la profilaxis de una terapia de infecciones o enfermedades neoplásicas.
Algunas realizaciones están relacionadas con el uso médico de la composición que comprende administrar a un mamífero una primera composición que incluye un inmunógeno, el inmunógeno codifica al menos una parte de un primer antígeno; y administrar una segunda composición, que incluye un péptido de amplificación, directamente al sistema linfático del mamífero, en el que el péptido corresponde a un epítopo de dicho primer antígeno, en el que la primera composición y la segunda composición no son iguales, en el que la primera composición comprende un plásmido no replicante que codifica un inmunógeno y además comprende un inmunopotenciador, y en el que la primera composición se administra al menos dos veces en un curso de uno hasta aproximadamente siete días o como una infusión continua que tiene una duración de entre aproximadamente 8 horas hasta aproximadamente siete días. Los métodos pueden incluir además la etapa de obtener, analizar o detectar y provocar la respuesta de los linfocitos T.
La primera composición puede incluir un ácido nucleico que codifica el antígeno o su fragmento inmunógeno. La primera composición puede incluir un ácido nucleico capaz de expresar el epítopo en un pAPC. La primera composición puede incluir un polipéptido inmunógeno y un inmunopotenciador, por ejemplo. El inmunopotenciador puede ser una citoquina, un ligando del receptor del tipo Toll, y otros similares. El adyuvante puede incluir una secuencia inmunoestimuladora, un ARN y otros similares.
El polipéptido inmunógeno puede ser dicho péptido amplificante. El polipéptido inmunógeno puede ser dicho primer antígeno. El polipéptido inmunógeno puede administrarse como un componente de un protozoo, bacteria, virus, vector viral, o partícula de tipo vírica, o similares. El adyuvante puede administrarse como un componente de un protozoo, bacteria, virus, vector viral o partícula de tipo vírica, o similares. La segunda composición puede estar sin adyuvante y sin inmunopotenciador. La etapa de administración incluye la administración directa al sistema linfático del mamífero. Las administraciones directas al sistema linfático del mamífero pueden incluir la administración directa a un nodo de linfa o vaso de linfa. La administración directa puede ser a dos o más nodos de linfa o vasos de linfa. El nodo de linfa puede ser, por ejemplo, nodos...
Reivindicaciones:
1. El uso de una composición de entrada que se administra directamente al sistema linfático de un mamífero, comprendiendo dicha composición de entrada un plásmido no replicante que codifica un inmunógeno y que comprende además un inmunopotenciador, comprendiendo el inmunógeno un antígeno o su fragmento inmunógeno; y una composición de amplificación que se administra directamente al sistema linfático del mamífero, comprendiendo dicha composición de amplificación un péptido de amplificación, en el que el péptido corresponde a un epítopo de dicho antígeno, en el que la composición de entrada y la composición de amplificación no son iguales, y en el que la composición de entrada se administra al menos dos veces, en un curso de uno hasta aproximadamente siete días o como una infusión continua que tiene una duración de entre aproximadamente 8 horas hasta aproximadamente 7 días para la fabricación de un medicamento de combinación de inmunización para la profilaxis o la terapia de enfermedades infecciosas o neoplásicas.
2. El uso de la reivindicación 1, en el que el inmunopotenciador es una citoquina.
3. El uso de la reivindicación 1, en el que el inmunopotenciador es un ligando del receptor del tipo Toll.
4. El uso de la reivindicación 3, en el que el inmunopotenciador comprende una secuencia inmunoestimuladora.
5. El uso de la reivindicación 3, en el que el inmunopotenciador comprende ARN.
6. El uso de la reivindicación 1, en el que la composición de amplificación está libre de inmunopotenciador.
7. El uso de la reivindicación 1, en el que la administración directa al sistema linfático del mamífero comprende la administración directa a un nodo de linfa o vaso de linfa.
8. El uso de la reivindicación 7, en el que la administración directa es a dos o más nodos de linfa o vasos de linfa.
9. El uso de la reivindicación 7, en el que el nodo de linfa es seleccionado de un grupo que consiste en nodos de linfa inguinales, axiliares, cervicales y tonsilares.
10. El uso de la reivindicación 1, en el que la administración de entrada y amplificación de composiciones produce una respuesta de linfocitos T efectores frente al antígeno.
11. El uso de la reivindicación 10, en el que la respuesta del linfocito T efector comprende la producción de una citoquina pro-inflamatoria.
12. El uso de la reivindicación 11, en el que la citoquina es γ-IFN o TNFα.
13. El uso de la reivindicación 10, en el que la respuesta del linfocito T efector comprende la producción de una quimioquina de linfocitos T.
14. El uso de la reivindicación 13, en el que la quimioquina es RANTES o MIP-1a.
15. El uso de la reivindicación 1, en el que el epítopo es un epítopo constitutivo.
16. El uso de la reivindicación 1, en el que el epítopo es un epítopo inmune.
17. El uso de la reivindicación 1, en el que la etapa de entrega o la etapa de administración comprenden una inyección de un solo bolo.
18. El uso de la reivindicación 1, en el que la etapa de entrega o la etapa de administración comprenden inyecciones de bolo repetidas.
19. El uso de la reivindicación 1, en el que la etapa de administración comprende una infusión continua.
20. El uso de la reivindicación 19, en el que la infusión tiene una duración de entre aproximadamente 8 horas hasta aproximadamente 7 días.
21. El uso de la reivindicación 1 que tiene un intervalo entre la terminación de la etapa de administración y el principio de la etapa de administración, en el que el intervalo es al menos aproximadamente siete días.
22. El uso de la reivindicación 21, en el que el intervalo está entre aproximadamente 7 y aproximadamente 14 días.
23. El uso de la reivindicación 21, en el que el intervalo es a lo largo de aproximadamente 75 días.
24. El uso de la reivindicación 1, en el que el antígeno es un antígeno asociado a la enfermedad.
25. El uso de la reivindicación 24, en el que el antígeno asociado a la enfermedad es un antígeno asociado a un tumor.
26. El uso de la reivindicación 24, en el que el antígeno asociado a la enfermedad es un antígeno asociado a un patógeno.
27. El uso de la reivindicación 1, en el que el antígeno es un antígeno asociado a una diana.
28. El uso de la reivindicación 27, en el que la diana es una célula neoplásica.
29. El uso de la reivindicación 27, en el que la diana es una célula infectada por un patógeno.
30. El uso de la reivindicación 29, en el que la célula infectada por el patógeno es infectada por un protozoo, una bacteria, unos hongos, un virus o un prión.
31. El uso de la reivindicación 10, en el que la respuesta del linfocito T efector es detectada por al menos un indicador seleccionado del grupo que consiste en un ensayo de citoquina, un ensayo de Elispot, un ensayo de citotoxicidad, un ensayo de tetrámero, una respuesta DTH, una respuesta clínica, el encogimiento del tumor, el aclaramiento del tumor, la inhibición de la progresión del tumor, un menor título del patógeno, el aclaramiento del patógena y la mejora de un síntoma de la enfermedad.
32. El uso de la reivindicación 10, en el que la respuesta del linfocito T efector es una respuesta de un linfocito T citotóxico.
33. El uso de la reivindicación 1, en el que la composición amplificante se administra en uno o varios tiempos.
34. Un juego de composiciones inmunógenas que comprenden una composición de entrada y amplificación, en el que la composición de entrada comprende un plásmido no replicante que codifica un inmunógeno y además comprende un inmunopotenciador, comprendiendo el inmunógeno un antígeno o su fragmento inmunógeno; y en el que la composición de amplificación comprende un péptido de amplificación, en el que el péptido corresponde a un epítopo de dicho antígeno, en el que la composición de entrada y la composición de amplificación no son iguales, para la profilaxis o la terapia de enfermedades infecciosas o neoplásicas en la administración de las composiciones directamente al sistema linfático de dicho mamífero, en el que la composición de entrada se administra al menos dos veces en un curso de uno hasta aproximadamente siete días con una infusión continua que tiene una duración de entre aproximadamente 8 horas hasta aproximadamente siete días.
35. El juego de la reivindicación 34, en el que el plásmido que codifica el inmunógeno comprende además una secuencia inmunoestimuladora que sirve como un agente inmunopotenciador.
36. El juego de la reivindicación 35, en el que el agente inmunopotenciador es seleccionado del grupo que consiste en un ligando de TLR, una secuencia inmunoestimuladora, un ADN que contiene CpG, un dsRNA, un ligando endocítico del Receptor de Reconocimiento de Patrones (PRR), un LPS, una madera de Panamá, tucaresol y una citoquina pro-inflamatoria.
37. El juego de la reivindicación 34 en el que el juego comprende 1-6 dosis de la composición de entrada.
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]