VACUNA CONTRA EL VIRUS DE LA HEPATITIS C.
Ácido nucleico que comprende:
(a)una secuencia de nucleótidos codificante de un polipéptido Met-NS3-NS4A-NS4B-NS5A-NS5B que presenta una identidad de aminoácidos respecto a la secuencia SEC ID nº 1 de por lo menos 85%,
con la condición de que dicho polipéptido presente actividad de proteasa suficiente para procesarse a sí mismo para producir una proteína NS5B, y dicha proteína NS5B sea enzimáticamente activa, en el que dicho ácido nucleico es un vector de expresión que puede expresar dicho polipéptido a partir de dicha secuencia de nucleótidos en una célula humana; o
(b)un casete de expresión génica que puede expresar un polipéptido Met-NS3-NS4A-NS4B-NS5A-NS5B que presenta una identidad de aminoácidos respecto a la secuencia SEC ID nº 1 de por lo menos 85% en una célula humana, con la condición de que dicho polipéptido pueda procesarse a sí mismo para producir una proteína NS5B y dicha proteína NS5B sea enzimáticamente inactiva, comprendiendo dicho casete de expresión:
a)un promotor acoplado transcripcionalmente a una secuencia de nucleótidos codificante de dicho polipéptido;
b)un sitio 5'' de unión ribosómica acoplado funcionalmente a dicha secuencia de nucleótidos,
c)un terminador unido al extremo 3'' de dicha secuencia de nucleótidos, y
d)una señal 3'' de poliadenilación acoplada funcionalmente a dicha secuencia de nucleótidos
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/32512.
Solicitante: MERCK SHARP & DOHME CORP.
ISTITUTO DI RICERCHE DI BIOLOGIA MOLECOLARE P. ANGELETTI S.P.A.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 126 EAST LINCOLN AVENUE,RAHWAY, NJ 07065.
Inventor/es: BETT, ANDREW, J., SHIVER, JOHN, W., NICOSIA, ALFREDO, LAHM, ARMIN, CORTESE, RICCARDO, EMINI, EMILIO, A., LUZZAGO, ALESSANDRA, COLLOCA,STEFANO, KASLOW,DAVID,C.
Fecha de Publicación: .
Fecha Concesión Europea: 12 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07K14/18F4
- C12N15/861 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores adenovirales.
Clasificación PCT:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/40 C12N 15/00 […] › Proteínas de virus ARN, p. ej. Flavivirus.
- C12N15/51 C12N 15/00 […] › Virus de la hepatitis.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12N15/861 C12N 15/00 […] › Vectores adenovirales.
Clasificación antigua:
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/40 C12N 15/00 […] › Proteínas de virus ARN, p. ej. Flavivirus.
- C12N15/51 C12N 15/00 […] › Virus de la hepatitis.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- C12N15/861 C12N 15/00 […] › Vectores adenovirales.
Fragmento de la descripción:
Vacuna contra el virus de la hepatitis C.
Antecedentes de la invención
Las referencias citadas en la presente solicitud no son admitidas como técnica anterior respecto a la invención reivindicada.
Aproximadamente 3% de la población mundial se encuentra infectada por el virus de la hepatitis C (VHC) (Wasley et al., Semin. Liver Dis. 20:1-16, 2000). La exposición al VHC resulta en una enfermedad aguda manifiesta en un pequeño porcentaje de los casos, mientras que en la mayoría de casos, el virus establece una infección crónica que provoca inflamación del hígado y que progresa lentamente hasta la insuficiencia cardiaca y cirrosis (Iwarson, FEMS Microbiol. Rev. 14:201-204, 1994). Además, los estudios epidemiológicos indican que el VHC presenta un papel importante en la patogénesis del carcinoma hepatocelular (Kew, FEMS Microbiol. Rev. 14:211-220, 1994; Alter, Blood 85:1681-1695, 1995).
Antes de la implementación del cribado rutinario de sangre para el VHC en 1992, la mayoría de las infecciones se contraían por la exposición involuntaria a sangre contaminada, productos sanguíneos u órganos trasplantados. En aquellas áreas en las que se ha llevado a cabo el cribado de la sangre para el VHC, el VHC se contrae mediante la exposición percutánea directa a sangre infectada, es decir, la utilización intravenosa de drogas. Entre los métodos menos frecuentes de transmisión se incluyen la exposición perinatal, la hemodiálisis y el contacto sexual con una persona infectada por VHC (Alter et al., N. Engl. J. Med. 341(8):556-562, 1999; Alter, J. Hepatol. 31 supl. 88-91, 1999; Semin. Liver Dis. 201:1-16, 2000).
El genoma del VHC consta de un ARN de una cadena de aproximadamente 9,5 kb codificante de una poliproteína precursora de aproximadamente 3.000 aminoácidos (Choo et al., Science 244:362-364, 1989; Choo et al., Science 244:359-362, 1989; Takamizawa et al., J. Virol. 65:1105-1113, 1991). La poliproteína del VHC contiene las proteínas víricas en el orden siguiente: C-E1-E2-p7-NS2-NS3-NS4A-NS4B-NS5A-NS5B.
Las proteínas víricas individuales se producen mediante proteolisis de la poliproteína del VHC. Las proteasas de la célula huésped liberan las proteínas estructurales putativas C, E1, E2 y p7, y crean el extremo N-terminal de NS2 en el aminoácido 810 (Mizushima et al., J. Virol. 68:2731-2734, 1994; Hijikata et al., P.N.A.S. USA 90:10773-10777, 1993).
Las proteínas no estructurales NS3, NS4A, NS4B, NS5A y NS5B presumiblemente forman la maquinaria replicativa del virus y resultan liberadas de la poliproteína. Una proteína dependiente de cinc asociada a NS2 y el extremo N-terminal de NS3 son responsables del corte entre NS2 y NS3 (Grakoui et al., J. Virol. 67:1385-1395, 1993; Hijikata et al., P.N.A.S. USA 90:10773-10777, 1993). Una serina proteasa determinada que se localiza en el dominio N-terminal de NS3 es responsable de los cortes proteolíticos en las uniones NS3/NS4A, NS4A/NS4B, NS4B/NSSA y NS5A/NS5B (Bartenschlager et al., J. Virol. 67:3835-3844, 1993; Grakoui et al., Proc. Natl. Acad. Sci. USA 90:10583-10587, 1993; Tomei et al., J. Virol. 67:4017-4026, 1993). NS4A proporciona un cofactor para la actividad de NS3 (Failla et al., J. Virol. 68:3753-3760, 1994; De Francesco et al., patente US nº 5.739.002).
La NS5A es una proteína altamente fosforilada que proporciona resistencia al interferón (De Francesco et al., Semin. Liver Dis. 20(1):69-83, 2000; Pawlotsky, Viral Hepat. Supl. 1:47-48, 1999).
La NS5B proporciona una ARN polimerasa dependiente de ARN (De Francesco et al., publicación internacional número WO 96/37619; Behrens et al., EMBO 15:12-22, 1996; Lohmann et al., Virology 249:108-118, 1998).
Sumario de la invención
La presente invención proporciona un ácido nucleico que comprende:
El ácido nucleico resulta particularmente útil como componente de un adenovector o vacuna de plásmido de ADN que proporciona un amplio abanico de antígenos para generar una respuesta inmunológica contra el VHC mediada por células (CMI) específica para el VHC.
Una respuesta CMI específica para el VHC se refiere a la producción de linfocitos T citotóxicos y células T ayudante que reconocen un antígeno del VHC. La respuesta CMI también puede incluir efectos inmunológicos no específicos del VHC.
La referencia a una "secuencia sustancialmente similar" indica una identidad de por lo menos aproximadamente 85% respecto a una secuencia de referencia. De esta manera, por ejemplo, los polipéptidos que presentan una secuencia de aminoácidos sustancialmente similar a la secuencia SEC ID nº 1 presentan una identidad de secuencia global de por lo menos aproximadamente 85% respecto a la secuencia SEC ID nº 1.
Los polipéptidos correspondientes a NS3, NS4A, NS4B, NS5A y NS5B presentan una identidad de secuencia de aminoácidos de por lo menos aproximadamente 85% respecto a la región correspondiente en la secuencia SEC ID nº 1. Dichos polipéptidos correspondientes también se denominan en la presente memoria polipéptidos NS3, NS4A, NS4B, NS5A y NS5B.
La expresión en el interior de una célula humana presenta aplicaciones terapéuticas para el tratamiento activo de una infección por VHC y para el tratamiento profiláctico contra una infección por VHC.
Un vector de expresión contiene una secuencia de nucleótidos codificante de un polipéptido conjuntamente con elementos reguladores para la transcripción y procesamiento correctos. Entre los elementos reguladores que pueden encontrarse presentes se incluyen los asociados naturalmente a la secuencia de nucleótidos codificante del polipéptido, y elementos reguladores exógenos no asociados naturalmente a la secuencia de nucleótidos. Los elementos reguladores exógenos, tales como un promotor exógeno, pueden resultar útiles para la expresión en un huésped particular, tal como en una célula humana. Entre los elementos reguladores que resultan útiles para la expresión funcional se incluyen un promotor, un terminador, un sitio de unión ribosómica y una señal de poliadenilación.
La expresión "acoplado transcripcionalmente" se refiere a que el promotor se encuentra situado de manera que la transcripción de la secuencia de nucleótidos puede resultar inducida por la unión de la ARN polimerasa al promotor. El acoplamiento transcripcional no requiere que la secuencia que se transcribe sea contigua al promotor.
La expresión "funcionalmente acoplado" se refiere a la capacidad de mediar en un efecto sobre la secuencia de nucleótidos. El acoplamiento funcional no requiere que las secuencias acopladas sean contiguas entre sí. Una señal de poliadenilación 3' funcionalmente acoplada a la secuencia de nucleótidos facilita el corte y poliadenilación del ARN transcrito. Un sitio de unión ribosómica 5' funcionalmente acoplado a la secuencia de nucleótidos...
Reivindicaciones:
1. Ácido nucleico que comprende:
2. Ácido nucleico según la reivindicación 1, que comprende: una secuencia de nucleótidos codificante de un polipéptido Met-NS3-NS4A-NS4B-NS5A-NS5B que presenta una identidad de aminoácidos respecto a la secuencia SEC ID nº 1 de por lo menos 85%, con la condición de que dicho polipéptido presente actividad de proteasa suficiente para procesarse a sí mismo para producir una proteína NS5B, y dicha proteína NS5B sea enzimáticamente inactiva, en el que dicho ácido nucleico es un vector de expresión que puede expresar dicho polipéptido a partir de dicha secuencia de nucleótidos en una célula humana.
3. Ácido nucleico según la reivindicación 1, que comprende: una secuencia de nucleótidos codificante de un polipéptido Met-NS3-NS4A-NS4B-NS5A-NS5B que presenta una identidad de aminoácidos respecto a la secuencia SEC ID nº 1 de por lo menos 95%, en la que la secuencia de dicho polipéptido mantiene la mayoría o la totalidad de las regiones antigénicas de células T de secuencia SEC ID nº 1, con la condición de que dicho polipéptido presente actividad de proteasa suficiente para procesarse a sí mismo para producir una proteína NS5B, y dicha proteína NS5B sea enzimáticamente inactiva, en el que dicho ácido nucleico es un vector de expresión que puede expresar dicho polipéptido a partir de dicha secuencia de nucleótidos en una célula humana.
4. Ácido nucleico según la reivindicación 1, que comprende: un ácido nucleico que comprende un casete de expresión génica que puede expresar un polipéptido Met-NS3-NS4A-NS4B-NS5A-NS5B que presenta una identidad de aminoácidos respecto a la secuencia SEC ID nº 1 de por lo menos 95% en una célula humana, con la condición de que dicho polipéptido pueda procesarse a sí mismo para producir una proteína NS5B y dicha proteína NS5B sea enzimáticamente inactiva, comprendiendo dicho casete de expresión:
5. Ácido nucleico según la reivindicación 4, en el que dicha secuencia de nucleótidos presenta una identidad respecto a la secuencia codificante de la secuencia SEC ID nº 2 de por lo menos 65%.
6. Ácido nucleico según la reivindicación 4 ó 5, en el que dicho ácido nucleico es un plásmido adecuado para la administración en un ser humano y comprende además un origen de replicación procariótico y un gen codificante de un marcador seleccionable.
7. Ácido nucleico según la reivindicación 4 ó 5, en el que dicho ácido nucleico es un adenovector constituido por lo siguiente:
8. Ácido nucleico según la reivindicación 7, en el que dicho casete de expresión se encuentra en una orientación antiparalela a E1.
9. Ácido nucleico según la reivindicación 4 ó 5, en el que dicho ácido nucleico es un adenovector constituido por lo siguiente:
10. Ácido nucleico según la reivindicación 7, 8 ó 9, en el que dicha primera región corresponde a Ad5, dicha segunda región corresponde a Ad5, dicha tercera región corresponde a Ad5, dicha cuarta región corresponde a Ad5, y dicha quinta región corresponde a Ad5.
11. Ácido nucleico según la reivindicación 7, 8 ó 9, en el que dicha primera región corresponde a Ad5 o a Ad6, dicha segunda región corresponde a Ad5 o a Ad6, dicha tercera región corresponde a Ad6, dicha cuarta región corresponde a Ad6, y dicha quinta región corresponde a Ad5 o a Ad6.
12. Ácido nucleico según cualquiera de las reivindicaciones 4 a 11, en el que dicho promotor es el promotor intermedio-temprano de citomegalovirus humano, dicho sitio 5' de unión ribosómica está constituido por la secuencia SEC ID nº 12, y dicha señal 3' de poliadenilación es la señal de poliadenilación de BGH.
13. Ácido nucleico según cualquiera de las reivindicaciones anteriores, que codifica el polipéptido de secuencia SEC ID nº 1.
14. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que el polipéptido difiere de la secuencia SEC ID nº 1 en 1 a 20 aminoácidos.
15. Ácido nucleico según la reivindicación 14, en el que el polipéptido difiere de la secuencia SEC ID nº 1 en 1 a 5 aminoácidos.
16. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que la secuencia de nucleótidos es la secuencia codificante de la secuencia SEC ID nº 2.
17. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que la secuencia de nucleótidos es la secuencia codificante de la secuencia SEC ID nº 3.
18. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que la secuencia de nucleótidos es la secuencia codificante de la secuencia SEC ID nº 10.
19. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que la secuencia de nucleótidos es la secuencia codificante de la secuencia SEC ID nº 11.
20. Ácido nucleico según cualquiera de las reivindicaciones 1 a 12, en el que la secuencia de nucleótidos es la secuencia codificante de la secuencia SEC ID nº 2 o difiere de la secuencia SEC ID nº 2 en 1 a 50 nucleótidos.
21. Ácido nucleico según la reivindicación 5, en el que dicho ácido nucleico es un adenovector constituido por una secuencia de nucleótidos que presenta una identidad respecto a SEC ID nº 4 de por lo menos 65%, o un derivado de la misma, en el que dicho derivado de la misma presenta la sustitución de la secuencia codificante de la poliproteína de VHC presente en SEC ID nº 4 por la secuencia codificante de la poliproteína de VHC de SEC ID nº 3, SEC ID nº 10 o SEC ID nº 11.
22. Adenovector constituido por la secuencia de ácidos nucleicos de SEC ID nº 4 o un derivado de la misma, en el que dicho derivado de la misma presenta la sustitución de la secuencia codificante de la poliproteína de VHC presente en SEC ID nº 4 por la secuencia codificante de la poliproteína de VHC de SEC ID nº 3, SEC ID nº 10 o SEC ID nº 11.
23. Composición farmacéutica que comprende el ácido nucleico según cualquiera de las reivindicaciones 2 a 3 y 6 a 22, y un portador farmacéuticamente aceptable.
24. Ácido nucleico según cualquiera de las reivindicaciones 2 a 3 y 6 a 22, que es un adenovector para la utilización en un método de tratamiento de un ser humano mediante terapia.
25. Ácido nucleico según la reivindicación 24, para la utilización en el tratamiento o la prevención de VHC.
26. Utilización de un ácido nucleico según cualquiera de las reivindicaciones 2 a 3 y 6 a 22 para la preparación de un medicamento destinado al tratamiento o la prevención del VHC en un ser humano.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Composiciones y métodos para la expresión de ARNs de guía de CRISPR utilizando el promotor de H1, del 29 de Enero de 2020, de THE JOHNS HOPKINS UNIVERSITY: Un sistema CRISPR-Cas no natural que comprende un vector que comprende un promotor H1 bidireccional, en donde el promotor de H1 bidireccional comprende: a) elementos […]
Métodos y composiciones para tratar depósitos amiloides, del 22 de Enero de 2020, de UNIVERSITY OF IOWA RESEARCH FOUNDATION: Una partícula de rAAV2 que comprende una proteína de la cápside de AAV2 y un vector que comprende un ácido nucleico que codifica para una […]
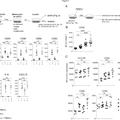 Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Adenovirus que expresan antígenos oncógenos heterólogos, del 4 de Septiembre de 2019, de BOARD OF REGENTS THE UNIVERSITY OF TEXAS SYSTEM: Un adenovirus oncolítico recombinante que tiene un genoma que comprende una o más secuencias de ácido nucleico heterólogas que codifican un antígeno oncógeno, […]
Vector de virus adenoasociado, del 28 de Agosto de 2019, de KING'S COLLEGE LONDON: Un vector de virus adenoasociado (AAV) recombinante que comprende: (a) una proteína de la cápside del AAV2 variante, en el que la proteína de la cápside del AAV2 variante […]
Mutantes de E1A y E1B de adenovirus selectivos de tumor, del 10 de Julio de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un adenovirus recombinante que comprende una secuencia de ADN que se inserta en un sitio de inserción de E1b- 19K, en el que dicho sitio de inserción […]
Procedimiento novedoso y composiciones, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Uno o más primeros polipéptidos inmunógenos para su uso en un procedimiento de generación de una respuesta inmunológica frente a Mycobacterium spp., en los […]