MEZCLAS MONODISPERSAS DE CONJUGADOS DE FARMACO DE CALCITONINA CON OLIGOMERO QUE COMPRENDE POLIETILENGLICOL, SUS USOS, Y METODO PARA OBTENERLAS.
Una mezcla monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular,
una mezcla sustancial y puramente monodispersa de conjugados en la que al menos alrededor de 95 por ciento de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular, o una mezcla puramente monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular;
en la que los conjugados comprenden calcitonina de salmón acoplada a un primer oligómero y a un segundo oligómero;
en la que cada oligómero comprende un resto de polietilenglicol que tiene 2, 3, 4, 5, 6, 7 u 8 subunidades de polietilenglicol y uno o más restos lipófilos;
en la que el uno o más restos lipófilos se seleccionan de un resto alquilo lineal, saturado o insaturado que tiene 1 a 28 átomos de carbono, y un resto de ácido graso lineal, saturado o insaturado que tiene 2 a 18 átomos de carbono;
en la que el primer oligómero está acoplado covalentemente a una función amina de Lys11 de la calcitonina de salmón, y el segundo oligómero está acoplado covalentemente a una función amina de Lys18 de la calcitonina de salmón
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/17575.
Solicitante: BIOCON LIMITED.
Nacionalidad solicitante: India.
Dirección: 20TH K.M. HOSUR ROAD, ELECTRONICS CITY P.O.,BANGALORE 560 100 KARNATAKA.
Inventor/es: EKWURIBE, NNOCHIRI, N., PRICE, CHRISTOPHER, H., ANSARI, ASLAM, M., ODENBAUGH, AMY, L.
Fecha de Publicación: .
Fecha Concesión Europea: 6 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K47/48H4P
- C07K14/585 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Calcitoninas.
Clasificación PCT:
- A61K38/23 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Calcitoninas.
- A61K47/48
- A61P19/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para la osteoporosis.
- C07K14/585 C07K 14/00 […] › Calcitoninas.
Clasificación antigua:
- A61K38/23 A61K 38/00 […] › Calcitoninas.
- C07K14/585 C07K 14/00 […] › Calcitoninas.
Fragmento de la descripción:
Mezclas monodispersas de conjugados de fármaco de calcitonina con oligómero que comprende polietilenglicol, sus usos, y métodos para obtenerlas.
Campo de la invención
La presente invención se refiere a conjugados de fármaco con oligómero, y, más particularmente, a conjugados de fármaco de calcitonina con oligómero.
Antecedentes de la invención
La calcitonina es una hormona de origen natural con una semivida corta que se cree que actúa directamente sobre osteoclastos (vía receptores sobre la superficie celular para calcitonina). Esta acción puede inhibir directamente la resorción ósea osteoclástica, lo que puede conducir a efectos séricos hipocalcémicos y/o hipofosfatémicos. La calcitonina puede ser útil para tratar diversos trastornos óseos, incluyendo osteoporosis y enfermedad de Paget.
La osteoporosis es una osteopatía en la que el tejido óseo se mineraliza normalmente, pero la cantidad de hueso disminuye y la integridad estructural del hueso trabecular se ve alterada. El hueso cortical se hace más poroso y más delgado. Esto hace al hueso más débil y más tendente a la fractura. En los Estados Unidos de América, alrededor de 21% de mujeres postmenopáusicas tienen osteoporosis (baja densidad ósea), y alrededor de 16% han tenido una fractura. En mujeres mayores de 80, alrededor de 40% han experimentado una fractura de la cadera, vértebras, brazo, o pelvis. La población de hombres y mujeres ancianos está aumentando, y por lo tanto el número de personas con osteoporosis está aumentando.
La calcitonina, dada como una inyección subcutánea, ha mostrado mejoras significativas en la densidad ósea; sin embargo, se ha dado a conocer una incidencia elevada de efectos secundarios, incluyendo dolor en el sitio de la inyección, sofoco y náusea, lo que puede limitar el uso del fármaco.
La enfermedad de Paget del hueso es un trastorno óseo metabólico de origen desconocido que normalmente afecta a personas ancianas. La enfermedad provoca una formación incrementada e irregular de hueso a medida que los osteocitos, que son responsables de disolver el hueso viejo del cuerpo y sustituirlo por nuevo, pierden el control. Durante un período de tiempo, el nuevo hueso deformado se hace más grande, más débil, y tiene más vasos sanguíneos que el hueso normal. A diferencia del hueso normal, la estructura es irregular y consecuentemente más débil, lo que hace que tenga tendencia a la fractura incluso después de una pequeña lesión.
En la forma más leve, la enfermedad no tiene síntomas. En casos más graves, el dolor puede ser intenso. La progresión imparable de la enfermedad puede hacer que los huesos se arqueen, el cráneo puede aumentar de tamaño, y la médula espinal se puede curvar. A medida que los huesos se agrandan, pueden provocar presión en los nervios cercanos, lo que puede dar como resultado debilidad muscular. En el caso de un grave agrandamiento del cráneo, esta presión puede dar como resultado sordera, metamorfopsia, mareos y acúfenos.
La calcitonina puede ser eficaz tratando trastornos de la remodelación esquelética incrementada, tal como enfermedad de Paget. En el tratamiento de la enfermedad de Paget, el uso crónico de calcitonina puede producir una reducción de los síntomas a largo plazo; sin embargo, los efectos secundarios de la administración de calcitonina pueden incluir náusea, hinchamiento de las manos, urticaria, y retortijón.
Diversas referencias han propuesto conjugar polipéptidos, tales como calcitonina, con mezclas polidispersas de polietilenglicol o polímeros que contienen polietilenglicol. Por ejemplo, la patente U.S. nº 5.359.030 de Ekwuribe propone conjugar polipéptidos tales como calcitonina con mezclas polidispersas de polímeros glucolipídicos modificados con polietilenglicol, y mezclas polidispersas de polímeros de ácidos grasos modificados con polietilenglicol. Se prefiere que el peso molecular medio numérico del polímero que resulta de cada combinación esté en el intervalo de alrededor de 500 a alrededor de 10.000 Daltons.
La polidispersidad de las mezclas poliméricas y conjugados descritos en Ekwuribe es probablemente el resultado del uso de polietilenglicol polidisperso en la síntesis de polímeros. PEG se produce típicamente mediante polimerización de apertura del anillo de óxido de etileno catalizada por bases. La reacción se inicia añadiendo óxido de etileno a etilenglicol, con hidróxido de potasio como catalizador. Este proceso da como resultado una mezcla polidispersa de polímeros de polietilenglicol que tienen un peso molecular medio numérico en un intervalo dado de pesos moleculares. Por ejemplo, los productos de PEG ofrecidos por Sigma-Aldrich de Milwaukee, Wisconsin, se proporcionan en mezclas polidispersas tales como PEG 400 (Mn 380-420); PEG 1.000 (Mn 950-1.050); PEG 1.500 (Mn 1.400-1.600); y PEG 2.000 (Mn 1.900-2.200).
Higgins et al. (British Journal of Pharmacology, 134, Proceedings Supplement, 2001-11, 53P) describen la bioeficacia de un análogo de calcitonina de salmón conjugado covalentemente a oligómeros anfifílicos.
El documento WO 97/14740 A1 describe el suministro oral de calcitonina mediante conjugación con oligómeros anfifílicos. Los oligómeros anfifílicos consisten en un segmento de polietilenglicol (PEGn, n = de media 7, 8, 9, 12 y 20) y una unidad alquílica o una unidad de azúcar protegido.
Radha Krishnan B. et al. (Proceedings of the Controlled Release Society, 26, 1999, 149-150) describen calcitonina de salmón conjugada con oligómeros anfifílicos que consisten en un segmento de PEG hidrófilo y una unidad alquílica hidrófoba.
La patente US 6.191.105 describe insulina acoplada covalentemente con un polímero que incluye (i) un resto de polialquilenglicol lineal y (ii) un resto lipófilo, en el que la insulina, el resto de polialquilenglicol lineal y el resto lipófilo están dispuestos conformacionalmente en relación entre sí de forma que la insulina en la composición tiene una resistencia in vivo aumentada frente a la degradación enzimática, con relación a la insulina sola.
El documento WO 00/78302 A describe un conjugado de insulina, PEG, y ácido oleico, que se puede administrar oralmente.
El documento WO 00/09073 A describe un compuesto terapéutico conjugado con un oligómero, en el que el oligómero comprende un resto lipófilo acoplado a un resto hidrófilo.
Es deseable proporcionar mezclas no polidispersas de conjugados de fármaco de calcitonina con oligómero en las que el oligómero comprende polietilenglicol.
Sumario de la invención
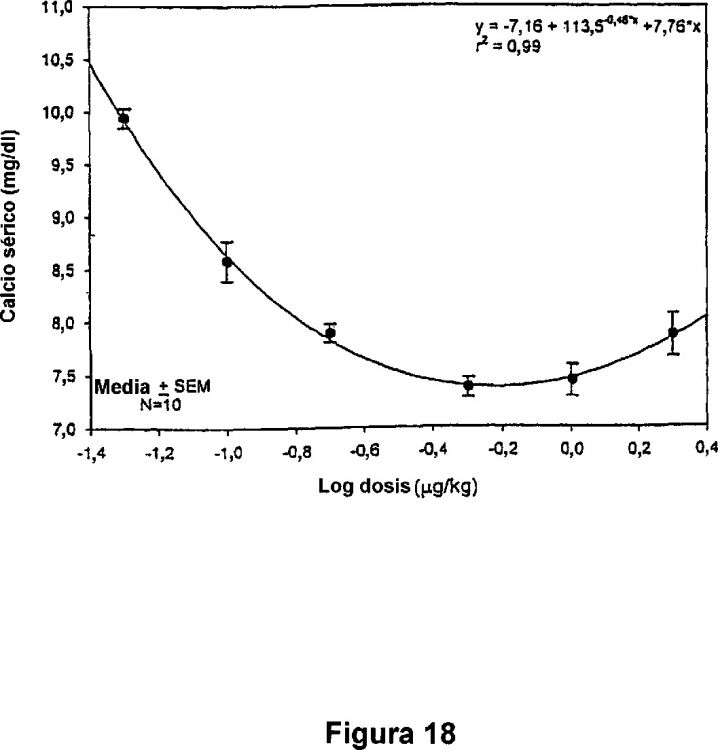
Se ha descubierto inesperadamente que una mezcla de conjugados de fármaco de calcitonina con oligómero que comprende polietilenglicol según realizaciones de la presente invención puede reducir los niveles de calcio sérico en 10, 15 o incluso 20 por ciento o más. Además, una mezcla de conjugados de fármaco de calcitonina con oligómero que comprende polietilenglicol según realizaciones de la presente invención puede ser más eficaz sobreviviendo en un modelo in vitro de digestión intestinal que calcitonina no conjugada. Además, mezclas de conjugados de calcitonina con oligómero que comprende polietilenglicol según realizaciones de la presente invención pueden mostrar una mayor biodisponibilidad que la calcitonina no conjugada.
Según realizaciones de la presente invención, se proporciona una mezcla monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular, una mezcla sustancial y puramente monodispersa de conjugados en la que al menos alrededor de 95 por ciento de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular, o una mezcla puramente monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular;
en la que los conjugados comprenden calcitonina de salmón acoplada a un primer oligómero y a un segundo oligómero;
en la que cada oligómero comprende un resto de polietilenglicol que tiene 2, 3, 4, 5, 6, 7 u 8 subunidades de polietilenglicol y uno o más restos lipófilos;
en la que el uno o más restos lipófilos se seleccionan de un resto alquilo lineal, saturado o insaturado que tiene 1 a 28 átomos de carbono, y un resto de ácido graso lineal, saturado o insaturado que tiene 2 a 18 átomos de carbono;
en la que el primer...
Reivindicaciones:
1. Una mezcla monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular, una mezcla sustancial y puramente monodispersa de conjugados en la que al menos alrededor de 95 por ciento de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular, o una mezcla puramente monodispersa de conjugados en la que alrededor de 100 por cien de los compuestos en la mezcla tienen el mismo peso molecular y tienen la misma estructura molecular;
en la que los conjugados comprenden calcitonina de salmón acoplada a un primer oligómero y a un segundo oligómero;
en la que cada oligómero comprende un resto de polietilenglicol que tiene 2, 3, 4, 5, 6, 7 u 8 subunidades de polietilenglicol y uno o más restos lipófilos;
en la que el uno o más restos lipófilos se seleccionan de un resto alquilo lineal, saturado o insaturado que tiene 1 a 28 átomos de carbono, y un resto de ácido graso lineal, saturado o insaturado que tiene 2 a 18 átomos de carbono;
en la que el primer oligómero está acoplado covalentemente a una función amina de Lys11 de la calcitonina de salmón, y el segundo oligómero está acoplado covalentemente a una función amina de Lys18 de la calcitonina de salmón.
2. La mezcla según la reivindicación 1, en la que la adición del resto de polietilenglicol proporciona características seleccionadas de las siguientes: (a) la capacidad para reducir los niveles de calcio sérico en al menos 5 por ciento, (b) una resistencia aumentada a la degradación por quimiotripsina o tripsina cuando se compara con la resistencia a la degradación por quimiotripsina o tripsina de la calcitonina que no está acoplada al oligómero, (c) una bioeficacia que es mayor que la bioeficacia de la calcitonina que no está acoplada al oligómero, y sus combinaciones.
3. La mezcla según la reivindicación 1, en la que la calcitonina está acoplada covalentemente al oligómero mediante un enlace hidrolizable, un enlace no hidrolizable, o ambos.
4. La mezcla según la reivindicación 1, en la que cada oligómero tiene la misma estructura molecular.
5. Una composición farmacéutica que comprende:
la mezcla según la reivindicación 1; y
un vehículo farmacéuticamente aceptable.
6. Una mezcla sustancialmente monodispersa de conjugados según la reivindicación 1, que comprende calcitonina de salmón acoplada covalentemente en Lys11 de la calcitonina de salmón a un resto de ácido carboxílico de un ácido carboxílico, que está acoplado covalentemente, en el extremo distal al resto de ácido carboxílico, a un resto de polietilenglicol terminado en metilo que tiene al menos 7 subunidades de polietilenglicol, y acoplada covalentemente en Lys18 de la calcitonina de salmón a un resto de ácido carboxílico de un ácido carboxílico, que está acoplado covalentemente, en el extremo distal al resto de ácido carboxílico, a un resto de polietilenglicol terminado en metilo que tiene al menos 7 subunidades de polietilenglicol.
7. La mezcla según la reivindicación 6, en la que los conjugados consisten cada uno en calcitonina de salmón acoplada covalentemente en Lys11 de la calcitonina de salmón a un resto de ácido carboxílico de ácido octanoico, que está acoplado covalentemente, en el extremo distal al resto de ácido carboxílico, a un resto de polietilenglicol terminado en metilo que tiene 7 subunidades de polietilenglicol, y acoplada covalentemente en Lys18 de la calcitonina de salmón a un resto de ácido carboxílico de ácido octanoico, que está acoplado covalentemente, en el extremo distal al resto de ácido carboxílico, a un resto de polietilenglicol terminado en metilo que tiene al menos 7 subunidades de polietilenglicol.
8. Uso de una mezcla de conjugados de cualquiera de las reivindicaciones 1 a 7 para la preparación de un medicamento para el tratamiento de un trastorno óseo caracterizado por una excesiva resorción ósea osteoclástica o efectos séricos hipercalcémicos.
9. Uso según la reivindicación 8, en el que el trastorno óseo es osteoporosis, enfermedad de Paget, o hipercalcemia.
10. Una mezcla de conjugados según la reivindicación 1, en la que cada conjugado comprende una calcitonina acoplada a un oligómero que comprende un resto de polietilenglicol que tiene al menos 4 subunidades de polietilenglicol, teniendo dicha mezcla una distribución de pesos moleculares con una desviación estándar menor que alrededor de 22 Daltons.
11. Una mezcla de conjugados según la reivindicación 1, en la que cada conjugado comprende una calcitonina acoplada a un oligómero que comprende un resto de polietilenglicol,
en la que la mezcla tiene un coeficiente de dispersidad (DC) mayor que 10.000 en el que
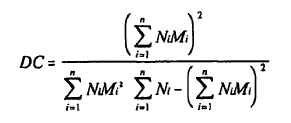
en la que
n es el número de diferentes moléculas en la muestra;
Ni es el número de iª moléculas en la muestra; y
Mi es la masa de la iª molécula.
12. La mezcla de conjugados según la reivindicación 11, en la que el coeficiente de dispersidad es mayor que 100.000.
13. Una mezcla de conjugados según la reivindicación 1, en la que cada conjugado tiene el mismo peso molecular y tiene la estructura de la fórmula:
en la que:
14. Un procedimiento para sintetizar una mezcla monodispersa o una mezcla sustancial y puramente monodispersa o una mezcla puramente monodispersa de conjugados según la reivindicación 1, en la que cada conjugado comprende calcitonina de salmón acoplada a un primer oligómero y a un segundo oligómero, comprendiendo cada oligómero un resto de polietilenglicol que tiene 2, 3, 4, 5, 6, 7 u 8 subunidades de polietilenglicol y uno o más restos lipófilos seleccionados de un resto de alquilo lineal, saturado o insaturado, que tiene 1 a 28 átomos de carbono, y un resto de ácido graso lineal, saturado o insaturado, que tiene 2 a 18 átomos de carbono; comprendiendo dicho procedimiento:
Patentes similares o relacionadas:
Antagonistas peptídicos de la familia calcitonina CGRP de hormonas peptídicas y su uso, del 17 de Junio de 2020, de Soares, Christopher, J: Un antagonista del péptido relacionado con el gen de la calcitonina, o una sal farmacéuticamente aceptable del mismo, teniendo dicho antagonista la estructura […]
Miméticos de la calcitonina para el tratamiento de enfermedades y trastornos, del 9 de Enero de 2019, de KeyBioscience AG: Un péptido que tiene una secuencia de aminoácidos según SEQ ID NO: 38, que está carboxilada opcionalmente en su N-terminal o modificada de otro modo para reducir la carga […]
Antagonistas peptídicos de la familia calcitonina CGRP de hormonas peptídicas y su uso, del 26 de Julio de 2017, de Soares, Christopher, J: Un antagonista del péptido relacionado con el gen de la calcitonina que tiene la estructura de Fórmula I: X1-Y1-Z1 (I), en la que X1 comprende X11-X12-X13-X14-X15-X16-X17 […]
Miméticos de la calcitonina para el tratamiento de enfermedades y trastornos, del 21 de Septiembre de 2016, de KeyBioscience AG: Un péptido que tiene una secuencia de aminoácidos según SEQ ID NO: 43, que está carboxilada opcionalmente en su N-terminal o modificada de otro […]
Proteínas de fusión de albúmina, del 3 de Diciembre de 2014, de NOVOZYMES BIOPHARMA DK A/S: Una proteína de fusión de albúmina que comprende (i) factor IX, o un fragmento o una variante del factor IX, en la que la variante tiene al menos el 75 % de identidad […]
Proteínas de fusión de albúmina, del 4 de Junio de 2014, de NOVOZYMES BIOPHARMA DK A/S: Una proteína de fusión de albúmina que comprende (i) factor VII, o un fragmento o una variante del factor VII, fusionado con el extremo N-terminal de la (ii) […]
Método de escisión de polipéptidos usando un mutante de la proteasa OmpT, del 19 de Marzo de 2013, de DAIICHI SANKYO COMPANY, LIMITED: Un método de escisión de polipéptidos caracterizado porque hay arginina o lisina en la posición P1 de un sitio de escisión deseado en un polipéptido, […]
Epítopos T de antígenos de preprocalcitonina, del 23 de Abril de 2012, de INSTITUT GUSTAVE ROUSSY: Péptido inmunogónico que constituye un epítopo T presentado por CMH I, caracterizado porque se selecciona entre: a) el péptido de secuencia: VLLQAGSLHA (SEQ ID NO: 1) b) […]