METODO PARA PRODUCIR 7-ETIL-10-(4-(1-PIPERIDINO)-1-PIPERIDINO)-CARBONILOXI-CAMPTOTECINA.
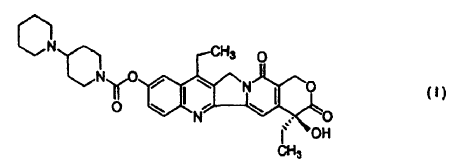
Un método para preparar 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina de fórmula I:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CZ2004/000050.
Solicitante: PLIVA-LACHEMA A.S..
Nacionalidad solicitante: República Checa.
Dirección: KARASEK 1,621 33 BRNO.
Inventor/es: DOBROVOLNY,PETR.
Fecha de Publicación: .
Fecha Concesión Europea: 2 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- C07D491/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 491/00 Compuestos heterocíclicos que contienen en el sistema cíclico condensado, a la vez uno o más ciclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo, y uno o más ciclos que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos en los grupos C07D 451/00 - C07D 459/00, C07D 463/00, C07D 477/00 ó C07D 489/00. › en los que el sistema condensado contiene cuatro o más heterociclos.
Clasificación PCT:
- C07D491/22 C07D 491/00 […] › en los que el sistema condensado contiene cuatro o más heterociclos.
Clasificación antigua:
- C07D491/22 C07D 491/00 […] › en los que el sistema condensado contiene cuatro o más heterociclos.
Descripción:
Método para producir 7-etil-10-[4-(1-piperidino)-1-piperidino]-carboniloxi-camptotecina.
Campo de la invención
Esta invención se refiere a un método para preparar 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina de fórmula I:
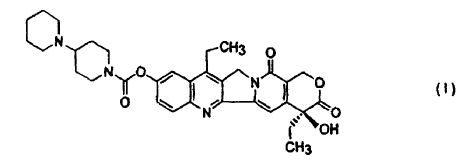
La 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina, que también se conoce como base de irinotecán, se usa para preparar el hidrocloruro de irinotecán trihidratado, citostáticamente activo, un inhibidor de la topoisomerasa que se usa en el tratamiento del cáncer de pulmón y de recto.
Fundamento de la invención
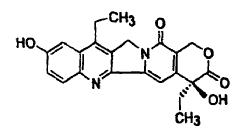
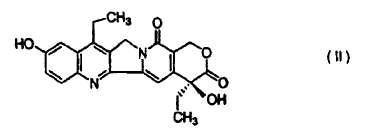
La 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina se ha preparado hasta ahora por condensación de 7-etil-10-hidroxicamptotecina de fórmula:
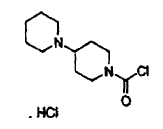
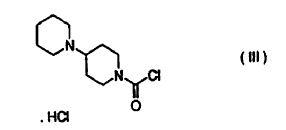
con hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina de fórmula:
en piridina a temperatura ambiente. Este método se ha descrito en las siguientes patentes de EE.UU.: 4.604.463 (T. M. Kanagawa, S. Sawada, K. Nokata, E-Sugino, M. Mutai), expedida el 5 de agosto de 1.986; S. Sawada, S. Okajima, R. Aiyama, K. Nokata, T. Furuta, T. Yokokura, E. Sugino, K. Yamachuchi, T. Miyasaka, Chemical and Pharmaceutical Bulletin 1.991, 39 (6), 1.446-1.454; la patente internacional WO 96/31513 (K. E. Henegar, J. C. Sih), publicada el 10 de octubre de 1.996; la patente de EE.UU. 6.235.907 (K. E. Henegar, J. C. Sih), expedida el 22 de mayo de 2.001; la patente de EE.UU. 6.444.820 (K. E. Henegar, J. C. Sih), expedida el 3 de septiembre de 2.002.
Sin embargo, este método de preparación de base de irinotecán adolece del hecho de que en la condensación se forman impurezas coloreadas que se tienen que retirar por adsorción en una columna de gel de sílice y posterior recristalización de etanol. Estas etapas de purificación van acompañadas de pérdidas sustanciales del producto final y sus rendimientos son sólo aproximadamente el 64%. Por otra parte, el método requiere la destilación de piridina, extracción de una capa de cloroformo con disoluciones de carbonato de sodio y cloruro de sodio y secado de la capa de cloroformo sobre sulfato de magnesio. Por lo tanto, se requería un método de preparación mejor de base de irinotecán. Tal objetivo se ha conseguido por el método de acuerdo con la presente invención.
Sumario de la invención
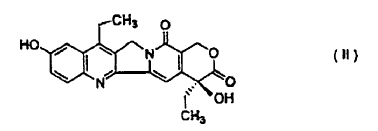
La presente invención se refiere a un método para preparar 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina de fórmula I, caracterizado por que la 7-etil-10-hidroxicamptotecina de fórmula II:
se condensa con hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina de fórmula III:
en un disolvente aprótico polar tal como acetonitrilo y en presencia de 4-dimetilaminopiridina. La condensación transcurre en suspensión, en el caso de que el disolvente aprótico polar disuelva sólo la 4-dimetilaminopiridina mientras la 7-etil-10-hidroxicamptotecina y el hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina permanezcan sin disolver en este disolvente aprótico polar. La cantidad de hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina empleada en la reacción de condensación es preferiblemente 1,3 a 3 moles, más preferiblemente 1,6 a 1,9 moles, por 1 mol de 7-etil-10-hidroxicamptotecina. La cantidad de 4-dimetilaminopiridina usada en la condensación oscila preferiblemente entre 1,5 y 4 moles, más preferiblemente entre 1,8 y 2,2 moles, por 1 mol de 7-etil-10-hidroxicamptotecina. La cantidad del disolvente aprótico polar usada en la condensación es preferiblemente 400 a 600 moles, más preferiblemente 430 a 460 moles, por mol de 7-etil-10-hidroxicamptotecina. La condensación se realiza preferiblemente a una temperatura de 70 a 80ºC, más preferiblemente a 73 a 77ºC.
Después de terminar la condensación, los presentes compuestos de lastre, que consisten en por ej., 4-dimetilaminopiridina, 4-piperidinopiperidina y urea, se retiran por lavado de la base de irinotecán obtenida mediante un disolvente aprótico polar, preferiblemente acetonitrilo. El rendimiento de la condensación es al menos 94% y el producto obtenido contiene al menos el 98% de la base de irinotecán deseada, cuando se determina por cromatografía líquida de alta resolución.
La principal ventaja del método de acuerdo con esta invención consiste en que el tratamiento final de la mezcla de reacción después de la condensación sólo transcurre con pérdidas insignificantes del producto final y que la condensación no va acompañada de impurezas coloreadas.
Ejemplos
Ejemplo 1
En un vaso de precipitados en un baño de ultrasonidos se ponen 10 g (0,0247 moles) de 7-etil-10-hidroxicamptotecina y 99 ml de acetonitrilo. Se agita la suspensión obtenida en el baño de ultrasonidos hasta homogeneidad. Después se transfiere cuantitativamente la suspensión a un matraz Keller de tres bocas, equipado con un agitador mecánico, termómetro y condensador de reflujo. En el vaso de precipitados ahora vacío se ponen ahora 6,2 g (0,0502 moles) de 4-dimetilaminopiridina cristalina y 40 ml de acetonitrilo. Se agita la mezcla hasta que se disuelve la porción cristalina. Se añade después cuantitativamente la disolución obtenida a la suspensión de 7-etil-10-hidroxicamptotecina. Se añaden después al vaso de precipitados vacío 13,6 g (0,0434 moles) de hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina y 79 ml de acetonitrilo y se agitó la suspensión en el baño de ultrasonidos hasta que fue homogénea. Se transfirió cuantitativamente la suspensión obtenida al matraz Keller de tres bocas, que ya contenía 7-etil-10-hidroxicamptotecina y 4-dimetilaminopiridina en acetonitrilo y se añaden 382 ml de acetonitrilo a la mezcla. La suspensión obtenida de la reacción en el matraz Keller se agita a 75ºC durante 5 h. Después de 2 h la suspensión ligeramente amarilla llega a ser más espesa y su color se vuelve color café con leche, indicando así el correcto curso de la reacción. Después de 5 h, se deja enfriar la suspensión a 18 a 20ºC, se filtra y se lava la torta de filtración con 300 ml de acetonitrilo. Después de retirar el acetonitrilo por filtración por succión, se seca la 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina obtenida a 60 a 65ºC a peso constante en un secador. Esto proporciona 14,1 g (rendimiento del 94,3%) de producto que, según cromatografía líquida de alta resolución, contiene 98,9% de7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina.
Reivindicaciones:
1. Un método para preparar 7-etil-10-[4-(1-piperidino)-1-piperidino]carboniloxicamptotecina de fórmula I:
caracterizado por que se somete la 7-etil-10-hidroxicamptotecina de fórmula II:
a una reacción de condensación con hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina de fórmula III:
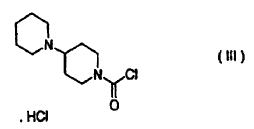
en un disolvente aprótico polar, por ej., en acetonitrilo, en presencia de 4-dimetilaminopiridina.
2. El método según la reivindicación 1, caracterizado por que el hidrocloruro de 1-clorocarbonil-4-piperidinopiperidina se emplea en una cantidad de 1,3 a 3 moles, preferiblemente en una cantidad de 1,6 a 1,9 moles, por 1 mol de 7-etil-10-hidroxicamptotecina.
3. El método según cualquiera de las reivindicaciones precedentes, caracterizado por que se emplea 4-dimetilaminopiridina en una cantidad de 1,5 a 4 moles, preferiblemente en una cantidad de 1,8 a 2,2 moles, por 1 mol de 7-etil-10-hidroxicamptotecina.
4. El método según cualquiera de las reivindicaciones precedentes, caracterizado por que se emplea el disolvente aprótico polar en una cantidad de 400 a 600 moles, preferiblemente en una cantidad de 430 a 460 moles, por 1 mol de 7-etil-10-hidroxicamptotecina.
5. El método según cualquiera de las reivindicaciones precedentes, caracterizado por que la reacción de condensación se realiza a una temperatura de 70 a 80ºC, preferiblemente a una temperatura de 73 a 77ºC.
Patentes similares o relacionadas:
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
 Fármacos heteroaromáticos que pueden marcarse y sus conjugados, del 29 de Enero de 2020, de RAMOT AT TEL AVIV UNIVERSITY LTD.: Un compuesto de fórmula I:
I Y-CF2-(CR1R2)n-X-(CR1R2)m-R1
en la que:
Y es un fármaco o un reactivo bioactivo, que comprende un anillo heteroaromático […]
Fármacos heteroaromáticos que pueden marcarse y sus conjugados, del 29 de Enero de 2020, de RAMOT AT TEL AVIV UNIVERSITY LTD.: Un compuesto de fórmula I:
I Y-CF2-(CR1R2)n-X-(CR1R2)m-R1
en la que:
Y es un fármaco o un reactivo bioactivo, que comprende un anillo heteroaromático […]
Reactivos de merilformilo sustituido y procedimiento de uso de los mismos para modificar propiedades fisicoquímicas y/o farmacocinéticas de compuestos, del 15 de Enero de 2020, de Sphaera Pharma Pte. Ltd: Un compuesto farmacéutico modificado, que se selecciona entre el grupo que consiste en: - Compuesto n.º 295: yoduro de 1-(acetoximetil)-4-((4-etoxi-3-(1-metil-7-oxo-3-propil-4,7-dihidro-1H-pirazolo[4,3- […]
Síntesis de alcaloides policíclicos y su uso como agonistas de TGR5, del 11 de Diciembre de 2019, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que tiene una fórmula **(Ver fórmula)** en la que una línea discontinua ("---") se usa para ilustrar que un enlace […]
Conjugados de liberación lenta de SN-38, del 20 de Noviembre de 2019, de Prolynx LLC: Un conjugado de fórmula (I)**Fórmula** en la que PEG es lineal o ramificado y, cuando q es 2-8, de múltiples brazos, polietilenglicol; X es O, NH, (CH2)m, […]
Métodos y sistemas para la síntesis del análogo de camptotecina, del 21 de Agosto de 2019, de Vivacitas Oncology Inc: Un método para fabricar el compuesto AR-67**Fórmula** Que comprende: Formar AP4622-1**Fórmula** A partir de propano-1,3-ditiol y 3-hidroxibenzaldehído; Añadir […]
Compuestos tricíclicos sustituidos como inhibidores de FGFR, del 19 de Marzo de 2019, de Incyte Holdings Corporation: Un compuesto de fórmula II:**Fórmula** o una sal farmacéuticamente aceptable del mismo, en la que: W es CR17R18; X es CR15 o N; R1 es […]
Métodos útiles en la síntesis de análogos de halicondrina B, del 20 de Febrero de 2019, de EISAI R&D MANAGEMENT CO., LTD: Un método para preparar un intermedio en la síntesis de eribulina, comprendiendo dicho método hacer reaccionar un compuesto que tiene la fórmula (I): **(Ver […]