MATERIAL HIBRIDO NANOESTRUCTURADO QUE COMPRENDE NANOPARTICULAS DE ORO METODO DE PREPARACION Y USO.
Material híbrido nanoestructurado que comprende nanopartículas de oro,
método de preparación y uso.
La presente invención se refiere a un material híbrido nanoestructurado compuesto de al menos dos componentes: un núcleo metálico, constituido por dos o más nanopartículas de oro, dando lugar a un agregado o nanocluster de oro y una matriz de un compuesto inorgánico, preferentemente sílice, que envuelve el núcleo metálico, capaz de absorber la radiación infrarroja cercana y su utilización en una aplicación biotecnológica, preferentemente, el tratamiento o profilaxis de una patología por terapia fototérmica
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702285.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS
UNIVERSIDAD POLITECNICA DE VALENCIA.
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: CORMA CANOS,AVELINO, BOTELLA ASUNCION,PABLO, FERNANDEZ JOVER,EDUARDO, NAVARRO VILLALBA,MARIA TERESA.
Fecha de Solicitud: 14 de Agosto de 2007.
Fecha de Publicación: .
Fecha de Concesión: 27 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K47/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo.
- A61N5/06 A61 […] › A61N ELECTROTERAPIA; MAGNETOTERAPIA; RADIOTERAPIA; TERAPIA POR ULTRASONIDOS (medida de corrientes bioeléctricas A61B; instrumentos quirúrgicos, dispositivos o métodos para transferir formas no mecánicas de energía hacia o desde el cuerpo A61B 18/00; aparatos de anestesia en general A61M; lámparas incandescentes H01K; radiadores de infrarrojos utilizados como calefactores H05B). › A61N 5/00 Radioterapia (dispositivos o aparatos aplicables a la vez a la terapia y al diagnóstico A61B 6/00; aplicación de material radiactivo al cuerpo A61M 36/00). › utilizando radiación luminosa (A61N 5/01 tiene prioridad).
- B22F1/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B22 FUNDICION; METALURGIA DE POLVOS METALICOS. › B22F TRABAJO DE POLVOS METALICOS; FABRICACION DE OBJETOS A PARTIR DE POLVOS METALICOS; FABRICACION DE POLVOS METALICOS (fabricación de aleaciones mediante metalurgia de polvos C22C ); APARATOS O DISPOSITIVOS ESPECIALMENTE ADAPTADOS PARA POLVOS METALICOS. › Tratamiento especial de polvos metálicos, p. ej. para facilitar su trabajo, para mejorar sus propiedades; Polvos metálicos en sí , p. ej. mezclas de partículas de composiciones diferentes.
Clasificación PCT:
- A61K47/00 A61K […] › Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo.
- A61N5/06 A61N 5/00 […] › utilizando radiación luminosa (A61N 5/01 tiene prioridad).
- B22F1/00 B22F […] › Tratamiento especial de polvos metálicos, p. ej. para facilitar su trabajo, para mejorar sus propiedades; Polvos metálicos en sí , p. ej. mezclas de partículas de composiciones diferentes.
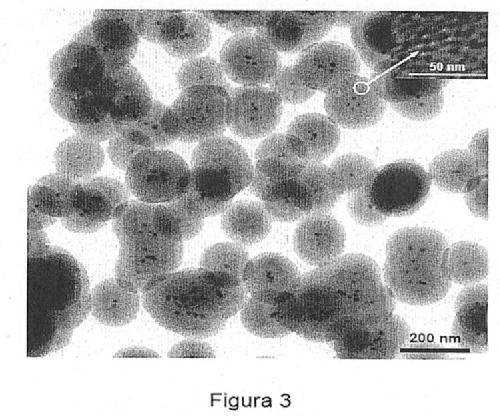
Fragmento de la descripción:
Material híbrido nanoestructurado que comprende nanopartículas de oro método de preparación y uso.
Campo técnico de la invención
La presente invención se enmarca dentro de las aplicaciones de la nanotecnología y la biomedicina. La preparación de partículas coloidales de oro estables en medios biológicos requiere de su protección mediante una cubierta externa. La incorporación de 2 o más nanopartículas de oro dentro de una misma cápsula conlleva la interacción entre las mismas frente a estímulos electromagnéticos. Ello permite su aplicación como herramientas de diagnóstico, control de la liberación de fármacos o tratamientos por fototermia.
Estado de la técnica anterior a la invención
Actualmente existe un interés creciente en el desarrollo de estructuras con propiedades ópticas controladas a escala nanométrica, con el fin de aplicarlas en sistemas biotecnológicos para diagnóstico y terapia de enfermedades a escala celular. Así, el tratamiento de enfermedades consecuencia de una degeneración celular, p.e. el cáncer, precisa de la eliminación selectiva de las células malignas sin dañar los tejidos adyacentes. Una de las posibles actuaciones es la terapia térmica en la que el tejido lesionado se irradia con una fuente de calor para producir hipertermia. El aumento de temperatura asociado causa numerosas interacciones biológicas a nivel celular, como la desnaturalización de las proteínas y ácidos nucleicos, necrosis celular, ruptura de membranas, etc. Como fuentes de calor se ha empleado microondas, ultrasonidos y radiación láser de alta frecuencia. Esta técnica, sin embargo, presenta como principal inconveniente la escasa selectividad, destruyendo tanto las células malignas como las sanas, con un riesgo elevado de quemaduras en el cuerpo del paciente cuando la exposición a la radiación térmica se mantiene durante periodos prolongados.
Una modificación de dicha técnica es la terapia fototérmica, basada en la incorporación de un componente ópticamente activo a las células, que absorbe la luz infrarroja en el intervalo de 800-1300 nm, en el que los tejidos biológicos presentan escasa o nula absorbancia. De esta manera, el calor se genera únicamente en las células provistas del material absorbente. La destrucción celular tiene lugar por hipertermia pero también debido a las tensiones ocasionadas por la formación de burbujas consecuencia de la evaporación del medio líquido circundante a las partículas del material fotosensible, pudiendo llevar a la lisis celular (fototermolisis).
En la solicitud de patente US2007091967 se describe un material compuesto de una matriz polimérica conteniendo nanopartículas de rodamina 590 o rodamina 610, capaz de dispersar la luz láser de 585-630 nm, si bien dicho intervalo queda muy lejos de la longitud de onda necesaria en tratamientos fototérmicos.
En el caso de nanopartículas metálicas con propiedades ópticas, se ha descrito (W.S. Seo, J.H. Lee, X. Sun, Y. Suzuki, D. Mann, Z. Liu, M. Terashima, P.C. Yang, M.V. McConnell, D.G. Nishimura y H. Dai, Nature Mater. 5, 971 (2006)) el uso de nanocristales de Fe/Co encapsulados en una cubierta de grafito capaces de absorber la radiación láser de 808 nm de longitud de onda. Si bien no se ha comprobado la actividad de dicho sistema en medios biológicos, la presencia de componentes potencialmente tóxicos en el organismo limita sus aplicaciones terapéuticas.
Por el contrario, las partículas de oro coloidal constituyen una opción de fácil preparación y altamente biocompatible. Estas presentan una resonancia plasmónica centrada a 520 nm (para un diámetro medio de la nanopartícula de 10 nm), si bien dicho máximo de absorbancia puede desplazarse unos 30 nm al modificar el diámetro de partícula, el ligando empleado para su estabilización o el disolvente. Sin embargo, el uso de estas nanopartículas en tratamientos de fototermia queda limitado por la escasa absorbancia que presentan en el intervalo de 800-1300 nm, correspondiente a la radiación infrarroja cercana. Se han utilizado nanopartículas de sílice protegidas por una cubierta delgada de oro de espesor variable como agente fotosensible. Estas nanocubiertas de oro se tratan en US-6.530.944. La ventaja de dicho material es la posibilidad de modular el máximo de resonancia plasmónica variando el diámetro total de las nanopartículas y el espesor de la cubierta de oro. De esta forma, resulta posible elaborar nanocubiertas de oro con una resonancia plasmónica centrada a 800 nm. Sin embargo, existen importantes inconvenientes para su aplicación en organismos vivos. De un lado, la superficie externa accesible para su funcionalización con sustancias químicas (fármacos, biomarcadores) y anticuerpos específicos de receptores de membrana de las células objetivo es limitada. De otro lado, la estabilidad en fluidos biológicos es baja, con una considerable tendencia a la agregación y formación de depósitos metálicos.
En la solicitud WO06122222 se detalla la preparación de nanovarillas de oro de dimensiones controladas y sus aplicaciones en diagnóstico y fototermolisis. Variando la forma (determinada por la relación de diámetros máximo y mínimo) es posible obtener partículas del metal noble con un máximo de absorción centrado en el infrarrojo cercano. Este material presenta, no obstante, las mismas limitaciones que las nanocubiertas de oro para aplicaciones biotecnológicas.
Se ha descrito la preparación de nanoclusters de oro por agregación controlada de nanopartículas de oro (B. Khlebtsov, V. Zharov, A. Melnikov, V. Tuchin y N. Khlebtsov, Nanotechnology 17, 5167 (2006)) y su aplicación en fototermolisis (V.P. Zharov, K.E. Mercer, E.N. Galitovskaya y M.S. Smeltzer, Biophysical Journal 90, 619 (2006)). A partir de partículas de oro de diámetro entre 30 y 40 nm se obtiene, por agregación, nanoclusters entre 100 y 200 nm. Como consecuencia, el máximo de resonancia plasmónica se desplaza desde 530 nm de las nanopartículas monodispersas hasta unos 650 nm. Asimismo, el intervalo de relajación térmica aumenta en estos nanoclusters, lo que se traduce en un efecto fototérmico más intenso. Además, la presencia de varias nanopartículas juntas o próximas genera un efecto sinérgico consistente en un solapamiento de las nanoburbujas correspondientes a las partículas simples, dando lugar a una burbuja de mayores dimensiones de efectos más destructivos sobre la estructura celular. A pesar de su probada ausencia de citotoxicidad, estos nanoclusters presentan el problema de la estabilidad en medios biológicos. La presencia de especies iónicas en fluidos corporales disminuye el potencial Z del coloide de oro, lo que conduce a la formación de agregados metálicos que precipitan. Además, los ligandos orgánicos empleados para estabilizar los nanocluster en medio acuoso pueden provocar una respuesta inmune que conduzca a su eliminación del torrente sanguíneo.
En función de lo expuesto, y para superar los inconvenientes de los materiales conseguidos hasta ahora, se ha planteado como muy interesante encapsular las nanopartículas de oro dentro de una cubierta protectora que les confiera estabilidad y carácter inerte frente al sistema inmunitario y a la vez permita un alto grado de funcionalización. Secundariamente, la inclusión de partículas coloidales de oro y/o sus agregados (se considera 2 partículas agregadas cuando la distancia entre ellas es inferior a su diámetro medio) evitaría la extravasación y la rápida excreción por vía renal.
El encapsulamiento en sílice resulta particularmente ventajoso en la medida en que permite controlar los parámetros texturales de la cubierta y al mismo tiempo ofrece numerosas posibilidades de funcionalización. En este sentido, resulta especialmente conveniente la incorporación de nanoparticulas de oro en una matriz de sílice mesoporosa, pudiendo conseguir un alto de ordenación de sus poros, con tamaño de poro controlable y una elevada área superficial. Así, en la solicitud de patente US-2003157330 se describe un procedimiento de recubrimiento mediante propagación de la pared de MCM-41 por hidrólisis controlada de un alcóxido de silicio sobre una nanopartícula de oro en presencia de un surfactante, obteniendo un nanocomposite Oro-MCM41 con un núcleo metálico constituido por una única partícula de oro, generalmente centrada en la matriz de silicato, y un diámetro medio entre 300 y 500 nm. La eliminación del oro por disolución da lugar a nanoparticulas huecas, reivindicando que su interior puede utilizarse para el transporte de catalizadores, colorantes orgánicos y moléculas biológicamente activas. El método de preparación de estos materiales y sus...
Reivindicaciones:
1. Un material híbrido nanoestructurado caracterizado porque comprende al menos dos componentes:
2. Un material híbrido nanoestructurado según la reivindicación 1, caracterizado porque comprende al menos dos componentes:
3. Un material híbrido nanoestructurado según la reivindicación 1, caracterizado porque comprende al menos dos componentes:
4. Un material híbrido nanoestructurado según la reivindicación 1, caracterizado porque comprende al menos dos componentes:
5. Un material híbrido nanoestructurado según la reivindicación 1 caracterizado porque la matriz que envuelve el núcleo metálico es una matriz no estructurada y no porosa, y es de sílice.
6. Un material híbrido nanoestructurado según la reivindicación 1 o 3, caracterizado porque la matriz que envuelve el núcleo metálico es no estructurada y porosa, con diámetro de poro comprendido entre 1 y 100 nm, y es de sílice.
7. Un material híbrido nanoestructurado según la reivindicación 1 o 4, caracterizado porque la matriz que envuelve el núcleo metálico es estructurada y porosa, con diámetro de poro comprendido entre 1 y 30 nm, y es de un compuesto de silicio.
8. Un material material híbrido nanoestructurado según la reivindicación 1 ó 7 caracterizado porque está compuesto de nanopartículas que presentan una matriz silícea con orden a larga distancia.
9. Un material material híbrido nanoestructurado según la reivindicación 8, caracterizado porque dicha matriz silícea está seleccionada entre una matriz con estructura tipo MCM- 41, MCM-48, MCM-50, FSM-16, HMS, KIT-1, MSU-1, MSU-2, MSU- 3, MSU-V, SBA-1, SBA-2, SBA-3, SBA-8, SBA-11, SBA-12, SBA- 14, SBA-15, SBA-16, STAC-1, Ma y PCH.
10. Un material según la reivindicación 9 caracterizado porque la distancia centro de poro a centro de poro en la matriz de sílice está comprendida entre 3,4 y 4,2 nm, y el espesor de la pared oscila entre 1 y 2 nm.
11. Un material según una cualquiera de las reivindicaciones 1 a 10, caracterizado porque las nanopartículas del material híbrido presentan forma esférica, hexagonal o alargada.
12. Un material según cualquiera de las reivindicaciones 1 a 11 caracterizado porque las nanopartículas del material híbrido presentan un diámetro medio comprendido entre 80 y 300 nm.
13. Un material según cualquiera de las reivindicaciones 1 a 11 caracterizado porque las nanopartículas del material híbrido contienen preferentemente entre 2 y 20 nanopartículas de oro dentro de la matriz.
14. Un material según cualquiera de las reivindicaciones 1 a 11 caracterizado porque las nanopartículas de oro presentan un tamaño uniforme comprendido entre 10 y 60 nm.
15. Un método de preparación del material híbrido definido en la reivindicación 1 caracterizado porque comprende poner en contacto una solución coloidal de oro con una solución acuosa de un compuesto inorgánico y mantener la agitación para permitir el crecimiento de la matriz inorgánica que envuelve al núcleo metálico en torno al nanocluster de oro.
16. Un método de preparación según la reivindicación 15, caracterizado porque comprende además lavar y secar el material híbrido obtenido a una temperatura de al menos 100°C.
17. Un método de preparación según la reivindicación 15, caracterizado porque dicho compuesto inorgánico es un compuesto de silicio.
18. Un método de preparación según la reivindicación 17, caracterizado porque dicho compuesto de silicio está seleccionado entre un alcóxido de silicio, un alquilsilano, silicato sódico y sílice coloidal.
19. Un método de preparación según la reivindicación 15, caracterizado porque comprende introducir un co-solvente a la solución acuosa del compuesto inorgánico con una relación co-solvente:agua en volumen comprendida entre 1:1 y 4:1.
20. Un método de preparación según la reivindicación 19, caracterizado porque dicho compuesto inorgánico es un compuesto de silicio.
21. Un método de preparación según la reivindicación 19, caracterizado porque dicho co-solvente está seleccionado entre un alcohol de cadena alifática con un número de carbonos comprendido entre 1 y 6.
22. Un método de preparación según una de las reivindicaciones 15 a 21, caracterizado porque comprende lavar y secar el material híbrido formado e introducir dicho material híbrido en una disolución acuosa de una fuente de fluoruro.
23. Un método de preparación del material híbrido según la reivindicación 15 o 22, caracterizado porque dicha solución acuosa es una solución de un compuesto de silicio, y dicho método comprende además:
24. Un método según la reivindicación 23 caracterizado porque el compuesto de silicio es un alcóxido de silicio, un alquilsilano, silicato sódico o sílice coloidal.
25. El método según la reivindicación 23 caracterizado porque el compuesto de fluoruro es ácido fluorhídrico o una sal amónica, sódica o potásica del mismo.
26. El método según la reivindicación 23 caracterizado porque comprende introduce un co-solvente a la solución acuosa del compuesto de silicio en una relación co-solvente:agua en volumen comprendida entre 1:1 y 4:1.
27. El método según la reivindicación 26 caracterizado porque comprende dicho co-solvente es un alcohol de cadena alifática con un número de carbonos comprendido entre 1 y 6.
28. Un método según la reivindicación 15 caracterizado porque comprende:
29. El método según la reivindicación 28, caracterizado porque la matriz inorgánica es de un compuesto de silicio seleccionado entre un alcóxido de silicio, un alquilsilano, silicato sódico y sílice coloidal.
30. El método según la reivindicación 28, caracterizado porque el surfactante orgánico es un compuesto catiónico, aniónico o neutro.
31. El método según la reivindicación 28, caracterizado porque la matriz inorgánica es de un compuesto de silicio, y se introduce un co-solvente a la solución acuosa del compuesto de silicio en una relación co-solvente:agua en volumen comprendida entre 1:1 y 4:1.
32. El método según la reivindicación 31 caracterizado porque el co-solvente es un alcohol de cadena alifática con un número de carbonos comprendido entre 1 y 6.
33. Uso de un material híbrido nanoestructurado que comprende al menos dos componentes:
34. Uso según la reivindicación 33, caracterizado porque las células conteniendo las nanopartículas del material híbrido son expuestas a una radiación electromagnética cuya longitud de onda se encuentra entre 800 y 1300 nm.
35. Uso según la reivindicación 33 ó 34, caracterizado porque la radiación electromagnética es de intensidad suficiente para generar calor en las nanopartículas en cantidad efectiva para destruir o lesionar irreversiblemente las células.
36. Uso según una de las reivindicaciones 33 a 35, caracterizado porque la fuente de radiación electromagnética es un láser.
Patentes similares o relacionadas:
MÉTODO PARA OBTENER ALEACIONES METÁLICAS A PARTIR DE UN CONJUNTO DE MATERIAS PRIMAS, del 2 de Julio de 2020, de UNIVERSIDAD TÉCNICA FEDERICO SANTA MARÍA: La invención se refiere a un método para obtener aleaciones metálicas a partir de un conjunto de materias primas, caracterizado porque comprende las siguientes etapas: a) […]
Dispositivo de ablación por chispas y procedimiento de generación de nanopartículas, del 17 de Junio de 2020, de VSParticle Holding B.V: Un dispositivo de ablación por chispas de generación de nanopartículas provisto de una entrada/salida para el gas y que comprende un generador de chispas […]
Polvos basados en hierro para el moldeo por inyección de polvo, del 6 de Mayo de 2020, de HOGANAS AB (PUBL): Materia prima para el moldeo por inyección de metal, que comprende; a) un polvo basado en hierro, con un tamaño de partículas mediano de 25-45 μm, y 99 % de las partículas […]
Clústeres cuánticos atómicos estables, su método de obtención y uso de los mismos, del 6 de Mayo de 2020, de UNIVERSIDADE DE SANTIAGO DE COMPOSTELA: Clústeres cuánticos atómicos, AQCs, estables caracterizados por estar compuestos por menos de 500 átomos de metal, su procedimiento de obtención caracterizado […]
 Método para impresión 3D empleando una suspensión, del 29 de Abril de 2020, de Particle3D ApS: Un proceso para la impresión 3D de un objeto tridimensional (3D), comprendiendo dicho proceso:
a) proporcionar una suspensión que comprende:
• 50-95% en peso de la […]
Método para impresión 3D empleando una suspensión, del 29 de Abril de 2020, de Particle3D ApS: Un proceso para la impresión 3D de un objeto tridimensional (3D), comprendiendo dicho proceso:
a) proporcionar una suspensión que comprende:
• 50-95% en peso de la […]
Pasta de soldadura, del 22 de Abril de 2020, de SENJU METAL INDUSTRY CO. LTD.: Pasta de soldadura que forma uniones de soldadura adaptada para soldar un sustrato, comprendiendo la pasta de soldadura: un componente de polvo […]
USOS TERAPÉUTICOS DE CLÚSTERES CUÁNTICOS ATÓMICOS, del 2 de Abril de 2020, de Nanogap Sub NM Powder, S.A: Se proporciona una invención relacionada con composiciones y usos terapéuticos de clústeres cuánticos atómicos (AQC), en particular composiciones que consisten […]
Recubrimiento de plata de ultra baja emisividad (ultra baja E), del 19 de Febrero de 2020, de FERRO CORPORATION: Una composición absorbente de infrarrojos, cuya parte seca comprende, antes de la cocción: a. del 65 al 93 % en peso de un componente de plata, […]