CONJUGADOS DE POLIAMINA CON RETINOIDES ACIDOS Y PREPARACION DE LOS MISMOS.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GR2002/000045.
Solicitante: PAPAIOANNOU, DIONYSIOS
DRAINAS, DIONYSIOS
BIOMEDICA LIFE SCIENCES S.A.
Nacionalidad solicitante: Grecia.
Dirección: DEPT. OF CHEMISTRY, UNIVERSITY OF PATRAS, UNIVERSITY CAMPUS,26500 PATRAS.
Inventor/es: PAPAIOANNOU,DIONYSIOS, DRAINAS,DIONYSIOS, BIOMEDICA LIFE SCIENCES S.A.
Fecha de Publicación: .
Fecha Concesión Europea: 25 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- A61K47/48H4F
- A61K47/48H4K
Clasificación PCT:
- A61K47/48
Clasificación antigua:
- A61K47/48
Fragmento de la descripción:
Conjugados de poliamina con retinoides ácidos y preparación de los mismos.
Campo de la invención
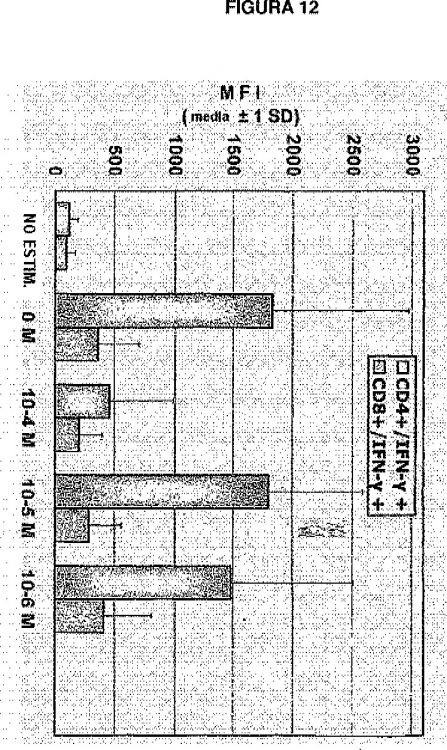
La presente invención se refiere a la preparación de una serie de conjugados de poliamina nuevos con derivados de vitamina A que inhiben la ribozima RNasa P y la producción de IL-2 e IFN-? a través de células mononucleares de sangre periférica in vitro y que tienen aplicaciones terapéuticas potenciales en trastornos neoplásticos, de la queratinización e inflamatorios. En particular, la invención se refiere a conjugados, obtenidos de la condensación de poliaminas lineales, conformacionalmente restringidas, cíclicas y ramificadas con retinoides ácidos, tales como el ácido all-trans-retinoico.
Antecedentes de la invención
Las poliaminas lineales, como la espermina (SPM, 1) y espermidina (SPD, 2), y sus compuestos con otros productos naturales, colectivamente denominados conjugados de poliamina, se distribuyen ampliamente en organismos vivos y presentan propiedades biológicas interesantes.
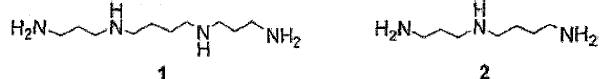
Con el fin de determinar las relaciones de la actividad biológica de la estructura y posiblemente identificar los compuestos guía para el desarrollo de productos farmacéuticos basados en poliamina, se han sintetizado una diversidad de conjugados y análogos de poliamina lineales, ramificados, conformacionalmente limitados y cíclicos (Blagbrough y col., PHARM. SCI., 3, 223 (1997); Schulz y col., ANGEW. CHEM. INT. END. ENGL., 36, 314 (1997); Papaioannou y col., EUR. J. ORG. CHEM., 1841 (2000) y Kong Thoo Lin y col., SYNTHESIS, 1189 (2000)). Debido a su naturaleza policatiónica, las poliaminas interactúan fuertemente con ácidos nucleicos y desempeñan una función importante en su biosíntesis y metabolismo. Estabilizan la conformación de ADN y pueden inducir cambios en la conformación a pesar de la formación de puentes intra o intermoleculares. Las poliaminas producen modificaciones específicas de moléculas de ARN especializadas, estabilizan ribonucleasas y estimulan la acción de ribonucleasas y ribozimas. Ejercen efectos pleiotrópicos en la síntesis de proteínas, son esenciales para el crecimiento normal y están implicadas en los procesos de diferenciación de células mamíferas. Las concentraciones de poliaminas y las enzimas responsables de su biosíntesis son notablemente superiores en la proliferación rápida de células mamíferas; por lo general, estas concentraciones aumentan en todas las células tras la inducción de la diferenciación. Las poliaminas son directamente responsables del aumento en la velocidad de la síntesis macromolecular que tiene lugar durante el desarrollo y crecimiento de tumores. La inhibición de enzimas biosintéticas que producen poliaminas y del sistema de recaptación de poliaminas responsable de alimentar la célula con poliaminas exógenas ha resultado ser un objetivo muy atractivo para la quimioterapia del cáncer. Recientemente, las poliaminas selectivamente N-alquiladas que imitan parcialmente el comportamiento natural de las poliaminas, inhiben el crecimiento celular y son metabólicamente estables, se han desarrollado como agentes anticancerígenos nuevos (para referencias principales véase la revisión de Papaioannou y col., EUR. J. ORG. CHEM., 1841 (2000)).
Los retinoides constituyen una gran familia de compuestos orgánicos relacionados estructuralmente con la Vitamina A de origen natural (retinol, 3) y análogos, tales como retinal (4) y ácido all-trans-retinoico (5) y una diversidad de otros análogos sintéticos, tales como acitretina (6), ácido 13-cis-retinoico (7) y ácido 9-cis-retinoico (8). Los análogos 9 y 10 del ácido all-trans-retinoico de cadena corta del polieno también se pueden considerar miembros de esta familia.
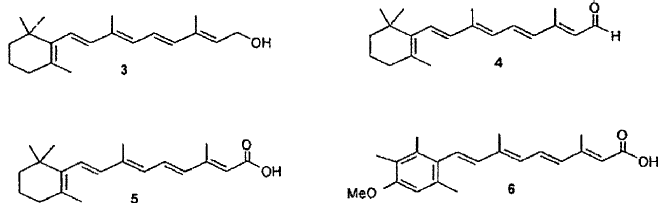
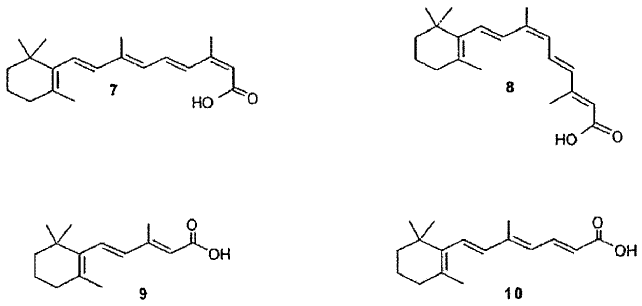
Los retinoides pueden producir respuestas biológicas específicas después de unirse a y activar receptores o grupos de receptores especiales. Los retinoides naturales o sintéticos desempeñan una función importante en la visión, crecimiento celular, reproducción, proliferación y diferenciación de diversos tejidos epiteliales o no epiteliales. Aunque ya se usan ampliamente en el tratamiento sistémico y tópico de diversos trastornos, los retinoides revelan una serie considerable de efectos secundarios incluso cuando se usan en dosis terapéuticas. Así pues, numerosos análogos de retinoides nuevos se han sintetizado para intentar mejorar el índice terapéutico, perfil biológico y selectividad de estos compuestos para la aplicación clínica en dermatología, oncología, reumatología e inmunología (para monografías generales véase Sporn, Roberts and Goodman (Eds.), The Retinoids, vol. 1 y 2, Academic Press, Orlando, 1984; Sporn and Roberts, CIBA FOUND. SYMP., 113, 1 (1985); Sporn, Roberts and Goodman (Eds.), The Retinoids: Biology, Chemistry and Medicine, 2ª ed., Raven Press, New York, 1994; Dawson and Okimura (Eds.), Chemistry and Biology of Synthetic Retinoids, CRC Press, Boca Ratón, 1990; Packer (Ed.), Methods in Enzymology, Academic Press, vol. 189, parí A, 1990 y vol. 190, part B, 1991)). La aplicación clínica de retinoides sintéticos en la gestión de trastornos recalcitrantes y anteriormente neoplásticos incurables, inflamatorios y de queratinización ha presentado una revolución real en dermatología y otros campos médicos (Tsambaos, DERMATOSEN, 44, 182 (1996), Muindi, CANCER TREAT. RES., 87, 305 (1996)). Regulando la expresión genética, los retinoides son capaces de regular la diferenciación y crecimiento de células transformadas o de inhibir la transformación maligna de una diversidad de células que revierten su diferenciación (DeLuca, FASEB J., 5, 2924 (1991), Lotan y Glifford, BIOMED. PARMACOTHER., 45, 145 (1991)). En los mecanismos de regulación de la expresión genética por parte de retinoides, están implicados ciertos miembros de la gran familia de receptores de hormonas de glándulas tiroideas y esteroideas, es decir proteínas nucleares a las que se unen específicamente retinoides (DeLuca, FASEB J., 5, 2924 (1991), Leid y col., TRENOS BIOCHEM. SCI., 17, 427 (1992)). Los receptores de retinoides ya se han aislado y estudiado (Redfern, PATHOBIOL. 60, 254 (1992), Giguere y col., NATURE, 330, 624 (1987), Petkovich y col., NATURE, 330, 444 (1987)). Actúan como factores de trascripción seguido de la activación por medio de ligandos adecuados. En la actualidad, el desarrollo de nuevos fármacos basados en retinoides está basado en la síntesis de nuevos ligandos para los receptores de ácidos retinoicos RARa,ß,? y RXRa,ß,? y los receptores huérfanos (Lippman y Lotan, J. NUTR. 130 (2S Suppl), 479S (2000)).
Recientemente se ha reseñado que los retinoides naturales, como ácido retinoico y retinol, así como análogos sintéticos de ácido retinoico, por ejemplo, isotretinoin (ácido 13-cis-retinoico, acitretina y los arotinoides Ro 13-7410, Ro 15-0778, Ro 15-1570 y Ro 13-6298 pero también otros compuestos, por ejemplo, calcipotriol, antralin y su combinación, conocidos por su actividad antisoriática, inhiben la enzima ribonucleasa P (RNasa P) (Papadimou y col., J. BIOL. CHEM. 273, 24375 (1998), Papadimou y col., SKIN PHARMACOL APPL SKfN PHYSIOL. 13, 345 (2000), Papadimou y col., EUR. J. BIOCHEM. 267, 1173 (2000), Drainas y col, SKIN PHARMACOL. APPL SKIN PHYSIOL.13, 128 (2000), Papadimou y col., BIOCHEM. PHARMACOL. 60, 91 (2000)), que se ha aislado y caracterizado a partir del molde de limo Dictyostelium discoideum (Stathopoulos y col.; EUR.J. BIOCHEM. 228, 976 (1995)) y de queratinocitos epidérmicos humanos normales. (Drainas y col, resultados no publicados). Estos resultados abogan por la hipótesis de que los retinoides, además de regular la trascripción de ADN, también pueden regular la actividad de enzimas desempeñando papeles clave en biosíntesis macromolecular, por su implicación en procesos post-trascripcionales, en los que no está implicada la unión a receptores del ácido retinoico. La RNasa P es responsable de hacer madurar los extremos 5' de las moléculas del precursor tRNA. La actividad de la RNasa P se ha encontrado en todos los organismos pro- y eucarióticos estudiados hasta el momento (Frank y Pace ANNU. REV. BIOCHEM. 67, 153 (1998)). Las enzimas de RNase P son complejos de ARN con proteínas y si actividad se atribuye principalmente a su subunidad de ARN. Varios descubrimientos indican que la estructura de la subunidad...
Reivindicaciones:
1. Conjugados de poliaminas con retinoides ácidos en los que dichos conjugados son amidas de poliaminas en las que el grupo R del grupo acilo RCO es uno de los residuos de retinoide R1-R6 indicados en los siguientes retinoides ácidos y análogos del ácido all-trans-retinoico de cadena corta del polieno farmacéuticamente importantes:
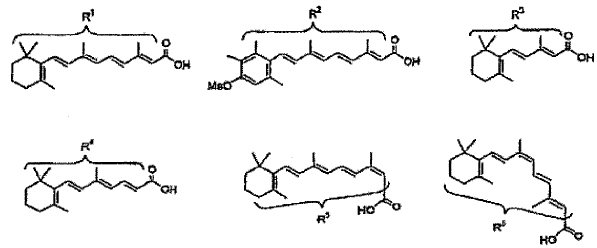
y dichas poliaminas son:
a) tri-, tetra- y hexa-aminas lineales, cuyos conjugados tienen las fórmulas generales siguientes:
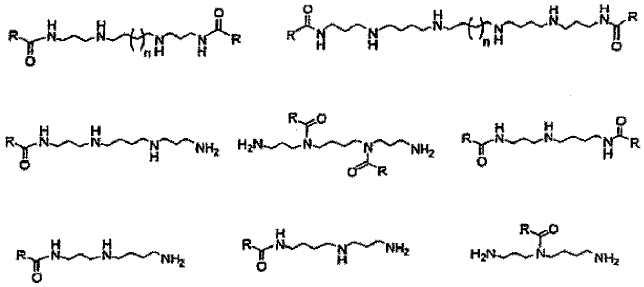
en la que n es 1 a 9
b) poliaminas conformacionalmente restringidas, cuyos conjugados tienen la fórmula general siguiente:
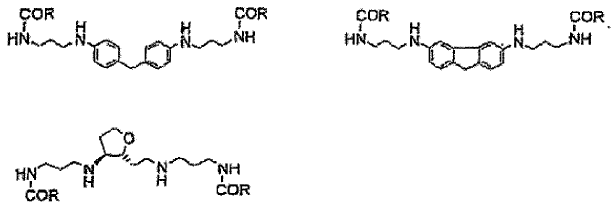
c) poliaminas cíclicas, cuyos conjugados tienen las fórmulas generales siguientes:
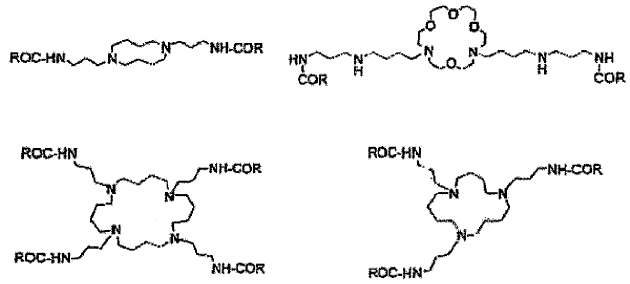
d) poliaminas ramificadas (diméricas), cuyos conjugados tienen la fórmula general siguiente:
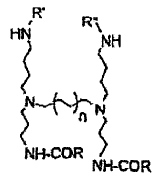
en la que
R' es COR ó (CH2)3NHCOR y R'' es COR ó (CH2)3NHCOR
y n es uno de los números 1, 2 y 7.
2. Un procedimiento para la preparación de un compuesto de acuerdo con la reivindicación 1 que implica las dos siguientes etapas:
a) síntesis de compuestos con la fórmula general
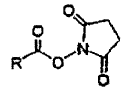
en la que R es uno de los residuos de retinoide R1-R6 de la reivindicación 1, que implica la esterificación de retinoides ácidos con HOSu en presencia del agente de acoplamiento DCC y la purificación con cromatografía ultrarrápida en columna
b) acilación selectiva directa de los grupos amino primarios de poliaminas con los compuestos obtenidos como anteriormente, o la acilación de los grupos amino secundarios de poliaminas, protegidos en sus funciones amino primarias con el grupo trifluoroacetilo o el 9-fluorenilmetoxicarbonilo, con los retinoides ácidos de la reivindicación 1 en presencia del agente de acoplamiento PyBrOP, seguido de desprotección.
3. Un procedimiento de acuerdo con la reivindicación 2, cuyo procedimiento implica la acilación selectiva directa de las funciones amino primarías de poliaminas o sus correspondientes sales de clorhidrato o trifluoroacetato con los compuestos de la etapa a) de la reivindicación 2, en el que el disolvente se selecciona entre diclorometano, cloroformo y dimetilformamida y la base, en caso necesario, se selecciona entre trietilamina y diisopropiletilamina o cualquier otra amina terciaria o en general cualquier otra base no nucleófica.
4. Un procedimiento de acuerdo con la reivindicación 3 caracterizado porque la acilación selectiva de las funciones amino primarias de poliaminas se efectúa con cualquier otro derivado del ácido carboxílico activado conocido para acilar selectivamente funciones amino primarias en presencia de las secundarias.
5. Un procedimiento de acuerdo con la reivindicación 2 caracterizado porque la mono- o bis-acilación selectiva de las funciones amino primarias de poliaminas tiene lugar indirectamente e implica las siguientes etapas:
(i) protección de las funciones amino secundarias de poliaminas, que soportan el grupo tritilo de protección en sus funciones amino primarias, con él grupo 9-fluorenilmetoxicarbonilo o trifluoroacetilo
(ii) detritilación
(iii) mono- o bis-acilación con los compuestos de la etapa a) de la reivindicación 2
(iv) desprotección y purificación completa, en caso necesario, por cromatografía ultrarrápida en columna.
6. Un procedimiento de acuerdo con la reivindicación 2 caracterizado porque la acilación selectiva de las funciones amino secundarias de poliaminas implica las siguientes etapas:
(i) trifluoroacetilación selectiva de las funciones amino primarias de poliaminas
(ii) acilación de las funciones amino secundarias con los retinoides ácidos de la reivindicación 1 en presencia del agente de acoplamiento PyBroP
(iii) eliminación de los grupos trifluoroacetilo por hidrólisis alcalina.
7. Preparaciones o productos farmacéuticos que contienen los compuestos reivindicados en la reivindicación 1 para aplicaciones terapéuticas en humanos.
Patentes similares o relacionadas:
COMPLEJO DE ÁCIDO NUCLEICO Y COMPOSICIÓN DE SUMINISTRO DE ÁCIDO NUCLEICO, del 7 de Diciembre de 2011, de OTSUKA PHARMACEUTICAL CO., LTD. TAKEUCHI, HIROFUMI: Complejo de ácido nucleico que comprende un ácido nucleico y una dextrina cíclica altamente ramificada, en el que la dextrina cíclica altamente ramificada es […]
NUEVOS COMPUESTOS INMUNOEFECTORES, del 8 de Abril de 2010, de CORIXA CORPORATION: Un compuesto que tiene la fórmula:
 METODO DE PRODUCCION DE UNA PREPARACION CATIONICA DE LIPOSOMAS QUE COMPRENDE UN COMPUESTO LIPOFILO, del 15 de Enero de 2010, de MEDIGENE AG: Un método para producir una preparación catiónica de liposomas que comprende al menos un compuesto anfifílico seleccionado de lípidos catiónicos en una […]
METODO DE PRODUCCION DE UNA PREPARACION CATIONICA DE LIPOSOMAS QUE COMPRENDE UN COMPUESTO LIPOFILO, del 15 de Enero de 2010, de MEDIGENE AG: Un método para producir una preparación catiónica de liposomas que comprende al menos un compuesto anfifílico seleccionado de lípidos catiónicos en una […]
USO DE CONJUGADOS DE ACIDO BILIAR O SAL BILIAR CON ACIDO GRASO, del 19 de Noviembre de 2009, de GALMED INTERNATIONAL LTD.: Un conjugado de ácido biliar o sal biliar con ácido graso de fórmula general II W- X - G en la que G es un radical de ácido biliar o sal biliar, que, si se desea, está conjugado […]
Derivativos del ácido siálico para la derivatización y conjugación de proteínas, del 20 de Diciembre de 2019, de LIPOXEN TECHNOLOGIES LIMITED: Un procedimiento de producción de un derivativo aldehído de un ácido siálico en el que un material de partida que tiene una unidad de ácido siálico en el […]
GELES DE QUITOSANO(A) CONTENIENDO NANOPARTICULAS METALICAS DE COBRE, PLATA Y ANTIBIOTICOS (CIPROFLOXACINO, CEFOTAXIME, GENTAMICINA Y CLOXACILINA), del 12 de Diciembre de 2019, de CARDENAS Y CIA LTDA: En la presente invención se describen geles de quitosano (poli-beta-glucosamina) con propiedades bactericidas y fungicidas en mezcla con nanopartículas […]
Compuestos de polímero de polialquileno y usos de los mismos, del 20 de Noviembre de 2019, de Biogen MA Inc: Una composición farmacéutica que comprende un conjugado y un vehículo, adyuvante, diluyente, conservante y/o solubilizante farmacéuticamente […]
Composiciones y métodos para la liberación dirigida de fármacos in vitro e in vivo a células de mamíferos mediante minicélulas intactas derivadas de bacterias, del 23 de Octubre de 2019, de ENGENEIC MOLECULAR DELIVERY PTY LTD: Una composición que comprende: (a) una pluralidad de minicélulas intactas derivadas de bacterias que tienen paredes celulares intactas, en donde la pluralidad […]