COMPOSICION FARMACEUTICA PARA TRATAR CANCER DE PANCREAS LOCALMENTE AVANZADO (CPLA) NO EXTIRPABLE.
Uso de un vector adenovírico, que comprende una secuencia de ácido nucleico que codifica un FNT-a humano y que está ligada operativamente a un promotor inducible por radiación,
en la fabricación de una composición farmacéutica para tratar el cáncer de páncreas localmente avanzado (CPLA) no extirpable en un ser humano, en el que
(a)se administrará una dosis de la composición farmacéutica que comprende (i) un vehículo farmacéuticamente aceptable y (ii) de aproximadamente 4 x 107 a aproximadamente 4 x 1012 unidades de partícula (up) de dicho vector adenovírico localmente en un tumor del ser humano aproximadamente una vez a la semana en un período terapéutico que comprende aproximadamente 3-8 semanas;
(b)se administrará una dosis de radiación ionizante al ser humano durante el período terapéutico; y
(c)se administrará una dosis de uno o más agentes quimioterapéuticos al ser humano durante el período terapéutico
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/034544.
Solicitante: GENVEC, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 65 WEST WATKINS MILL ROAD,GAITHERSBURG, MD 20878.
Inventor/es: KESSLER,PAUL,D, RASMUSSEN,HENRIK,S, CHU,KAREN,W.
Fecha de Publicación: .
Fecha Concesión Europea: 24 de Febrero de 2010.
Clasificación Internacional de Patentes:
- A61K38/21A
- C07K14/525 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factor de necrosis tumoral (TNF).
- C12N15/861 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores adenovirales.
Clasificación PCT:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07K14/525 C07K 14/00 […] › Factor de necrosis tumoral (TNF).
- C12N15/861 C12N 15/00 […] › Vectores adenovirales.
Clasificación antigua:
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07K14/525 C07K 14/00 […] › Factor de necrosis tumoral (TNF).
- C12N15/861 C12N 15/00 […] › Vectores adenovirales.
Fragmento de la descripción:
Composición farmacéutica para tratar cáncer de páncreas localmente avanzado (CPLA) no extirpable.
Campo de la invención
Esta invención se refiere al uso de un vector adenovírico en la fabricación de una composición farmacéutica para tratar el cáncer de páncreas localmente avanzado (CPLA) en un ser humano.
Antecedentes de la invención
La identificación de una terapia eficaz contra uno o varios tipos diferentes de cáncer es el deseo de la investigación sobre el cáncer. Sólo la Sociedad Estadounidense contra el Cáncer distribuyó aproximadamente mil millones de dólares el año pasado entre los investigadores sobre el cáncer que trabajan para dilucidar los mecanismos de una multitud de tipos de cáncer. Sin embargo, a pesar de la extensa investigación sobre la enfermedad, sigue siendo difícil para la comunidad médica encontrar agentes terapéuticos eficaces contra el cáncer. Los profesionales de la salud han obtenido un éxito limitado con las terapias estándar actuales: la quimioterapia, la radioterapia y la cirugía. Sin embargo, cada terapia tiene limitaciones inherentes. La quimioterapia y la radioterapia provocan un daño de consideración en el tejido normal sano, a pesar de los esfuerzos por dirigir tal terapia al tejido anómalo (p. ej., tumores). La cirugía puede ser eficaz en eliminar las masas de células cancerosas; sin embargo, no es posible, incluso para el mejor cirujano, garantizar la eliminación total del tejido afectado, ni todos los tumores tienen una ubicación anatómica que permita su resección quirúrgica. Las limitaciones de las terapias existentes se reflejan en una tasa de supervivencia relativa durante 5 años del 60% para todos los cánceres combinados (Cáncer Facts & Figures 2001, The American Cancer Society, Nueva York, NY).
Los profesionales de la salud han considerado la administración de secuencias de ácidos nucleicos terapéuticas como una posible alternativa a las terapias existentes contra el cáncer. La producción local de agentes terapéuticos a niveles biológicamente relevantes en sitios diana in vivo, reduciendo de ese modo la toxicidad de los tejidos normales, aborda algunas de las limitaciones asociadas a la terapia convencional. Se han examinado numerosos genes en cuanto a sus efectos antitumorales. Uno de los agentes antitumorales más prometedores es el factor de necrosis tumoral (FNT), en particular, el FNT-a, que ha mostrado una actividad con respecto a un número de líneas celulares cancerosas. El FNT-a es un polipéptido de 17 kDa secretado por macrófagos y monocitos. Se ha observado que el FNT-a destruye selectivamente la vasculatura tumoral y activa una miríada de inmunocitos, así como que induce a la apoptosis de algunos tipos de células tumorales (Baher et al., Anticancer Research, 19, 2917-2924 (1999), y Mauceri et al., C. R. Acad. Sci. III, 322, 225-228 (1998)). Sin embargo, el uso del FNT en seres humanos como agente anticancerígeno ha estado limitado por sus graves efectos sistémicos, incluyendo la hipotensión y la insuficiencia respiratoria (Mauceri et al., supra). Además, muchos tipos de cáncer no responden al tratamiento con la proteína FNT-a, tal como, por ejemplo, el cáncer de páncreas (Brown et al., J; Immunotherapy, 10, 376-378 (1991)), el cáncer gástrico (Muggia, Anticancer Drugs, 3, 211-217 (1992)), el cáncer de mama metastásico (Budd et al., Cancer, 68, 1694-1695 (1991)) y el cáncer colorrectal (Heim et al, Onkologie, 13, 444-447 (1990)).
En el documento WO 03/039458 A2, se describe un procedimiento para tratar el cáncer en un ser humano usando FNT. Este procedimiento comprende administrar a un ser humano una dosis de una composición farmacéutica que comprende (i) un vehículo farmacéuticamente aceptable y (ii) un vector adenovírico que comprende una secuencia de ácido nucleico que codifica el FNT-a ligado operativamente a un promotor, comprendiendo la dosis de aproximadamente 1 x 106 a aproximadamente 4 x 1012 unidades de partícula (up) de vector adenovírico, al menos una vez en un período terapéutico que comprende hasta aproximadamente 10 semanas.
Se ha publicado que la administración sistémica de la proteína FNT-a ha tenido un éxito clínico limitado debido a los graves efectos tóxicos limitantes de la dosis, y que esta limitación ha sido superada por el uso de un enfoque de administración génica combinado con un promotor inducible mediante radiación para expresar la proteína FNT-a en el tejido tumoral radiado (Weichselbaum et al, Lancet Oncology, 3, 665-671 (2002)).
Sigue existiendo la necesidad de una composición adecuada para su uso en el tratamiento de una variedad de tipos de cáncer en un paciente, así como de un procedimiento para administrar la composición con el fin de tratar el cáncer. En particular, sigue existiendo la necesidad de una composición y un procedimiento que optimice los efectos locales de los agentes anticancerígenos, tales como el FNT, a la vez que minimice la toxicidad. La invención proporciona tal composición y tal procedimiento. Estas y otras ventajas de la invención, así como otras características de la invención, quedarán claras a partir de la descripción de la invención proporcionada en la presente memoria.
Breve resumen de la invención
La invención proporciona el uso de un vector adenovírico, que comprende una secuencia de ácido nucleico que codifica un FNT-a humano y que está ligada operativamente a un promotor inducible mediante radiación, en la fabricación de una composición farmacéutica para tratar cáncer de páncreas localmente avanzado (CPLA) no extirpable en un ser humano, en el que
Breve descripción de las figuras
La figura 1 es una representación esquemática del genoma de un vector adenovírico sin modificar.
La figura 2 es una representación esquemática de un vector adenovírico que contiene un genoma adenovírico modificado y elementos genéticos según una realización de la invención.
La figura 3A es una vista posterior de un tumor sólido con una ilustración de un patrón preferido para aplicaciones múltiples de una monodosis de composición farmacéutica en el tumor sólido. La figura 3B es una vista lateral de un tumor sólido con una ilustración de un patrón preferido para aplicaciones múltiples de una monodosis de composición farmacéutica en el tumor sólido.
La figura 4 es una vista posterior de un sarcoma de tejido blando con una ilustración de un patrón preferido para aplicaciones múltiples de una monodosis de composición farmacéutica en el sarcoma de tejido blando.
Descripción detallada de la invención
La invención proporciona el uso de un vector adenovírico en la fabricación de una composición farmacéutica para tratar el CPLA en un ser humano (p. ej., un paciente en necesidad de tal tratamiento). El procedimiento implica la administración de FNT-a en un tumor, preferiblemente, directamente en el tumor, en combinación con quimioterapia y radioterapia, mediante lo que se reduce el tamaño del tumor. En particular, el procedimiento comprende administrar a un ser humano en necesidad de tratamiento una composición farmacéutica que comprende un vector adenovírico, preferiblemente, un vector adenovírico de replicación deficiente, que comprende una secuencia de ácido nucleico que codifica un FNT-a humano en un vehículo farmacéuticamente aceptable. El procedimiento comprende además administrar una dosis de radiación ionizante y una dosis de uno o más agentes quimioterapéuticos al ser humano. La administración de la secuencia codificante del FNT-a humano, especialmente, en combinación con la administración de la radiación y la quimioterapia, ofrece una mejora de los tratamientos...
Reivindicaciones:
1. Uso de un vector adenovírico, que comprende una secuencia de ácido nucleico que codifica un FNT-a humano y que está ligada operativamente a un promotor inducible por radiación, en la fabricación de una composición farmacéutica para tratar el cáncer de páncreas localmente avanzado (CPLA) no extirpable en un ser humano, en el que
2. El uso de la reivindicación 1, en el que el vector adenovírico, la dosis de radiación ionizante y la dosis del uno o más agentes quimioterapéuticos se administrarán al ser humano simultáneamente durante el período terapéutico.
3. El uso de la reivindicación 1 o la reivindicación 2, en el que la composición farmacéutica se inyectará en el tumor, de modo se destruyan las células tumorales del tumor.
4. El uso de la reivindicación 3, en el que la composición farmacéutica se inyectará en el tumor, de modo que se reduzca el tamaño del tumor.
5. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una reducción del aproximadamente 25% al 50% del tamaño del tumor durante al menos cuatro semanas tras finalizar el período terapéutico en comparación con la superficie del tumor antes del período terapéutico.
6. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una reducción como mínimo del aproximadamente 50% en el tamaño del tumor durante al menos cuatro semanas tras finalizar el período terapéutico en comparación con la superficie del tumor antes del período terapéutico.
7. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una desaparición del tumor que se mantiene durante al menos cuatro semanas.
8. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una reducción como mínimo del 10% del nivel de antígeno tumoral CA19-9 a las 4-12 semanas de finalizar el período terapéutico en comparación con el nivel de antígeno tumoral CA19-9 antes del período terapéutico.
9. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por la conversión del estadio quirúrgico del tumor de no extirpable a extirpable a las 12 semanas de finalizar el período terapéutico.
10. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una disminución como mínimo del 50% de la intensidad del dolor según lo asignado por los criterios de respuesta al beneficio clínico durante cualquier período de cuatro semanas consecutivas en las 12 semanas posteriores a la finalización del período terapéutico en comparación con la intensidad del dolor antes del período terapéutico.
11. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por una disminución como mínimo del 50% del consumo de analgésicos según lo asignado por los criterios de respuesta al beneficio clínico durante cualquier período de cuatro semanas consecutivas en las 12 semanas posteriores a la finalización del período terapéutico en comparación con el consumo de analgésicos antes del período terapéutico.
12. El uso de la reivindicación 3, mediante el que el tratamiento del cáncer de páncreas localmente avanzado no extirpable se manifestará por un aumento de al menos 20 puntos en la puntuación de la escala de rendimiento de Karnofsky según lo asignado por los criterios de respuesta al beneficio clínico durante cualquier período de cuatro semanas consecutivas en las 12 semanas posteriores a la finalización del período terapéutico en comparación con la puntuación antes del período terapéutico.
13. El uso de cualquiera de las reivindicaciones 1-12, en el que el vector adenovírico es de replicación deficiente.
14. El uso de cualquiera de las reivindicaciones 1-13, en el que el promotor inducible por radiación es el promotor EGR-1.
15. El uso de cualquiera de las reivindicaciones 1-14, en el que se administrará una dosis de composición farmacéutica en un tumor aproximadamente una vez a la semana en un período terapéutico que comprende aproximadamente de tres a siete semanas.
16. El uso de cualquiera de las reivindicaciones 1-15, en el que el período terapéutico comprende hasta seis semanas y se administrará una dosis de composición farmacéutica en cada semana del período terapéutico.
17. El uso de cualquiera de las reivindicaciones 1-16, en el que la composición farmacéutica se administrará en el tumor mediante administración transabdominal percutánea, administración endoscópica o mediante administración endoscópica guiada por ultrasonido.
18. El uso de cualquiera de las reivindicaciones 1-17, en el que la composición farmacéutica se administrará en el tumor mediante 2-5 inyecciones.
19. El uso de cualquiera de las reivindicaciones 1-18, en el que la dosis de radiación ionizante comprende de aproximadamente 40 grays (Gy) a aproximadamente 60 Gy y se administrará durante el período terapéutico.
20. El uso de la reivindicación 19, en el que se administrará una fracción de la dosis de radiación ionizante al día durante cinco días en cada semana del período terapéutico.
21. El uso de la reivindicación 20, en el que la fracción de dosis de radiación ionizante comprende aproximadamente 1-2 Gy.
22. El uso de la reivindicación 20 o la reivindicación 21, en el que la fracción de la dosis de radiación ionizante se administrará al ser humano al menos cuatro horas después de la administración de la composición farmacéutica.
23. El uso de cualquiera de las reivindicaciones 19-22, en el que se administrará además una dosis de refuerzo de radiación ionizante que comprende aproximadamente 5-10 Gy en el tumor.
24. El uso de cualquiera de las reivindicaciones 1-23, en el que el uno o más agentes quimioterapéuticos se seleccionan del grupo constituido por adriamicina, asparaginasa, bleomicina, busulfán, cisplatino, carboplatino, carmustina, capecitabina, clorambucil, citarabina, ciclofosfamida, camptotecina, dacarbazina, dactinomicina, daunorrubicina, dexrazoxano, docetaxel, doxorrubicina, etopósido, floxuridina, fludarabina, fluorouracilo, gemcitabina, hidroxiurea, idarrubicina, ifosfamida, irinotecan, lomustina, mecloretamina, mercaptopurina, meplhalán, metotrexato, mitomicina, mitotano, mitoxantrona, nitrosurea, paclitaxel, pamidronato, pentostatina, plicamicina, procarbazina, rituximab, estreptozocina, tenipósido, tioguanina, tiotepa, vinblastina, vincristina, vinorelbina, taxol, transplatino y 5-fluorouracilo.
25. El uso de la reivindicación 24, en el que el uno o los más agentes quimioterapéuticos se seleccionan del grupo constituido por 5-fluorouracilo, capecitabina y cisplatino, o combinaciones de los mismos.
26. El uso de la reivindicación 25, en el que el agente quimioterapéutico es 5- fluorouracilo.
27. El uso de la reivindicación 26, en el que la dosis de 5-fluorouracilo comprende de aproximadamente 100 mg/m2/día a aproximadamente 300 mg/m2/día.
28. El uso de la reivindicación 25, en el que el agente quimioterapéutico es capecitabina.
29. El uso de la reivindicación 28, en el que la dosis de capecitabina comprende de aproximadamente 800 mg/m2/día a aproximadamente 1.000 mg/m2/día.
30. El uso de la reivindicación 25, en el que el período terapéutico comprende cinco semanas y se administrarán aproximadamente 50-100 mg/m2 de cisplatino y aproximadamente 900-1.100 mg/m2 de 5-fluorouracilo comenzando en cada uno de dos días distintos del período terapéutico.
31. El uso de la reivindicación 30, en el se administrarán aproximadamente 75 mg/m2 de cisplatino y aproximadamente 1.000 mg/m2 de 5-fluorouracilo comenzando el día 1 y el día 29 del período terapéutico.
32. El uso de cualquiera de las reivindicaciones 24-31, en el que el uno o los más agentes quimioterapéuticos se administrarán en las 24 horas de la administración de la dosis de radiación ionizante.
33. El uso de cualquiera de las reivindicaciones 1-32, en el que además se extirpará quirúrgicamente el tumor tras finalizar el período terapéutico.
34. El uso de las reivindicación 33, en el que el tumor se extirpará quirúrgicamente a las 4-10 semanas de finalizar el período terapéutico.
35. El uso de las reivindicación 34, en el que el tumor se extirpará quirúrgicamente a las 3-6 semanas de finalizar el período terapéutico.
36. El uso de cualquiera de las reivindicaciones 33-35, en el que se administrará quimioterapia adyuvante tras la resección quirúrgica del tumor.
37. El uso de la reivindicación 36, en el que la quimioterapia adyuvante se administrará las 2-4 semanas siguientes a la resección quirúrgica del tumor.
38. El uso de cualquiera de las reivindicaciones 1-37, en el que se administrará además una dosis de un bloqueador H2 o un inhibidor de la bomba de protones.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Composiciones y métodos para la expresión de ARNs de guía de CRISPR utilizando el promotor de H1, del 29 de Enero de 2020, de THE JOHNS HOPKINS UNIVERSITY: Un sistema CRISPR-Cas no natural que comprende un vector que comprende un promotor H1 bidireccional, en donde el promotor de H1 bidireccional comprende: a) elementos […]
Métodos y composiciones para tratar depósitos amiloides, del 22 de Enero de 2020, de UNIVERSITY OF IOWA RESEARCH FOUNDATION: Una partícula de rAAV2 que comprende una proteína de la cápside de AAV2 y un vector que comprende un ácido nucleico que codifica para una […]
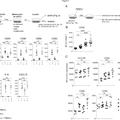 Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Adenovirus que expresan antígenos oncógenos heterólogos, del 4 de Septiembre de 2019, de BOARD OF REGENTS THE UNIVERSITY OF TEXAS SYSTEM: Un adenovirus oncolítico recombinante que tiene un genoma que comprende una o más secuencias de ácido nucleico heterólogas que codifican un antígeno oncógeno, […]
Vector de virus adenoasociado, del 28 de Agosto de 2019, de KING'S COLLEGE LONDON: Un vector de virus adenoasociado (AAV) recombinante que comprende: (a) una proteína de la cápside del AAV2 variante, en el que la proteína de la cápside del AAV2 variante […]
Mutantes de E1A y E1B de adenovirus selectivos de tumor, del 10 de Julio de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un adenovirus recombinante que comprende una secuencia de ADN que se inserta en un sitio de inserción de E1b- 19K, en el que dicho sitio de inserción […]
Composiciones de SYN3 y métodos, del 12 de Junio de 2019, de MERCK SHARP & DOHME CORP: Una composicion farmaceutica liofilizada que comprende N-(3-colamidopropil)-N-(3(actobionamidopropil))-colamida (SYN3), hidroxipropil-beta-ciclodextrina (HPßCD) y un sistema […]