ACTIVACION Y PRODUCCION DE PARTICULAS RADIOMARCADAS.
Partícula radiomarcada para la utilización radiofarmacéutica interna,
tal como una nanopartícula o micropartícula, que comprende tanto radionúclidos emisores ß- adecuados para la terapia del cáncer como radionúclidos emisores ß+ adecuados para la formación de imágenes médicas nuclear
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/050222.
Solicitante: THE EUROPEAN ATOMIC ENERGY COMMUNITY (EURATOM), REPRESENTED BY THE EUROPEAN COMMISSION.
Nacionalidad solicitante: Bélgica.
Dirección: 200, RUE DE LA LOI,1049 BRUSSELS.
Inventor/es: SOMERS, JOSEPH, APOSTOLIDIS, CHRISTOS, MAGILL, JOSEPH, GALY,JEAN, JEHENSON,PHILIPPE.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- A61K41/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales obtenidas por tratamiento de sustancias mediante energía ondulatoria o por radiación corpuscular.
- A61K41/00K
- A61K51/12H
- G21G1/12 FISICA. › G21 FISICA NUCLEAR; TECNICA NUCLEAR. › G21G CONVERSION DE ELEMENTOS QUIMICOS; FUENTES RADIACTIVAS. › G21G 1/00 Disposiciones para la conversión de los elementos químicos por radiación electromagnética, radiación corpuscular o bombardeo por partículas, p. ej. producción de isótopos radiactivos (por reacciones termonucleares G21B; conversión de combustible nuclear G21C). › por irradiación electromagnética, p. ej. rayos gamma o rayos X (dispositivos de irradiación G21K 5/00).
- G21H5/02 G21 […] › G21H OBTENCION DE ENERGIA A PARTIR DE FUENTES RADIACTIVAS; APLICACIONES DE LA RADIACION DE FUENTES RADIACTIVAS NO PREVISTAS EN OTRO LUGAR; UTILIZACION DE LOS RAYOS COSMICOS (medición de la radiación nuclear o de rayos X G01T; reactores de fusión G21B; reactores nucleares G21C; lámparas con atmósfera gaseosa llevada a la luminiscencia por una radiación corpuscular exterior o por un material radioactivo asociado estructuralmente a la lámpara H01J 65/04, H01J 65/06). › G21H 5/00 Aplicación de radiaciones de fuentes radiactivas o disposiciones a este efecto no previstas en otro lugar. › como trazadores.
Clasificación PCT:
- A61K41/00 A61K […] › Preparaciones medicinales obtenidas por tratamiento de sustancias mediante energía ondulatoria o por radiación corpuscular.
Clasificación antigua:
- A61K41/00 A61K […] › Preparaciones medicinales obtenidas por tratamiento de sustancias mediante energía ondulatoria o por radiación corpuscular.
Fragmento de la descripción:
Activación y producción de partículas radiomarcadas.
Campo de la invención
La presente invención se refiere generalmente a la activación y la producción de partículas radiomarcadas para la utilización radiofarmacéutica interna.
Antecedentes de la invención
Actualmente se utilizan partículas radiomarcadas para dos aplicaciones radiofarmacéuticas principales: radioterapia interna y formación de imágenes médicas nuclear.
Como es bien conocido, las partículas radiomarcadas de este tipo están constituidas generalmente por radionúclidos combinados con materiales portadores. Sus dimensiones varían desde unos cuantos nanómetros hasta varios cientos de micrómetros y las partículas son generalmente de forma esférica. Por tanto, con frecuencia se denominan micropartículas, microesferas, nanopartículas, perlas o microcápsulas.
Se han desarrollado muchos tipos diferentes de nano- y micropartículas. El material portador puede basarse en polímeros, resinas poliméricas, albúmina, o materiales inorgánicos tales como por ejemplo vidrio. La elección del radionúclido depende de la utilización prevista de la partícula radiomarcada. Para radioterapia, el radionúclido debe presentar un espectro de radiación apropiado para tratar múltiples tumores de pequeños a grandes. Generalmente, se utilizan emisores ß-. Para la formación de imágenes médicas nuclear, el radionúclido debe ser un emisor ß+, de modo que puedan detectarse los rayos ? producidos por el proceso de aniquilación, para los fines de la formación de imágenes.
La preparación de micro- y nanopartículas radiomarcadas se ha descrito ampliamente en la bibliografía científica y de patentes. En la mayoría de los procedimientos, se preparan partículas que comprenden núclidos precursores estables combinados con material portador, y las partículas se activan posteriormente en un reactor nuclear mediante bombardeo con neutrones. En algunos procedimientos, en primer lugar se producen los radionúclidos, y entonces se forman las partículas combinando los radionúclidos con el material portador.
Una desventaja de estos procedimientos es que requieren un reactor nuclear para activar el núclido precursor para dar el radioisótopo adecuado para radioterapia o formación de imágenes.
El documento DE 10037439 describe un procedimiento para activar yodo, en el que se irradia yodo-127 mediante neutrones. Los neutrones de irradiación se generan mediante un material moderador, excitado mediante un neutrón emitido por el material berilio con irradiación mediante fotones producidos por un rayo láser que incide sobre un hilo de tántalo.
Los documentos JP 05-208919, JP 07-222804, WO86/03 124 y la patente US nº 5.342.283 describen la activación de microesferas, por ejemplo microesferas de vidrio, mediante irradiación de neutrones.
Objetivo de la invención
El objetivo de la presente invención consiste en proporcionar un modo alternativo de preparación de partículas radiomarcadas para utilización radiofarmacéutica. Este objetivo se consigue mediante un procedimiento según se reivindica en la reivindicación 1.
Sumario de la invención
Según un aspecto, la presente invención propone un procedimiento para activar partículas para utilización radiofarmacéutica interna, comprendiendo las partículas núclidos precursores que van a activarse. Según la invención, el procedimiento comprende:
dirigir un rayo láser de alta intensidad sobre unos medios de conversión para producir un campo de irradiación de fotones bremsstrahlung; e
irradiar las partículas que comprenden núclidos precursores en el campo de irradiación para activar los núclidos precursores, obteniéndose así partículas radiomarcadas.
Se apreciará que el presente procedimiento utiliza un láser para producir el campo de irradiación que inducirá las reacciones nucleares requeridas para activar los núclidos precursores. Esto elimina la necesidad de un reactor nuclear. La interacción del rayo láser de alta intensidad con los medios de conversión produce un campo de irradiación de alta energía de fotones. La utilización de un rayo láser para activar partículas tales como microesferas y nanopartículas en vez de un reactor nuclear demuestra ser extremadamente ventajoso, en cuanto a costes, tamaño, funcionamiento y mantenimiento. Los denominados láseres de sobremesa son muy compactos y son particularmente adecuados para su instalación en hospitales. Por tanto, el presente procedimiento puede implementarse fácilmente en hospitales u otros centros de tratamiento mediante radioterapia, sin depender de reactores nucleares alejados.
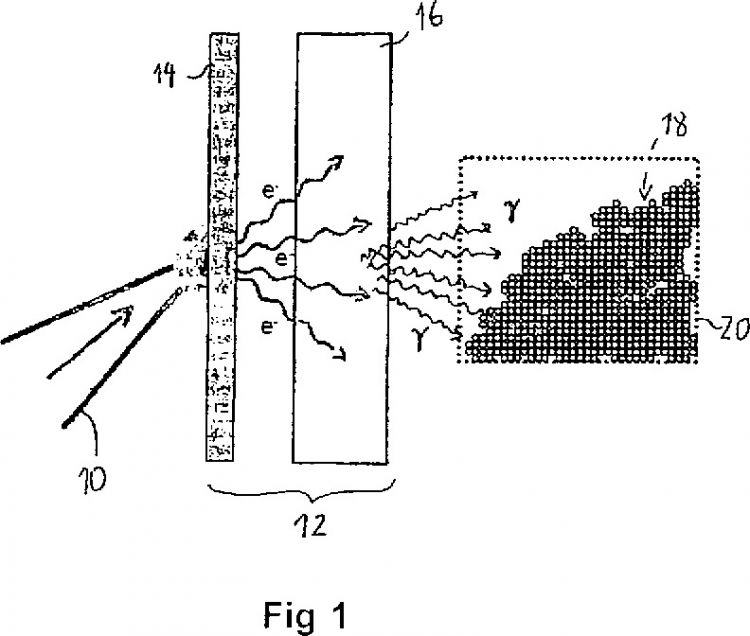
El campo de irradiación es un campo de fotones bremsstrahlung. Por tanto, los medios de conversión preferentemente incluyen un objetivo sólido, tal como por ejemplo una lámina metálica. Más preferentemente, los medios de conversión incluyen una primera parte de objetivo sobre la que se enfoca el rayo láser, produciendo así electrones de alta energía. Una segunda parte de objetivo está situada detrás del primer objetivo y los electrones de alta energía inciden sobre el mismo, de modo que actúa como un conversor de fotones bremsstrahlung que produce fotones de alta energía. La producción de fotones permite así la inducción de reacciones fotonucleares (indicado como (?, n)) en las partículas. La absorción de radiación electromagnética de alta energía en forma de fotones de rayos gamma, producidos por la interacción del rayo láser con los medios de conversión, hace que un núclido precursor expulse un neutrón, provocando la formación de un isótopo radiactivo del mismo elemento.
Los materiales preferidos para el objetivo metálico, respectivamente las primera y segunda partes de objetivo, son tántalo, wolframio, platino o cobre.
El presente procedimiento permite la activación de cualquier partícula adecuada para utilización radiofarmacéutica, que comprenda núclidos precursores que puedan activarse a través de reacciones (?, n). En particular, el procedimiento permite la activación de partículas que comprenden como núclidos precursores un isótopo estable de un elemento de la lista siguiente: Ag, Au, Br, C, Cd, Ce, Cl, Cr, Cu, Er, Eu, F, Fe, Ga, Gd, Ge, l, In, lr, K, Kr, Lu, Mo, N, Nd, Ni, O, Os, P, Pd, Pr, Pt, Rb, Re, Ru, Sb, Sc, Se, Sm, Sn, Te, Ti, W, Xe, Yb, Zn. La irradiación de isótopos estables de estos elementos con fotones producirá así radionúclidos que presentan espectros de radiación apropiados para su utilización médica.
Para la terapia del cáncer, resultan preferidas la partículas marcadas con un radionúclido emisor ß-. Una lista preferida de radionúclidos adecuados es la siguiente: 70Ga, 75Ge, 80Br, 81Se, 81mSe, 85mKr, 86Rb, 99Mo, 103Ru, 108Ag, 109Pd, 109mPd, 114mIn, 115Cd, 121Sn, 122Sb, 127Te, 129Te, 133Xe, 135Xe, 141Ce, 147Nd, 149Nd, 153Sm, 152mEu, 159Gd, 169Er, 175Yb, 176mLu, 185W, 186Re, 191Os, 192Ir, 197Pt, 197mPt. De ahí que para producir partículas marcadas con los radionúclidos anteriores a través de reacciones (?, n) con el presente procedimiento, las partículas que van a irradiarse deben comprender normalmente como núclidos precursores un isótopo estable del mismo elemento que el radionúclido deseado, con un número másico superior en una unidad al número másico del radionúclido deseado.
Para la formación de imágenes médicas nuclear, se prefieren partículas marcadas con emisores de positrones (ß+). Los núclidos emisores ß+ interaccionan con electrones mediante un proceso de aniquilación, que da como resultado la producción de dos fotones de 0,511 MeV que pueden detectarse, por ejemplo, mediante cámaras de tomografía por emisión de positrones. Una lista preferida de radionúclidos adecuados es la siguiente: 11C, 13N, 15O, 18F, 30P, 34mCl, 38K, 44Sc, 45Ti, 49Cr, 53Fe, 57Ni, 62Cu, 64Cu, 63Zn, 88Ga, 69Ge, 78Sr, 84Rb, 95Ru, 101Pd, 106Ag, 105Cd, 112ln, 120Sb, 126I,...
Reivindicaciones:
1. Partícula radiomarcada para la utilización radiofarmacéutica interna, tal como una nanopartícula o micropartícula, que comprende tanto radionúclidos emisores ß- adecuados para la terapia del cáncer como radionúclidos emisores ß+ adecuados para la formación de imágenes médicas nuclear.
2. Partícula radiomarcada según la reivindicación 1, que comprende un radionúclido emisor ß- seleccionado de entre la lista que comprende; 70Ga, 69Zn, 75Ge, 80Br, 85mKr, 99Mo, 109Pd, 115Cd, 122Sb, 149Nd y 169Er; y un radionúclido emisor ß+ seleccionado de entre la lista que comprende 68Ga, 63Zn, 69Ge, 78Br, 79Kr, 91Mo, 101Pd, 105,107Cd, 120Sb, 141Nd y 165Er.
3. Partícula radiomarcada según la reivindicación 1, que comprende una pareja de radionúclidos emisores ß- y ß+ del mismo elemento.
4. Partícula radiomarcada según la reivindicación 1, 2 ó 3, en la que las dimensiones de dichas partículas están en el intervalo de 10 nm a 500 µm, preferentemente de 1 a 100 µm.
5. Partícula radiomarcada según cualquiera de las reivindicaciones 1 a 4, en la que dichos radionúclidos se combinan con material portador.
6. Partícula radiomarcada según cualquiera de las reivindicaciones 1 a 5, en la que dichas partículas son insolubles en medios celulares.
7. Procedimiento para activar micro- y/o nanopartículas para la utilización radiofarmacéutica interna, comprendiendo dichas partículas núclidos precursores que van a activarse, caracterizado porque presenta
la dirección de un rayo láser de alta intensidad sobre unos medios de conversión para producir un campo de irradiación de fotones bremmstrahlung; y
la irradiación de dichas partículas que comprenden núclidos precursores en dicho campo de irradiación de fotones bremmstrahlung para activar dichos núclidos precursores, obteniéndose así las partículas radiomarcadas.
8. Procedimiento según la reivindicación 7, caracterizado porque dichos medios de conversión incluyen un objetivo metálico.
9. Procedimiento según la reivindicación 8, caracterizado porque dichos medios de conversión comprenden una primera parte de objetivo sobre la que se enfoca dicho rayo láser y una segunda parte de objetivo detrás de la primera parte de objetivo que actúa como conversor de fotones bremmstrahlung.
10. Procedimiento según la reivindicación 8 ó 9, caracterizado porque dicho objetivo metálico, respectivamente las partes de objetivo, están realizadas por tántalo, wolframio, platino o cobre.
11. Procedimiento según cualquiera de las reivindicaciones 7 a 10, caracterizado porque cada partícula comprende como núclido precursor un isótopo estable seleccionado de un elemento seleccionado de entre el grupo que comprende Ag, Au, Br, C, Cd, Ce, Cl, Cr, Cu, Er, Eu, F, Fe, Ga, Gd, Ge, I, In, Ir, K, Kr, Lu, Mo, N, Nd, Ni, O, Os, P, Pd, Pr, Pt, Rb, Re, Ru, Sb, Sc, Se, Sm, Sn, Te, Ti, W, Xe, Yb, Zn, o combinaciones de los mismos.
12. Procedimiento según cualquiera de las reivindicaciones 7 a 11, caracterizado porque dichas partículas radiomarcadas activadas comprenden radionúclidos seleccionados de entre el grupo que comprende: 70Ga, 75Ge, 80Br, 81Se, 81mSe, 85mKr, 86Rb, 99Mo, 103Ru, 108Ag, 109Pd, 109mPd, 114mIn, 115Cd, 121Sn, 122Sb, 127Te, 129Te, 133Xe, 135Xe, 141Ce, 147Nd, 149Nd, 153Sm, 152mEu, 159Gd, 169Er, 175Yb, 176mLu, 185W, 186Re, 191Os, 192Ir, 197Pt, 197mPt, 11C, 13N, 15O, 18F, 30P, 34mCl, 38K, 44Sc, 45Ti, 49Cr, 53Fe, 57Ni, 62Cu, 64Cu, 63Zn, 68Ga, 69Ge, 78Br, 84Rb, 95Ru, 101Pd, 106Ag, 105Cd, 112In, 120Sb, 126I, 140Pr, 141Nd, 190nIr, 196Au, o combinaciones de los mismos.
13. Procedimiento según cualquiera de las reivindicaciones 7 a 12, caracterizado porque dicho rayo láser que incide sobre dichos medios de conversión presenta una intensidad de por lo menos 1019 W/cm2, preferentemente de aproximadamente 1020 W/cm2 y superior.
14. Procedimiento según cualquiera de las reivindicaciones 7 a 13, caracterizado porque dichas partículas están en una forma química que es insoluble en medios celulares.
15. Procedimiento según cualquiera de las reivindicaciones 7 a 14, caracterizado porque cada una de dichas partículas que van a activarse son partículas de un isótopo estable en una forma química que es insoluble en medios celulares.
16. Procedimiento según cualquiera de las reivindicaciones 7 a 15, caracterizado porque dichas partículas que comprenden núclidos precursores se forman combinando núclidos precursores con material portador.
17. Procedimiento según cualquiera de las reivindicaciones 7 a 16, caracterizado porque cada una de dichas partículas comprende un núclido precursor estable que se activará en un radionúclido emisor ß- así como otro núclido precursor estable que se activará en un radionúclido emisor ß+.
18. Procedimiento según la reivindicación 17, caracterizado porque cada partícula que va a activarse comprende un núclido precursor seleccionado de entre la lista que comprende: 71Ga, 70Zn, 76Ge, 81Br, 86Kr, 100Mo, 110Pd, 116Cd, 123Sb, 150Nd y 170Er; y un núclido precursor seleccionado de entre la lista que comprende: 69Ga, 64Zn, 70Ge, 79Br, 80Kr, 92Mo, 102Pd, 106,108Cd, 121Sb, 142Nd y 166Er.
19. Procedimiento según la reivindicación 17, caracterizado porque cada partícula que va a activarse comprende parejas de núclidos precursores seleccionados de entre la lista siguiente: (69Ga; 71Ga), (64Zn; 70Zn), (70Ge; 76Ge), (79Br, 81Br), (80Kr, 86Kr), (92Mo, 100Mo), (102Pd, 110Pd), (106,108Cd, 116Cd), (121Sb, 123Sb), (142Nd, 150Nd) y (166Er, 170Er).
20. Procedimiento según cualquiera de las reivindicaciones 7 a 19, caracterizado porque las dimensiones de dichas partículas están en el intervalo de 10 nm a 500 µm, preferentemente de 1 a 100 µm.
21. Procedimiento según cualquiera de las reivindicaciones 7 a 20, caracterizado porque dichas partículas que comprenden núclidos precursores se colocan en un recipiente durante la irradiación.
22. Procedimiento según cualquiera de las reivindicaciones 7 a 21, caracterizado porque se lleva a cabo en el lugar de utilización de dichas partículas radiomarcadas.
23. Procedimiento para producir partículas radiomarcadas para la utilización radiofarmacéutica interna, que comprende las etapas que consisten en:
proporcionar las partículas que comprenden núclidos precursores; y
activar dichas partículas para obtener las partículas radiomarcadas;
caracterizado porque dicha etapa de activación se lleva a cabo según el procedimiento reivindicado según cualquiera de las reivindicaciones 7 a 22.
24. Procedimiento según la reivindicación 23, caracterizado porque presenta la etapa que consiste en suspender las partículas radiomarcadas en un medio acuoso apropiado para inyección en el cuerpo de un paciente.
25. Partícula según cualquiera de las reivindicaciones 1 a 6, para su utilización como medicamento.
Patentes similares o relacionadas:
Composición farmacéutica basada en nanoestructura de grafeno para prevenir o tratar enfermedades neurodegenerativas, del 22 de Julio de 2020, de Seoul National University R & DB Foundation: Una composición farmacéutica para su uso en la prevención o el tratamiento de enfermedades neurodegenerativas, que comprende puntos cuánticos de grafeno como […]
Sistema para el tratamiento o la prevención por termoterapia de infecciones resistentes a antimicrobianos o por biopelículas, del 6 de Mayo de 2020, de FUNDACIÓ HOSPITAL UNIVERSITARI VALL D'HEBRON - INSTITUT DE RECERCA: Un sistema para el tratamiento por termoterapia o la prevención de infecciones resistentes a antimicrobianos o por biopelículas, comprendiendo el sistema: - […]
Soluciones hipoosmóticas para la detección de ganglios linfáticos, del 29 de Abril de 2020, de Endomagnetics Ltd: Una suspensión hipoosmótica para uso en el diagnóstico de cáncer, siendo la suspensión hipoosmótica una solución acuosa que tiene una osmolalidad de 80 […]
Formulaciones para su uso en el tratamiento de afecciones de la piel, del 1 de Abril de 2020, de Soligenix, Inc: Formulación líquida para su uso en el tratamiento tópico de una afección de la piel seleccionada del grupo que consiste en linfoma de células T cutáneo (LCTC) y psoriasis, que […]
Canalrodopsinas para el control óptico de células, del 1 de Abril de 2020, de MASSACHUSETTS INSTITUTE OF TECHNOLOGY: Polipéptido de canal iónico activado por luz aislado que comprende una secuencia de aminoácidos de un polipéptido de canal de Stigeoclonium […]
Método y dispositivo para producir micro/nano-burbujas a base de lípidos optimizadas, del 11 de Marzo de 2020, de Trust Bio-sonics Inc: Un método para producir micro/nano burbujas a base de lípidos, que comprende etapas de: preparar una mezcla lipídica que comprende […]
Método para el tratamiento del acné, del 12 de Febrero de 2020, de DUSA PHARMACEUTICALS, INC.: Un agente fotodinámico para usar en un método para tratar el acné en una persona que necesita dicho tratamiento, el método comprende: […]
VACUNACIÓN CON MICROVESÍCULAS DERIVADAS DE CÉLULAS TUMORALES PARA TRATAMIENTO DE CÁNCER, del 6 de Febrero de 2020, de PINEDA OLVERA, Benjamín: La presente invención se refiere a microvesículas provenientes de células tumorales naturales y producidas in vitro bajo un estímulo estresor, tal como la radiación, las […]