Endoprótesis endovascular para la administración de fármacos.
Una endoprótesis vascular para su colocación en un lugar de lesión vascular con el fin de inhibir allí la restenosis.
La endoprótesis comprende un miembro estructural o cuerpo formado por uno o más filamentos y, sobre el filamento(s) del cuerpo de la endoprótesis, una cubierta liberadora de fármaco compuesta de a) un 20-60% del peso de sustrato de polímero y b) un 40-80% del peso de un compuesto inmunodepresor trieno macrocíclico, en el que el sustrato de la cubierta comprende un polímero de ácido poliláctico.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E12191560.
Solicitante: BIOSENSORS INTERNATIONAL GROUP, LTD.
Nacionalidad solicitante: Bermuda.
Dirección: Clarendon House, 2 Church Street Hamilton HM 11 BERMUDAS.
Inventor/es: SAVAGE,DOUGLAS,R, BETTS,RONALD,E, SHULZE,JOHN,E.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00).
- A61F2/90 A61F […] › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › caracterizados por una estructura en forma de red o malla.
- A61F2/91 A61F 2/00 […] › fabricadas a partir de hojas perforadas o tubos, p.ej. perforados por corte con laser o taladros grabados.
- A61K31/4353 A61 […] › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados en orto o en peri con sistemas heterocíclicos.
- A61K31/436 A61K 31/00 […] › conteniendo el sistema heterocíclico un ciclo de seis eslabones teniendo el oxígeno como heteroátomo del ciclo, p. ej. rapamicina.
- A61K47/34 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/06 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Ungüentos; Excipientes para éstos (aparatos para su fabricación A61J 3/04).
- A61K9/10 A61K 9/00 […] › Dispersiones; Emulsiones.
- A61K9/20 A61K 9/00 […] › Píldoras, pastillas o comprimidos.
- A61K9/70 A61K 9/00 […] › Bases para tiras, hojas o filamentos.
- A61L31/00 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › Materiales para otros artículos quirúrgicos.
- A61L31/08 A61L […] › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales para revestimientos.
- A61L31/10 A61L 31/00 […] › Materiales macromoleculares.
- A61L31/16 A61L 31/00 […] › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
- A61P17/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 17/00 Medicamentos para el tratamiento de problemas dermatológicos. › para tratar heridas, úlceras, quemaduras, cicatrices, queloides o similares.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- A61P35/00 A61P […] › Agentes antineoplásicos.
- A61P9/10 A61P […] › A61P 9/00 Medicamentos para el tratamiento de trastornos en el aparato cardiovascular. › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
- A61P9/14 A61P 9/00 […] › Vasoprotectores; Antihemorroidales; Medicamentos para el tratamiento de las varices; Estabilizadores capilares.
- C07D498/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › Sistemas puenteados.
PDF original: ES-2514391_T3.pdf

Fragmento de la descripción:
Endoprótesis endovascular para la administración de fármacos Ã?mbito de la invención La presente invención se refiere a una endoprótesis endovascular liberadora de fármaco.
Antecedentes de la invención 5
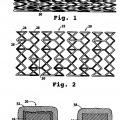
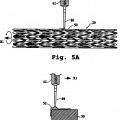
Una endoprótesis es un tipo de implante endovascular, habitualmente de forma tubular, que tiene una construcción tubular conectada con cable en forma de enrejado típica que es expansible para poderse insertarse de forma permanente dentro de un vaso sanguíneo con el fin de proporcionar apoyo mecánico al vaso y mantener o restablecer un canal de flujo durante o después de una angioplastia. La estructura de apoyo de la endoprótesis está diseñada para impedir un colapso temprano de un vaso que se ha debilitado 10 o dañado por la angioplastia.
Se ha demostrado que la inserción de las endoprótesis impide la reestructuración negativa y el espasmo del vaso mientras tiene lugar la cicatrización de la pared vascular dañada a lo largo de unos meses.
Durante el proceso de cicatrización, la inflamación causada por la angioplastia y el implante de la 15 endoprótesis provoca a menudo una proliferación de células musculares lisas y un nuevo crecimiento dentro de la endoprótesis, lo que cierra parcialmente el canal de flujo, y por tanto reduce o elimina el efecto beneficioso de la intervención de la angioplastia y de la colocación de la endoprótesis. Este proceso se denomina restenosis. También pueden formarse coágulos sanguíneos dentro de una endoprótesis recién implantada debido a la naturaleza trombótica de sus superficies, incluso cuando se utilizan materiales 20 biocompatibles para construirla.
Aunque pueden no formarse coágulos sanguíneos grandes durante la realización de la angioplastia o inmediatamente después debido a la práctica actual de inyectar fármacos antiagregantes potentes en la circulación sanguínea, siempre se produce algo de trombosis, al menos a nivel microscópico, en las superficies de la endoprótesis, y se cree que interviene de forma significativa en los primeros estadios de la 25 restenosis al establecer una matriz biocompatible en las superficies de las endoprótesis a las que las células musculares lisas pueden después unirse y en las que puede multiplicarse.
Se conocen cubiertas de endoprótesis que contienen sustancias bioactivas diseñadas para reducir o eliminar la trombosis o la restenosis. Tales sustancias bioactivas pueden estar dispersas o disueltas en una matriz de polímero bioduradera o bioerosionable que se une a la superficie de los filamentos de la 30 endoprótesis antes de su implantación. Tras la implantación, la sustancia bioactiva se difunde de la matriz de polímero y de forma preferente hacia el tejido vecino durante un período de al menos cuatro semanas y en algunos casos de hasta un año o más, lo que se corresponde de forma ideal con la evolución temporal de la restenosis, la proliferación de las células musculares lisas, la trombosis o una combinación de ellas.
Si el polímero es bioerosionable, además de liberar el fármaco por medio del proceso de difusión, 35 la sustancia bioactiva también puede liberarse a medida que el polímero se degrada o disuelve, lo que deja la sustancia más fácilmente disponible para el ambiente tisular ambiental. Se conocen endoprótesis bioerosionables y bioduraderas en las que las superficies externas o incluso todo el volumen del material de polímero es poroso. Por ejemplo, la publicación PCT nº WO 99/07308, que suele acompañar a la presente aplicación, revela tales endoprótesis. Cuando los polímeros bioerosionables se utilizan como cubiertas 40 liberadoras de fármacos, se reivindica en algunos casos que la porosidad ayuda al crecimiento del tejido hacia el interior, hace la erosión del polímero más predecible o regula o potencia la liberación del fármaco, como, por ejemplo, se revela en las patentes estadounidenses nº 6.099.562, 5.873.904, 5.342.348, 5.873.904, 5.707.385, 5.824.048, 5.527.337, 5.306.286 y 6.013.853.
Se sabe que la heparina, así como otras cubiertas superficiales antiagregantes o antitrombóticas, 45 se unen mediante enlaces químicos a la superficie de la endoprótesis para reducir la trombosis. Se sabe que una superficie heparinizada interfiere con la cascada de la coagulación sanguínea en los seres humanos, al evitar la unión de las plaquetas (precursor de la trombina) a la superficie de la endoprótesis. Se han descrito endoprótesis que incluyen una heparina en la superficie y una sustancia activa almacenada dentro de una cubierta (v. patentes estadounidenses nº 6.231.600 y 5.288.711, por ejemplo) . 50
Se han propuesto varias sustancias que reivindican de forma específica inhibir la proliferación de la célula muscular lisa y así inhibir la restenosis para ser liberadas de las endoprótesis endovasculares. Por ejemplo, la patente estadounidense nº 6.159.488 describe el uso de un derivado quinazolinona; la patente estadounidense nº 6, 171, 609, el uso de taxol; y la patente estadounidense nº 5.176.980, el uso de paclitaxel, un fármaco citotóxico considerado el ingrediente activo del taxol. El metal plata se cita en la 55
patente estadounidense nº 5.873.904. El tranilast, un fármaco estabilizador de la membrana que se cree tiene propiedades antinflamatorias, se reivindica en la patente estadounidense nº 5.733.327.
Se ha demostrado que la rapamicina, un inmunodepresor que suprime el crecimiento de las células musculares lisas y endoteliales, mejora la eficacia contra la restenosis cuando se libera de una cubierta de polímero de una endoprótesis. Vea, por ejemplo, las patentes estadounidenses nº 5.288.711 y 6.153.252. 5 Además, en la publicación PCT nº WO 97/35575, se han propuesto el compuesto inmunodepresor trieno macrocíclico everolimus y compuestos relacionados para tratar la restenosis por medio de su administración sistémica.
La publicación europea EP0950386 propone una endoprótesis que comprende un cuerpo estructural formado por muchos filamentos y una cubierta liberadora de fármacos que incluye un compuesto 10 trieno macrocíclico mezclado con un polímero en solución con una concentración final entre el 0, 001% y el 30% de peso de un fármaco.
Un compuesto seleccionado para inhibir la restenosis, mediante la liberación del fármaco de una endoprótesis, debe tener de forma ideal tres propiedades. Primera, como la endoprótesis debe tener un perfil bajo, lo que se traduce en una matriz de polímero fina, el compuesto debe ser suficientemente activo 15 para producir una dosis terapéutica continua durante un período mínimo de 4-8 semanas cuando se libera de una cubierta de polímero fina. Segundo, el compuesto debe inhibir, a una dosis baja, la proliferación de las células musculares lisas. Finalmente, las células endoteliales que recubren la superficie interna de la luz vascular están normalmente dañadas por el proceso de la angioplastia y colocación de la endoprótesis. El compuesto debe permitir el nuevo crecimiento de las células endoteliales dentro de la luz del vaso, con el 20 fin de proporcionar el retorno de la homeostasis vascular y promover interacciones normales y cruciales entre las paredes vasculares y el flujo de sangre a través del vaso.
Resumen de la invención
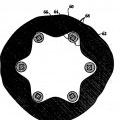
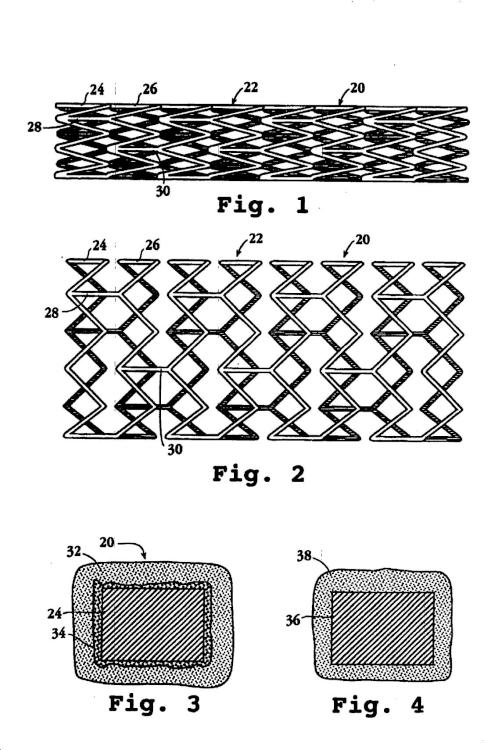
Un ejemplo incluye, en un aspecto, una endoprótesis vascular que se coloca en el lugar de la lesión vascular con el fin de inhibir allí la restenosis. La endoprótesis se construye de un miembro 25 estructural o cuerpo formado de uno o más filamentos y, sobre el filamento (s) del cuerpo de la endoprótesis, una cubierta liberadora de fármaco bioerosionable con un espesor de 3 a 15 micrones compuesta de a) un 20 y 60% del peso de sustrato de polímero de poli-dl-láctido y b) un 40-80% del peso de compuesto contra la restenosis. Una capa de imprimación de polímero con un espesor de 1 a 5 micrones y dispuesta entre los filamentos del cuerpo de la endoprótesis y la cubierta ayuda a estabilizar la cubierta en los filamentos de la 30 endoprótesis. La endoprótesis es expansible desde un estado contraído en el que la endoprótesis puede llevarse hasta un lugar de lesión vascular con un catéter a un estado expandido en el que la cubierta de la endoprótesis puede colocarse en contacto con el vaso en la zona de la lesión. La cubierta de la endoprótesis libera una cantidad inhibidora de la restenosis de un compuesto a lo largo de un período de al menos 4 semanas tras su colocación en el lugar de la lesión vascular. 35
En las diversas realizaciones de la invención, el compuesto contra la restenosis es un compuesto inmunodepresor trieno macrocíclico, el cuerpo de la endoprótesis puede ser una estructura de filamentos metálicos, puede formarse una capa de imprimación de un polímero... [Seguir leyendo]
Reivindicaciones:
1. Una endoprótesis vascular para su colocación en un lugar de lesión vascular con el fin de inhibir allí la restenosis. La endoprótesis comprende un miembro estructural o cuerpo formado por uno o más filamentos y, sobre el filamento (s) del cuerpo de la endoprótesis, una cubierta liberadora de fármaco compuesta de a) u.
2. 60% del peso de sustrato de polímero y b) u.
4. 80% del peso de un compuesto 5 inmunodepresor trieno macrocíclico, en el que el sustrato de la cubierta comprende un polímero de ácido poliláctico.
2. Una endoprótesis de acuerdo con la reivindicación 1 donde el sustrato de polímero de ácido poliláctico es un copolímero.
3. Una endoprótesis de acuerdo con la reivindicación 2 donde el sustrato de ácido poliláctico 10 es un copolímero que comprende ácido poliláctico y uno entre el grupo seleccionado de EVOH, ε-caprolactona, EVA, PVA y PEO.
4. Una endoprótesis de acuerdo con la reivindicación 3 donde el sustrato de polímero de ácido poliláctico es un copolímero que comprende ácido poliláctico y ε-caprolactona.
5. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde el 15 cuerpo de la endoprótesis es un metal.
6. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde la cubierta liberadora de fármaco tiene un espesor de 3 a 25 micrones.
7. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde el compuesto inmunodepresor trieno macrocíclico tiene la fórmula: 20
donde R es H o CH2-X-OH y X es un grupo lineal que contiene 1 a 7 átomos de carbono.
8. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde el sustrato de la cubierta está formado por poli-dl-láctido.
9. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes que no 25 contiene ninguna capa entre los filamentos de la endoprótesis y la cubierta liberadora de fármaco.
10. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde la cubierta liberadora de fármaco cubre los filamentos por todos los lados.
11. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde la capa liberadora del fármaco tiene un espesor de 3-20 micrones. 30
12. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde la superficie interna del cuerpo de la endoprótesis está cubierta de una segunda capa liberadora de fármaco que contiene un segundo fármaco.
13. Una endoprótesis de acuerdo con cualquiera de las reivindicaciones precedentes donde la 35 profundidad de la capa mencionada en la superficie superior del filamento no es uniforme.
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Régimen de terapia y métodos para sensibilizar células de cáncer tratadas con una terapia epigenética frente a inhibidores de PARP en múltiples cánceres, del 22 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una combinación que comprende un agente desmetilante del ADN y un inhibidor de poli ADP ribosa polimerasa (PARP) para su uso en el tratamiento del cáncer, en […]