Compuestos antineoplásicos y composiciones farmacéuticas de los mismos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CU2006/000002.
Solicitante: CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA.
Nacionalidad solicitante: Cuba.
Dirección: Ave. 31 entre 158 y 190 Cubanacan, Playa Ciudad de La Habana 10600 CUBA.
Inventor/es: ACEVEDO CASTRO, BORIS ERNESTO, MUSACCHIO LASA, ALEXIS, PEREA RODRIGUEZ,SILVIO,ERNESTO, UBIETA GÓMEZ,Raimundo, RODRÍGUEZ FERNÁNDEZ,ROLANDO EDUARDO, DE LA NUEZ VEULENS,ANIA, VERA ÁLVAREZ,ROBERTO, MAZOLA REYES,YULIET.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C237/30 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 237/00 Amidas de ácidos carboxílicos, estando sustituida la estructura carbonada de la parte ácida por grupos amino. › con el átomo de nitrógeno del grupo carboxamido unido a átomos de hidrógeno o a átomos de carbono acíclicos.
- C07C275/18 C07C […] › C07C 275/00 Derivados de urea, es decir, compuestos que contienen uno de los grupos en que los átomos de nitrógeno no forman parte de grupos nitro o nitroso. › de una estructura carbonada que contiene ciclos.
- C07C275/22 C07C 275/00 […] › que contiene ciclos que no son ciclos aromáticos de seis miembros.
- C07C275/36 C07C 275/00 […] › con al menos uno de los átomos de oxígeno unido además a un átomo de carbono de un ciclo aromático de seis miembros, p. ej. N-ariloxifenilureas.
- C07C313/06 C07C […] › C07C 313/00 Acidos sulfínicos; Acidos sulfénicos; Sus halogenuros, ésteres o anhídridos; Amidas de ácidos sulfínicos o sulfénicos, es decir, compuestos en los que átomos de oxígeno, unidos por enlaces sencillos, de grupos sulfínicos o sulfénicos han sido sustituidos por átomos de nitrógeno que no forman parte de grupos nitro o nitroso. › Sulfinamidas.
- C07C327/44 C07C […] › C07C 327/00 Acidos tiocarboxílicos. › a átomos de carbono de una estructura carbonada insaturada.
- C07D207/36 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Atomos de oxígeno o azufre.
- C07D213/82 C07D […] › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › en posición 3.
- C07D215/18 C07D […] › C07D 215/00 Compuestos heterocíclicos que contienen quinoleína o quinoleína hidrogenada en el sistema cíclico. › Atomos de halógeno o radicales nitro.
- C07D233/54 C07D […] › C07D 233/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, no condensados con otros ciclos. › que tienen dos enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos.
- C07D235/14 C07D […] › C07D 235/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, condensados con otros ciclos. › Radicales sustituidos por átomos de nitrógeno (por radicales nitro C07D 235/10).
- C07D239/36 C07D […] › C07D 239/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,3 o diazina-1,3 hidrogenada. › como átomo de oxígeno enlazado doblemente o como un radical hidroxi insustituido.
- C07D239/42 C07D 239/00 […] › Un átomo de nitrógeno (radicales nitro C07D 239/30).
- C07D487/04 C07D […] › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
- C07F9/22 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 9/00 Compuestos que contienen elementos de los grupos 5 o 15 del sistema periódico. › Amidas de ácidos del fósforo.
PDF original: ES-2550959_T3.pdf
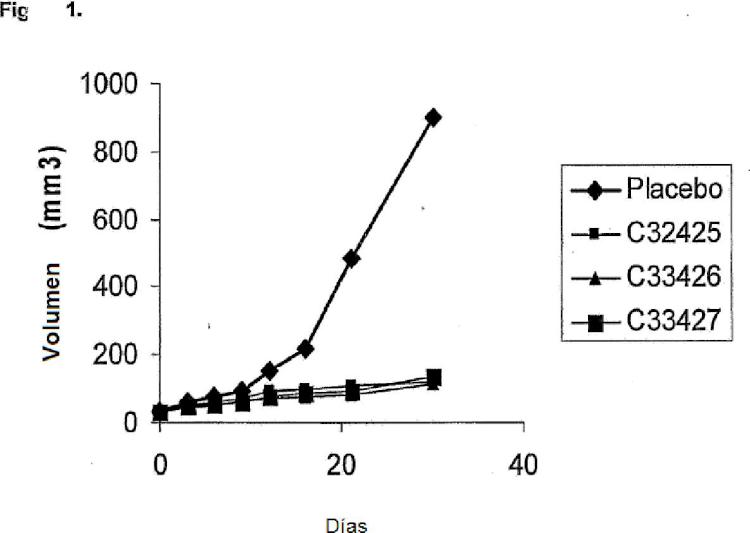
Fragmento de la descripción:
Compuestos antineoplásicos y composiciones farmacéuticas de los mismos Campo de la invención
La presente invención se puede describir en el campo de la farmacología molecular, particularmente en relación con oncología, y más específicamente con compuestos químicos obtenidos por modelado molecular in silico, que tiene una acción citotóxica clara y efecto antitumoral con base en su capacidad para bloquear el sitio aceptador de fosfato en sustratos de quinasa caseína 2, ya sea por interacción directa o indirecta.
Antecedentes
La quinasa caseína 2 (CK2) es una enzima de serina/treonina implicada en el aumento de la proliferación celular, siendo el núcleo su ubicación intracelular principal durante el proceso de transformación maligna (Tawfic S., Yu S., Wang H., et al. (2001) Protein kinase CK2 signal in neoplasia. Histol. Histopathol. 16:573-582). Más aún, algunas proteínas virales clave para el Virus de Inmunodeficiencia Humana patogénico (VIH) y Virus de Hepatitis C (HCV) se han reportado como sustratos CK2 (Meggio F., Marin O., et al. (2001) Mol Cell Biochem 227:145-151; Franck N., Le Seyec J., et al. (2005) Hepatitis C virus NS2 protein is phosphorylated by the protein kinase CK2 and targeted for degradation to the proteasome. J Virol. 79:2700-2008).
Los hallazgos de otros grupos en todo el mundo, también han confirmado la existencia de niveles elevados de CK2 en diferentes tumores sólidos de origen epitelial, en órdenes que varían de 3 a 7 veces más, respecto al tejido normal (Tawfic S., Yu S., et al. (2001) Protein kinase CK2 signal in neoplasia. Histol Histopatol. 16:573-582; Faust R.A., Gapany M., et al (1996) Elevated protein kinase CK2 activity in chromatin of head and necktumors: association with malignant transformation. Cáncer Letters 101:31-35), además de la actividad de fosforilación de la enzima CK2 es un evento muy importante en la transformación maligna de las células, constituye un fuerte marcador en la progresión del tumor (Seldin D.C., Leder P. (1995) Casein Kinase lia transgene-induced murine lymphoma: relation to theileroiosis in cattle. Science 267:894-897), la sobrexpresión de CK2 por otra parte conduce a la tumorigénesis de células mamarias por el aumento de la cascada de señalización Wnt/beta-catenina (Landesman-Bollag E., Romien-Mourez R., et al (2001) Protein Kinase CK2 in mammary gland tumorigenesis. Oncogene 20:3247-3257). Los recientes hallazgos también sugieren que el CK2 cumple una función esencial en algunos otros procesos como la remodelación de cromatina (Barz T., Ackenmann K., et al. (2003) Genome-wide expresslon screens Indícate a global role for protein kinase CK2 ¡n chromatin remodelllng. J Cell Sel. 116:1563-1577) y la regulación de la supervivencia celular (Unger G.M., Davls A.T., Slaton J.W., Ahmed K. (2004) Protein kinase CK2 as regulator of cell survlval: ¡mpllcatlons for cáncer therapy. Curr Cáncer Drug Targets, 4:77-84). De suma Importancia, para comprender el proceso de desarrollo del cáncer, han sido los hallazgos que demuestran que la fosforilación mediada por CK2 es una señal muy fuerte para la supervivencia celular, por lo tanto, se considera esta enzima como un mediador antlapoptótico de la fisiología celular (Ahmed K., Gerber D.A., Cochet C. (2002) Jolnlng the cell survival squad: an emerglng role for protein kinase CK2. Trends Cell Blol, 12:226-229; Torres J., Rodríguez J., et al (2003) Phosphorylatlon-regulated cleavage of the tumour suppressor PTEN by caspase-3: implications for the control of protein stablllty and PTEN-proteln ¡nteractlons. J Blol Chem, 278:30652-60).
Sobre la base de los hallazgos anteriores, se ha confirmado la fosforilación mediada por CK2 como un evento bioquímico, adecuado para ser utilizado como un objetivo potencial para la Intervención terapéutica en cáncer, haciendo a todos los inhibidores potenciales de dicho evento candidatos potenciales para el tratamiento de dicha afección. Hasta la fecha, diversos grupos de Investigación en todo el mundo han estado desarrollando diferentes estrategias para inhibir la fosforilación mediada por CK2 con dos enfoques experimentales: a) La inhibición directa de la enzima CK2, o b) el bloqueo del sitio de fosforilación cerca del dominio ácido descrito como común a todos los sustratos de CK2. Para ambos métodos, los autores han sido capaces de demostrar el concepto de que el evento inhibición de fosforilación mediada por CK2 conduce a la Inducción de apoptosis en las células tumorales, lo que implica una validación experimental de CK2 como un objetivo muy promisorio en el hallazgo de fármacos para tratamiento del cáncer.
Por ejemplo, se ha probado un Inhibidor directo de la enzima como el 4,5,6,7-tetrabromotriazol (TBB) como un potente inductor de degradación dependiente de caspasa y apoptosis en las células Jurkat, en el rango de concentración micromolar (Ruzzene M., Penzo D., Pinna L. (2002) Protein kinase CK2 inhibitor 4,5,6,7- tetrabromobenzotriazole (TBB) induces apoptosis and caspase-dependent degradation of haematopoietic lineage cell-specific protein 1 (HS1) in Jurkat cells. Biochem J., 364:41-47). También, al inhibir la expresión de la enzima CK2 al utilizar oligonucleótidos anticodificantes, un efecto apoptótico in vitro y se ha demostrado la acción antitumoral en un modelo de cáncer experimental en ratones (Guo C., Yu S., et al. (2001) A potential role of nuclear matrix-associated protein kinase CK2 in protection against drug-induced apoptosis in cáncer cells. J Blol Chem, 276:5992-5999; Slaton J.W., et al. (2004) Inductlon of apoptosis by antisense CK2 in human prostate cáncer xenograft model. Mol Cáncer Res. 2:712-721).
Otros compuestos, como los derivados de antraquinona, flavonoides y azobencilimidazoles halogenados, se han descrito como inhibidores de sitio de unión a ATP (Samo S., et al. (2002) Toward the rational design of protein kinase casein kinase-2 inhibitors. Pharmacol Therapeutics 93:159-168), y se ha reportado el ácido 5-oxo-5,6- dihidroindolo (1,2-a) quinazolin-7-ilo acético (IQA) como un inhibidor de CK2 selectivo utilizando detección de alto rendimiento (Vangrevelinghe E., et al. (2003) Biochemical and three-dimensional-structural study of the specific inhibition of protein kinase CK2 by [5-oxo-5,6-dihydroindolo-(1,2-a)quinazolin-7-yl]acetic acid (IQA). J. Med. Chem. 46:2556-2662).
Martínez. A. P., et al., (1967) describen un número de compuestos para actividades antivirales y antitumorales (Martínez. A., et al., J. MED. CHEM., vol. 10, 1967, page 1192). Sah. P. P. T., et al. (1950) describen la tiosemicarbazida como un reactivo para la identificación de aldehidos, cetonas, y quinonas (Sah. P. P. T., et al., Reel. Trav. Chim., vol. 69, 1950, pages 1545-1553).
Los compuestos mencionados anteriormente han mostrado su efecto inhibidor de actividad CK2 en el rango micromolar para la Concentración Inhibidora 50 (IC50), pero no se han reportado evidencias de ninguna acción antitumoral en modelos experimentales de cáncer.
El otro método descrito para inhibir el proceso de fosforilación mediada por CK2 ha sido el bloqueo del sitio de fosforilación dentro del dominio ácido encontrado en los sustratos de esta enzima. En la solicitud de patente WO 03/054002 y en el trabajo de Perea S.E et al. (2004) Antitumor effect of a novel proapoptotic peptide impairing the phosphorylation by the protein kinase CK2. Cáncer Res. 64:7127-7129, los autores proponen el uso de una familia de péptidos cíclicos que bloquean la fosforilación del sustrato CK2 in vitro, y muestran la citotoxicidad de células tumorales y el efecto antitumoral en modelos de cáncer de pre-clínicos. Sin embargo, los péptidos descritos en dichos informes tienen la limitación de no ser capaces per se de penetrar en las células, por lo que requieren un péptido de permeación de membrana que se fusiona a estas. En términos generales, cuando se compara con moléculas pequeñas, el uso de péptidos tiene los inconvenientes de una estabilidad in vivo reducida en la circulación, degradación, es muy difícil formular en administración oral y no se transportan fácilmente dentro de las células ((Ludger Wess, Isogenica: Improving peptides, Biocentury October 25, 2004). Otros problemas de péptidos ampliamente descritos en la literatura son el de la depuración más rápida, su potencial inmunogénico, y se sabe que su coste por dosis terapéutica es generalmente superior a los fármacos no peptídicos.
Resumen de la invención
Teniendo en cuenta las limitaciones potenciales del uso de los péptidos cíclicos mencionados anteriormente como agentes terapéuticos candidatos, la presente invención describe moléculas químicas capaces de inhibir la fosforilación mediada por CK2 mediante interacción directa o indirecta con el sitio aceptador... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto químico que bloquea la fosforilación mediada por Quinasa de Caseína 2 (CK2), para uso como un medicamento,
en donde el compuesto se selecciona de: (1Z)-3,5,5- tr¡met¡lc¡cloex-2-en-1-ona semicarbazona, N-( 4-amino-2, 6- di hidroxi pirim¡din-5-il)-N-isopropiltiourea, ácido N-but¡l-N'-(2-furilmet¡l)urea, 3-({[2-carboxietil)amino] carbonil}amino)propanoico, 1-(2-cloroetil)-3- (c¡anomet¡l)urea, (2E)-1-(1H-indol-3-il)acetona tiosemicarbazona, (1E,4E)-1- fenilhex-4-en-1-ona semicarbazona, 1-(2,5-dioxoimidazolidin-4-il)-3- (hidroximetil)urea, 1-tert-butil-3-(2- cloroetil)urea, 1-(2-cloroetil)-3-(1-metil-1-feniletil)urea, 1-(2-cloroetil)-3-[1, 1-dimetil-2- (metilsulfonil)etil]urea, (1E, 1E')-2,2'-(2,4-dioxopirimidin-1,3(2H,4H)diil)diacetaldehído ditiosemicarbazona, y 1-(2,5-dioxoimidazolidin-4-il)-N
Patentes similares o relacionadas:
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
1,5-Dihidro-4H-pirazolo[3,4-d]pirimidin-4-onas y 1,5-dihidro-4H-pirazolo[4,3-c]piridin-4-onas como inhibidores de la PDE1, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de fórmula (I) **(Ver fórmula)** en donde Y es N o CH; R1 se selecciona del grupo que consiste en alquilo C2-C8 lineal o ramificado, cicloalquilo […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Compuestos de heteroaril carboxamida como inhibidores de RIPK2, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I): **(Ver fórmula)** o sus sales farmacéuticamente aceptables, en la que: X es N y Y es CH; o X es CH y Y es N; […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Derivados de 5-[2-(piridin-2-ilamino)-1,3-tiazol-5-il]-2,3-dihidro-1H-isoindol-1-ona y su uso como inhibidores dobles de fosfatidilinositol··3-cinasa delta y gamma, del 15 de Julio de 2020, de ASTRAZENECA AB: Compuesto de formula (I) **(Ver fórmula)** donde X es C(O) o SO2; Y es SO2NHR5 o SO2R6; R1 se selecciona de alquilo C1-4, […]
Antagonistas del receptor de dopamina D3 que tienen una unidad estructural biciclo, del 15 de Julio de 2020, de Indivior UK Limited: Un compuesto, o una sal farmacéuticamente aceptable del mismo, que tiene la fórmula: **(Ver fórmula)** en donde; A y B juntos tienen la fórmula: **(Ver […]