SISTEMA DE SUMINISTRO DE ANTÍGENOS.
Un compuesto para la vacunación de un animal que comprende (i) una fracción seleccionada de gp120 del VIH,
la proteína LAM de Mycobacterium tuberculosis o una glicoproteína del virus de Ébola, o una parte de las mismas que se une a DC-SIGN en una célula dendrítica y es mayor que 10 aminoácidos en longitud; y (ii) un antígeno
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2004/003386.
Solicitante: THE ROYAL VETERINARY COLLEGE.
Nacionalidad solicitante: Reino Unido.
Dirección: UNIVERSITY OF LONDON, ROYAL COLLEGE STREET LONDON NW1 0TU REINO UNIDO.
Inventor/es: WERLING,DIRK THE ROYAL VETERINARY COLLEGE.
Fecha de Publicación: .
Fecha Solicitud PCT: 5 de Agosto de 2004.
Fecha Concesión Europea: 23 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- A61K39/385 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Haptenos o antígenos, unidos a soportes.
Clasificación PCT:
- A61K39/385 A61K 39/00 […] › Haptenos o antígenos, unidos a soportes.
- C12N15/62 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/68 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación antigua:
- A61K39/385 A61K 39/00 […] › Haptenos o antígenos, unidos a soportes.
- C12N15/62 C12N 15/00 […] › Secuencias de ADN que codifican proteínas de fusión.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356344_T3.pdf
Fragmento de la descripción:
Sistema de suministro de antígenos.
La presente invención se refiere a un sistema de suministro de antígenos. En particular, se refiere a un sistema que puede ser usado para vacunar animales contra enfermedades y para distinguir entre animales vacunados y animales infectados naturalmente.
La comprensión y la manipulación selectiva del sistema inmune adaptativo y innato natural en animales es altamente favorable desde una vista de la protección de los animales, tanto en los animales de granja como en los animales de compañía, de la enfermedad y de una disminución en la dependencia de la intervención de antibióticos para el control de la enfermedad debido a los crecientes riesgos de resistencia a los antibióticos, un tema de creciente importancia en todas la especies.
Los antibióticos son frecuentemente utilizados en una base indiscriminada para la protección de especies de animales agrícolas y de compañía contra un amplio rango de patógenos. Esta cultura del uso inapropiado de antibióticos desarrollo a través de los malos resultados de los antígenos de patógenos con respecto a la inmunidad protectora.
Por lo tanto, la necesidad de desarrollar y mejorar nuestro entendimiento del papel de anfitrión de inmunidad adaptativa en la protección del agente patógeno esta siendo impulsado, por ejemplo, tanto por cuestiones de bienestar animal y la creciente exigencia de los consumidores de carne de alta calidad con reducción de residuos de antibióticos.
Ahora hay una investigación creciente en antígenos moleculares con el propósito de inducir a la protección en las especies animales para su uso en productos de la vacuna. Sin embargo, debido a que tales productos raramente toman en cuenta los requerimientos para la maduración del sistema inmune celular con respecto a la protección de animales de la enfermedad, esta ha tenido eficacia limitada en muchos casos.
Una de las limitaciones de la vacunación como un medio de control de la enfermedad es la dificultad de distinguir a animales infectados naturalmente y animales vacunados. Por ejemplo, esta era una cuestión importante con relación con el brote reciente de la enfermedad de la fiebre aftosa (FA) en el Reino Unido, don de la vacunación no fue utilizado en parte por la razón de que una vez que un rebaño de vacas nacionales es vacunado, ciertos países no permitirán importaciones de ganado de la manada. Los métodos actuales de vacunación también disminuyen el valor del mercado de la carne como el cuerpo tiene que ser tratado como si estuviera infectado, y colgado durante mas tiempo para matar cualquier virus que pueda estar presente. Para la FA se hace hincapié en mantener los rebaños limpios, pero es casi imposible mantener los rebaños limpios ya que la transmisión es un problema (ej., de ratas, tejones etc). Las vacunas marcadoras, las cuales contienen un inmunógeno extranjero a los animales vacunados, se han propuesto como una forma de distinguir animales vacunados y animales infectados naturalmente.
US 2002/0187131 (D2) revela métodos para el suministro de antígeno aumentado a células presentadoras de antígeno tales como células dendríticas y la modulación de la respuesta inmune de ella.
Propongo que atacando a las células dendríticas usando una fracción la cual se une selectivamente a las células dendríticas, en combinación con un antígeno tal como una referencia a una enfermedad del animal, y tal fracción el cual se une selectivamente como se dijo no ocurre naturalmente en esa especie de animales, proporciona no solo un nuevo concepto de suministro de antígeno (vacunación), pero también permite la discriminación entre animales vacunados y infectados naturalmente.
Un primer aspecto de la invención proporciona un compuesto para la vacunación de un animal que comprende (i) una fracción seleccionada del gp120 de VIH, de la proteína LAM de Mycobacterium tuberculosis o una glicoproteína del virus de Ébola, o una parte del mismo la cual se une a DC-SIGN en una célula dendrítica y es mayor que 10 aminoácidos en tamaño; y (ii) un antígeno.
La fracción une una célula dendrítica pero no se une sustancialmente a otros tipos de células presentadoras de antígeno. Si una fracción se une selectivamente con se ha dicho puede ser determinado mediante la medición de la unión de la fracción de células dendríticas comparado a la unión de otras células presentadoras de antígeno, por ejemplo usando una fracción vinculante de fluorógenos y la medición de la fluorescencia asociado con las células dendríticas y otras células presentadoras de antígeno. Alternativamente, un anticuerpo anti-fracción puede ser usado para determinar que células la fracción une con el fin de determinar su selectividad por las células dendríticas.
Las células dendríticas son células presentadoras de antígeno muy potentes y se ha demostrado ser eficaz como adyuvante fisiológicos para provocar la inmunidad profiláctica o terapéutica. Capturan microorganismos que entran en los tejidos periféricos de la mucosa y luego migran a órganos linfoides secundarios, donde se presentan estos microorganismos en forma antihigiénica a las células T en reposo y así iniciar la respuesta inmune adaptativa.
Es sabido que las células dendríticas tiene presentes en sus superficies proteínas, generalmente receptoras, las cuales están expresadas selectivamente y las cuales pueden ser usadas como un blanco por una célula dendrítica. Así, la fracción se une a un receptor el cual el mismo es expresado selectivamente en células dendríticas. Normalmente, un receptor que se expresa en forma selectiva en una célula dendrítica es una la cual esta presente en un nivel 10-veces, preferible 100-veces, o mas preferible 1000-veces mayor en células dendríticas que otras células presentadoras de antígeno.
La fracción se une al receptor de reconocimiento de patrón DC-SIGN en una célula dendrítica. Un receptor de reconocimiento de patrón es un receptor que une un patógeno asociado patrón molecular.
DC-SIGN es también conocido como la célula especifica de la molécula de adhesión intercelular 3 - cogiendo lectinas del tipo-C no integrinas, DC-SIGN, y es altamente expresado en la superficie de las células dendríticas. DC-SIGN es a veces también llamado CD209.
DC-SIGN es una proteína transmembrana de tipo II la cual forma un dominio citoplasmático N-terminal, un dominio de transmembrana, una región del cuello, una región de repeticiones en tándem y un dominio lectinas de unión manosa del tipo-C (calcio dependiente) en su termino-C. En el humano y el ratón DC-SIGN es expresado por células dendríticas presente en la dermis, lamina propia de los tejidos mucosos tales como el recto, útero y el cuello uterino, y en el área de células T de las amígdalas, ganglios linfáticos y el bazo. En los humanos DC-SIGN tiene 404 aminoácidos.
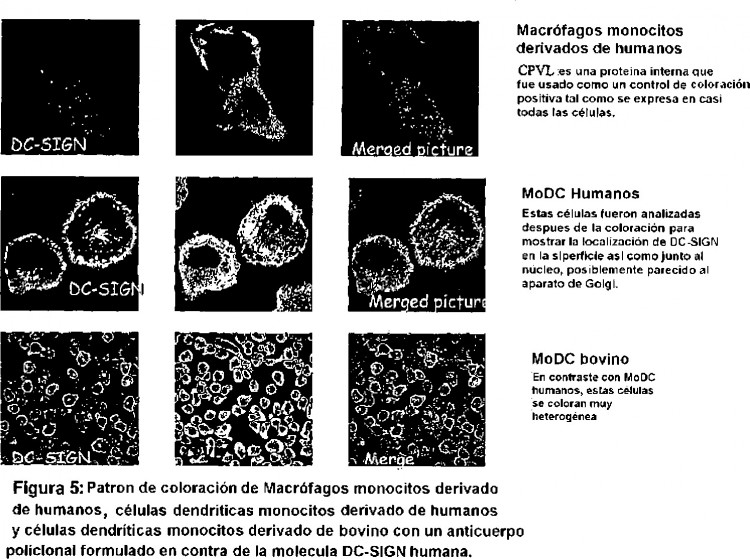
DC-SIGN ha sido encontrado en el humano, chimpancé, gorila, macaco, y donde el ADNc que codifica el polipéptido ha sido clonado. Las secuencias de aminoácidos y ADNc para DC-SIGN se encuentran en el siguiente Acceso del Banco de Genes Nos AF391086 (macaca mulatta), AY078913 (Pan troglodytes), NM_021155 (Humano) y NM_133238 (Mus). La figura 1 muestra una secuencia parcial de ADNc de una variante del bovino DC-SIGN. La secuencia de aminoácido deducido del variante de bovino 1 DC-SIGN, alineado con DC-SIGN del chimpancé, macaco y humano, es mostrada en la figura 3. La figura 6 muestra una secuencia parcial de ADNc de una segunda variante de bovino DC-SIGN. La secuencia de aminoácido deducido de variante de bovino 2 DC-SIGN, alineado con ratón, humano y variante de bovino 1 DC-SIGN, es mostrado en la figura 7. (ver ejemplo 7 para detalles de la clonación de ADNc).
Un análisis de dominio de la proteína SMART de humano, ratón y bovino (variante 2) DC-SIGN mostró que las proteínas comparten homología estructural, cada una contiene un receptor de lectinas de tipo-C. En DC-SIGN humano, el dominio de lectinas-C putativo es entre residuos 256 y 378; en ratón, el dominio lectinas-C putativo es entre residuos 108 y 229; y en bovino (variante 2) DC-SIGN, el dominio lectinas-C putativo es entre residuos 129-248.
Se cree que DC-SIGN es expresado selectivamente en la superficie de las células dendríticas y debido a su papel en el sistema inmune se cree que se puede conservar entre especies. Así, por ejemplo, el ADNc que codifica la secuencia de aminoácidos... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto para la vacunación de un animal que comprende (i) una fracción seleccionada de gp120 del VIH, la proteína LAM de Mycobacterium tuberculosis o una glicoproteína del virus de Ébola, o una parte de las mismas que se une a DC-SIGN en una célula dendrítica y es mayor que 10 aminoácidos en longitud; y (ii) un antígeno.
2. Un compuesto según la reivindicación 1 donde el antígeno es un polipéptido.
3. Un compuesto según cualquiera de las reivindicaciones precedentes donde el antígeno es un componente antigénico de un patógeno o un tumor, o, un antígeno prión.
4. Un compuesto según la Reivindicación 3 donde el antígeno comprende dos o mas de un componente antigénico de un patógeno o un tumor, o, un antígeno prión.
5. Un compuesto según la Reivindicación 3 o 4 donde el antígeno es una variante antigénica de un componente antigénico que tiene hasta 5% de sustituciones.
6. Un compuesto según las Reivindicaciones 3 - 5 donde el patógeno es cualquiera de una bacteria, virus, hongos, protozoos o helmintos.
7. Un compuesto según la Reivindicación 6 donde el antígeno es un componente antigénico de un patógeno asociado con la fiebre aftosa, la enfermedad vesicular porcina, peste de pequeños rumiantes, dermatosis nodular contagiosa, lengua azul, peste equina africana, peste porcina clásica, enfermedad de Newcastle, estomatitis vesicular, peste bovina, perineumonía contagiosa bovina, fiebre del valle Rift, viruela ovina y caprina, la peste porcina africana, y la influenza aviar altamente patógena o una variante de dicho componente que tiene hasta 5% de sustituciones.
8. Un compuesto según cualquiera de las reivindicaciones precedentes donde la fracción y el antígeno están unidos covalentemente.
9. Un compuesto según cualquiera de las reivindicaciones precedentes donde la fracción y el antígeno, cada uno comprende un polipéptido y ambos están presentes en la misma cadena de polipéptido.
10. Un molécula de ácido nucleico que codifica un compuesto según la Reivindicación 9.
11. Un vector de expresión que comprende una molécula de ácido nucleico según la Reivindicación 10.
12. Una célula huésped que comprende una molécula de ácido nucleico según la Reivindicación 10 o un vector de expresión según la Reivindicación 11.
13. Una vacuna que comprende un compuesto según cualquiera de las Reivindicaciones de 1 a 9 o una molécula de ácido nucleico según la Reivindicación 10.
14. Una vacuna según la Reivindicación 13 que comprende además un adyuvante.
15. Un compuesto según cualquiera de las Reivindicaciones 1 a 9 o una molécula de ácido nucleico según la Reivindicación 10 para su uso en la medicina.
16. Una composición farmacéutica que comprende un compuesto según cualquiera de las Reivindicaciones 1 a 9 o una molécula de ácido nucleico según la Reivindicación 10 y un portador farmacéuticamente aceptable.
17. Uso de un compuesto según cualquiera de las Reivindicaciones 1 a 9 o un ácido nucleico según la reivindicación 10 en la fabricación de un medicamento para combatir una enfermedad en un animal.
18. Uso de un compuesto según cualquiera de la Reivindicaciones 1 a 9 o un ácido nucleico según la Reivindicación 10 en la fabricación de una vacuna para la inmunización de un animal.
19. Uso según la Reivindicación 17 o 18 donde la enfermedad es una causada por un patógeno.
20. Uso según la Reivindicación 19 donde el patógeno es cualquiera de una bacteria, virus, hongos, protozoos o helminto.
21. Uso según la Reivindicación 20 donde el patógeno es uno asociado con la fiebre aftosa, la enfermedad vesicular porcina, peste de pequeños rumiantes, dermatosis nodular contagiosa, lengua azul, peste equina africana, peste porcina clásica, enfermedad de Newcastle, estomatitis vesicular, peste bovina, perineumonía contagiosa bovina, fiebre del valle Rift, viruela ovina y caprina, la peste porcina africana, y la influenza aviar altamente patógena.
22. Uso según la Reivindicación 17 o 18 donde el animal es un mamífero.
23. Uso según la Reivindicación 17 o 18 donde el animal es una animal de compañía o un animal de granja.
24. Uso según la Reivindicación 22 o 23 donde el animal es una vaca, oveja, caballo, cerdo, cabra, perro, gato o conejo.
25. Un método de fabricación de un compuesto según la Reivindicación 1 comprendiendo enlazar dicha fracción y dicho antígeno.
26. Un método de fabricación de un compuesto según la Reivindicación 9 el cual comprende un polipéptido, dicho método comprendiendo (i) cultivar de una célula huésped según la Reivindicación 12 que expresa dicho polipéptido y (ii) aislar dicho polipéptido.
27. Un método de fabricación de un ácido nucleico según la Reivindicación 10 comprendiendo el enlace de una molécula de ácido nucleico que codifica la fracción y una molécula de ácido nucleico que codifica un antígeno.
28. Un método para determinar si a un animal se ha administrado un compuesto según la Reivindicación 1, el método comprendiendo determinar en una muestra conteniendo anticuerpos tomada del animal, si el animal ha tenido una respuesta inmune a la fracción en el compuesto según la Reivindicación 1.
29. Un método según la Reivindicación 28 que comprende el paso adicional de determinar si el animal ha tenido una respuesta inmune al antígeno presente en dicho compuesto.
30. Un kit de partes que comprende (i) un compuesto según cualquiera de la Reivindicaciones 1 a 9 o una molécula de ácido nucleico según la Reivindicación 10 y (ii) medios para la detección de una respuesta inmune a la fracción presente en dicho compuesto y/o (iii) medios para la detección de una respuesta inmune al antígeno presente en dicho compuesto.
31. Un kit de partes según la Reivindicación 30 en donde si está presente la parte (ii) comprende todos, o una porción mayor que 10 residuos de aminoácidos de longitud, de dicha fracción que se une a un anticuerpo aparecido contra dicha fracción y la parte (iii) comprende todos, o una porción de al menos 5 aminoácidos de longitud, de dicho antígeno que se une a un anticuerpo aparecido contra dicho antígeno.
32. Un kit de partes que comprende (i) medios para la detección de una respuesta inmune a un antígeno de enfermedad animal y (ii) medios para la detección una respuesta inmune a una fracción seleccionada de la gp120 del VIH, la proteína LAM de Mycobacterium tuberculosis o una glicoproteína del virus de Ébola, o una parte de la mismas que se une a DC-SIGN en una célula dendrítica y es mayor que 10 aminoácidos en longitud.
33. Un kit de partes según cualquiera de las reivindicaciones 30 a 32 donde el medio para la detección de una respuesta inmune es un ELISA.
Patentes similares o relacionadas:
DERIVADOS DE OLIGOSACÁRIDOS SINTÉTICOS COMO VACUNA CONTRA BORDETELLA PERTUSSIS, del 2 de Julio de 2020, de INSTITUTO FINLAY DE VACUNAS: La presente invención proporciona fragmentos de oligosacáridos sintéticos provenientes del pentasacárido terminal del lipooligosacárido de Bordetella pertussis, un método […]
Proteínas recombinantes y sus usos terapéuticos, del 27 de Mayo de 2020, de Bioven 3 Limited: Una proteína recombinante, que comprende: una secuencia polipeptídica inmunogénica que incluye la subunidad B de la toxina del cólera (CT-B) o la subunidad […]
Bacterias mutantes para la producción de módulos generalizados para antígenos de membrana, del 13 de Mayo de 2020, de GLAXOSMITHKLINE BIOLOGICALS SA: Un procedimiento para preparar vesículas a partir de una bacteria gramnegativa en el que al menos una proteína que contiene un dominio catalítico LytM se inactiva […]
Composición de medio para preparar toxina botulínica, del 6 de Mayo de 2020, de Daewoong Co., Ltd: Una composición de medio libre de EET para su uso en el cultivo de Clostridium botulinum, la composición de medio comprende: peptonas de origen […]
Proteínas de fusión y vacunas de combinación, del 26 de Febrero de 2020, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende una proteína de fusión de fórmula I: (X)m-(R1)n-A-(Y)o-B-(Z)p (fórmula I) en la que X es un péptido señal o MHHHHHH (SEQ […]
Glucoconjugado de oligosacárido procedente de LOS con la toxina tosferínica de Bordetella pertussis y su aplicación en la profilaxis y el tratamiento de infecciones causadas por Bordetella pertussis, del 4 de Noviembre de 2019, de Siec Badawcza Lukasiewicz - PORT Polski Osrodek Rozwoju Technologii: Un método para preparar un glucoconjugado que comprende un oligosacárido (OS) procedente de LOS o su fragmento y la toxina tosferínica (PT) de B. pertussis en donde el método […]
Composiciones y métodos para mejorar la inmunogenicidad de los conjugados de polisacárido-proteína, del 23 de Octubre de 2019, de Kanvax Biopharmaceuticals Ltd: Un conjugado de polisacárido-proteína que comprende una proteína transportadora quimérica y un antígeno polisacárido, en donde la proteína […]
Composición de vacuna que comprende polisacáridos capsulares naturales conjugados de N. Meningitidis, del 24 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS SA: Una composición inmunogénica que comprende polisacáridos capsulares de N. meningitidis de los serogrupos A, C, W135 e Y, en donde cada polisacárido […]