ESTABILIZACION DE ANTICUERPOS CAMELIDOS DE CADENA LARGA CON SALES DE POTASIO.
Gránulo anticuerpo que consiste esencialmente en uno o más anticuerpos de cadena pesada como los encontrados en los Camélidos,
o en fragmentos derivados de los mismos, granulados con una sal de potasio, en el que el gránulo consiste en más del 80%, con preferencia más del 90%, de la sal de potasio
Tipo: Resumen de patente/invención. Número de Solicitud: W0114478EP.
Solicitante: UNILEVER N.V.
UNILEVER PLC
HINDUSTAN LEVER LTD..
Nacionalidad solicitante: Países Bajos.
Dirección: WEENA 455,NL-3013 AL ROTTERDAM.
Inventor/es: HEMMINGTON, SANDRA, PARRY, NEIL JAMES, CHAPPLE,ANDREW,P, HOWELL,STEVEN.
Fecha de Publicación: .
Fecha Concesión Europea: 2 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C11D3/00B4
- C11D3/384A
Clasificación PCT:
- C07K16/46 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C11D3/384 C […] › C11 ACEITES, GRASAS, MATERIAS GRASAS O CERAS ANIMALES O VEGETALES; SUS ACIDOS GRASOS; DETERGENTES; VELAS. › C11D COMPOSICIONES DETERGENTES; UTILIZACION DE UNA SOLA SUSTANCIA COMO DETERGENTE; JABON O SU FABRICACION; JABONES DE RESINA; RECUPERACION DE LA GLICERINA. › C11D 3/00 Otros compuestos que entran en las composiciones detergentes cubiertas por C11D 1/00. › Productos animales.
Clasificación antigua:
Fragmento de la descripción:
Estabilización de anticuerpos camélidos de cadena larga con sales de potasio.
Campo técnico
La presente invención se refiere en general a la estabilización de anticuerpos, o de fragmentos derivados de los mismos, en composiciones detergentes, en particular en composiciones detergentes blanqueadoras.
Antecedentes y técnica anterior
Los anticuerpos son polipéptidos que son capaces de enlazar específicamente con compuestos contra los que fueron cultivados. Los anticuerpos se utilizan para una diversidad de propósitos, tal como inmuno ensayos. Más recientemente, se ha propuesto su replicación en aplicaciones detergentes y de limpieza. El documento WO-A-98/56885 (Unilever) revela una enzima blanqueadora que es susceptible de generar una química blanqueadora, y que tiene una alta afinidad enlazadora con las manchas presentes en los tejidos, así como una composición blanqueadora enzimática que comprende la citada enzima blanqueadora, y un procedimiento para blanquear manchas en los tejidos. La afinidad enlazadora puede estar formada por una parte de la cadena de polipéptido de la enzima blanqueadora, o la enzima puede comprender una parte de enzima que sea capaz de generar una química de blanqueo que se acopla a un reactivo que tiene una alta afinidad enlazadora respecto a las manchas presentes en los tejidos. En este último caso, el reactivo puede ser bi-específico, comprendiendo una especificidad respecto a la mancha y una respecto a la enzima. Ejemplos de tales reactivos bi-específicos mencionados en la descripción son los anticuerpos, especialmente los derivados de lo Camélidos que tienen solamente una región variable de la cadena pesada de polipéptido (VHH), los péptidos, peptidomímicos, y otras moléculas orgánicas. La enzima es normalmente una oxidasa, tal como la oxidasa de glucosa, oxidasa de galactosa y alcohol oxidasa, que sea capaz de formar peróxido de hidrógeno u otro agente blanqueador. De ese modo, si el reactivo multiespecífico es un anticuerpo, la enzima forma un conjugado enzima/anticuerpo que constituye un ingrediente de una composición detergente. Durante el lavado, dicho conjugado enzima/anticuerpo de la composición detergente es objetivado por otro sitio funcional del anticuerpo, mientras que la enzima conjugada cataliza la formación de un agente blanqueador en las proximidades de la mancha, y la mancha se verá sometida al blanqueador.
Se ha prestado poca atención con respecto a la manera en la que tales anticuerpos son añadidos a la composición detergente con el fin de conseguir el efecto blanqueador deseado del complejo enzima-anticuerpo. Se ha encontrado que la estabilidad de almacenamiento de los anticuerpos en cuanto a ese problema de las composiciones de limpieza, no es siempre satisfactoria. Existe una amplia técnica anterior con respecto a la granulación de enzimas para su uso en detergentes, pero esta tecnología no puede ser transferida directamente a los anticuerpos.
El objeto de la presente invención consiste en proporcionar un procedimiento mediante el que los anticuerpos puedan ser incorporados en composiciones detergentes (blanqueadoras) de una manera estable.
Ahora se ha encontrado sorprendentemente que es posible incorporar anticuerpos en composiciones detergentes de una manera estable si los anticuerpos están granulados con sales de potasio. Esto es la inversa de la granulación de enzimas, por lo que han de tomarse medidas complicadas en la tecnología de granulación con el fin de proporcionar la estabilidad y la duración requeridas para la enzima.
Además, se ha encontrado sorprendentemente que la actividad del anticuerpo fue mejorada cuando se almacenó en forma granulada, en comparación con los métodos de almacenaje de la proteína común. Esto imparte, por lo tanto, una duración sustancialmente mejorada del anticuerpo y de su comportamiento asociado en forma de polvo o en forma de producto.
Definición de la invención
De acuerdo con un primer aspecto de la invención, se proporciona un gránulo de anticuerpo que consiste esencialmente en uno o más anticuerpos de cadena pesada encontrados en los Camélidos, o en fragmentos derivados de los mismos, granulados con una sal de potasio, en el que el gránulo consiste en más de un 80%, con preferencia más de un 90%, de sal de potasio.
De acuerdo con un segundo aspecto, se proporciona una composición enzimática blanqueadora de manchas o anti transferencia de tinte, que comprende el gránulo de anticuerpo de la invención.
De acuerdo con un tercer aspecto, se proporciona un procedimiento para preparar los citados gránulos de anticuerpo de la invención.
Descripción de la invención
En su primer aspecto, la invención se refiere a un gránulo de anticuerpo según se define en la reivindicación 1. Según se ha expuesto en lo que antecede, los anticuerpos de cadena pesada son polipéptidos que son susceptibles de enlazar específicamente con compuestos contra los que fueron cultivados.
El grado de enlace de un compuesto A con otra molécula B, puede ser expresado en general por la constante Kd de equilibrio químico que resulta de la siguiente reacción de enlace:
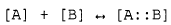
La constante Kd de equilibrio químico viene dada por:
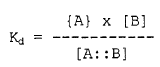
Se puede determinar si el ligante con la sustancia es específico o no a partir de la diferencia entre [valor Kd] del ligante del compuesto para esa sustancia, respecto al ligante para el material al que se aplica la sustancia, o respecto a otras sustancias que no se desea oxidizar. Para sustancias que se producen en las manchas, se puede prever que el último material sea el tejido en el que la mancha está presente, o las moléculas de tinte sobre prendas de vestir coloreadas. La diferencia entre las dos contantes de enlace debe ser mínimamente 100, y con preferencia más de 1000. Típicamente, el compuesto deberá enlazar con la sustancia coloreada con un valor Kd de 1*10-4 a 1*10-6, con un enlace de fondo con el tejido con una Kd de 1*10-2 a 1*10-3. Afinidades de enlace más altas (Kd menor de 1*10-3) y/o una diferencia más grande entre el enlace de la sustancia coloreada y el fondo, podrían incrementar la selectividad del proceso de oxidación. También, la eficacia de peso del compuesto en la composición detergente total podría ser incrementada, y se necesitarían cantidades más pequeñas del compuesto.
Los anticuerpos pueden ser extraídos a partir de varias fuentes. A partir de los ratones, se pueden obtener anticuerpos monoclonales que posean afinidades de enlace muy altas. A partir de tales anticuerpos, se pueden preparar los fragmentos Fab, Fv o scFv, que conserven sus propiedades de enlace. Tales anticuerpos o fragmentos pueden ser producidos a través de tecnología de ADN recombinante, por fermentación microbiana. Huéspedes bien conocidos de producción de anticuerpos y de sus fragmentos son la levadura, los hongos o las bacterias.
Una clase de anticuerpos de particular interés está formada por los anticuerpos de cadena pesada según se encuentran en Camélidos tales como el camello o la llama. Los dominios de enlace de estos anticuerpos consisten en un fragmento de polipéptido simple, en particular la región variable del polipéptido de cadena pesada (HC-V). Por el contrario, en los anticuerpos clásicos (murina, humano, etc.), el dominio de enlace consiste en dos cadenas de polipéptido (las regiones variables de de la cadena pesada (Vh) y de la cadena ligera (V1). Procedimientos para obtener inmunoglobulinas de cadena pesada a partir de los Camélidos, o fragmentos (funcionalizados) de los mismos, han sido descritos en el documento WO-A-94/04678 (Casterman y Hamers) y en el documento WO-A-94/25591 (Unilever y Free University of Brussels).
Alternativamente, los dominios de enlace pueden ser obtenidos a partir de los fragmentos Vh de anticuerpos clásicos por medio de un procedimiento conocido como "camelización". Con ello, el fragmento clásico Vh se transforma por sustitución de un número de aminoácidos, en un fragmento de tipo HC-V, con lo que se mantienen sus propiedades de enlace. Este procedimiento ha sido descrito por Riechmann y cols., en un número de publicaciones (J. Mol. Biol. (1996) 259, 957-969; Protein....
Reivindicaciones:
1. Gránulo anticuerpo que consiste esencialmente en uno o más anticuerpos de cadena pesada como los encontrados en los Camélidos, o en fragmentos derivados de los mismos, granulados con una sal de potasio, en el que el gránulo consiste en más del 80%, con preferencia más del 90%, de la sal de potasio.
2. Gránulo anticuerpo de acuerdo con la reivindicación 1, que comprende además un ligante polimérico.
3. Gránulo anticuerpo de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que el anticuerpo tiene una constante Kd de equilibrio químico para su antígeno de menos de 1*10-4, con preferencia menos de 1*10-6.
4. Gránulo anticuerpo de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que la constante Kd de equilibrio químico para el antígeno es menor de 1*10-7.
5. Una composición detergente que comprende el gránulo anticuerpo de una cualquiera de las reivindicaciones anteriores.
6. Una composición enzimática blanqueadora de manchas, que comprende el gránulo anticuerpo de las reivindicaciones 1-5.
7. Una composición enzimática anti transferencia de tinte, que comprende el gránulo anticuerpo de las reivindicaciones 1-5.
8. Procedimiento de preparación de un gránulo anticuerpo de acuerdo con las reivindicaciones 1-5, en el que el anticuerpo está granulado con una sal de potasio.
9. Procedimiento de acuerdo con la reivindicación 8, en el que la temperatura es de 30ºC o mayor, con preferencia de 30ºC a 80ºC.
10. Procedimiento de acuerdo con la reivindicación 8, en el que el pH se mantiene en un valor desde 6,0 hasta 10,0, con preferencia desde 7,0 hasta 9,0.
Patentes similares o relacionadas:
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Formulación anti-IFNAR1 estable, del 24 de Junio de 2020, de ASTRAZENECA AB: Una formulacion de anticuerpo que comprende: a. De 100 mg/ml a 200 mg/ml de anifrolumab; b. Lisina HCl 40 mM a 60 mM; c. Trehalosa […]
Proteínas y péptidos modificados, del 24 de Junio de 2020, de GLAXO GROUP LIMITED: Un dominio variable de inmunoglobulina único, que se une a TNFR1 y que se selecciona de cualquiera de las siguientes secuencias de aminoácidos: (a) DOM1h-131-206 caracterizada […]
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]
Dominios variables de inmunoglobulina, del 10 de Junio de 2020, de Ablynx NV: Dominio variable individual de inmunoglobulina de cadena pesada (ISVD), en que el residuo aminoacídico en la posición 89 es L y el residuo […]