ACIDO HIALURONICO ACRILATADO.
Proceso para la preparación de un producto de ácido hialurónico acrilatado comprendiendo las fases siguientes que consisten en:
a) preparar un líquido acuoso comprendiendo ácido hialurónico donde el pH se mantiene en un pH adecuado;
b) preparar un líquido orgánico comprendiendo cloruro de acriloilo y un solvente orgánico; y
c) mezclar el líquido orgánico de (b) y el líquido acuoso de (a), donde el pH se mantiene en un pH adecuado
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/063671.
Solicitante: NOVOZYMES BIOPHARMA DK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: KROGSHOEJVEJ 36,2880 BAGSVAERD.
Inventor/es: GROSS, RICHARD A., KUMAR,VINEET.
Fecha de Publicación: .
Fecha Concesión Europea: 30 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- C08B37/00P2F
- C08J3/24H
Clasificación PCT:
- C08B37/08 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › C08B 37/00 Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21). › Quitina; Sulfato de condroitín; Acido hialurónico; Sus derivados.
Fragmento de la descripción:
Ácido hialurónico acrilatado.
Campo de la invención
La presente invención se refiere a un proceso para producir un ácido hialurónico acrilatado (AH).
Antecedentes de la invención
El ácido hialurónico (AH) es un polímero carbohidrato natural y lineal que pertenece a la clase de los glicosaminoglicanos no sulfatados. Se compone de beta-1,3-N-acetil glucosamina y unidades de disacárido repetición de beta-1,4-ácido glucurónico con un peso molecular (PM) hasta 6 MDa. El AH está presente en el cartílago hialino, el líquido de articulación sinovial, y los tejidos de la piel, tanto dermis como epidermis. El AH puede ser extraído a partir de tejidos naturales incluyendo el tejido conjuntivo de vertebrados, del cordón umbilical humano y de las crestas de gallos. Sin embargo, actualmente se prefiere preparar este último por medio de métodos microbiológicos para minimizar el riesgo potencial de transferencia de agentes infecciosos, y para incrementar la uniformidad, calidad y disponibilidad del producto, (patente U.S. nº.6,951,743: WO 03/0175902).
Se han identificado numerosas funciones del AH en el cuerpo. Tiene un papel importante en organismos biológicos, como soporte mecánico para células de varios tejidos, tales como piel, tendones, músculos y cartílago. El AH se implica en procesos biológicos claves, tales como la humectación de tejidos, y la lubricación. También se supone que cumple un papel en muchas funciones fisiológicas, como la adhesión, el desarrollo, la motilidad de las células, el cáncer, la angiogénesis, y la curación de heridas. Debido a las propiedades físicas y biológicas únicas del AH (incluyendo viscoelasticidad, biocompatibilidad, biodegradabilidad), el AH se emplea en una amplia gama de aplicaciones actuales y en desarrollo en cosmética, oftalmología, reumatología, administración de medicamentos e inserción de genes, curación de heridas y la ingeniería de tejidos. El uso de AH en alguna de estas aplicaciones es limitado por el hecho de que el AH es soluble en agua a temperatura ambiente, es decir que, a aproximadamente 20ºC, se degrada rápidamente por hialuronidasa en el cuerpo, y es difícil de procesar en biomateriales. Por lo que se ha introducido la reticulación de AH para mejorar las propiedades físicas y mecánicas del AH y su tiempo de residencia in vivo.
El AH acrilatado se puede utilizar para realizar una reticulación mediada por enzima y producir materiales en forma de hidrogeles. El AH reticulado se puede utilizar en aplicaciones cosméticas, biomédicas y farmacéuticas. Por medio de la reticulación de AH es posible diseñar un compuesto con propiedades específicas para aplicaciones específicas. El AH acrilatado provee grupos reactivos funcionalizados que pueden ser modificados también por una adición de tipo Michael para introducir péptidos bioactivos para diferentes aplicaciones.
Los grupos de acrilato en AH han sido introducidos por síntesis de conjugados de metacrilato de glicidilo-AH (GMAH). Los derivados de GMAH son útiles para preparar hidrogeles biomiméticos de AH para estimular la reparación de tejidos y la curación de heridas. También se ha descubierto que las cantidades aumentadas de grupos de metacrilato conjugados corresponden a densidades reticuladas aumentadas e índices de degradación reducidos, y tienen un efecto insignificante en la citocompatabilidad y proliferación de células aórticas endoteliales humanas. Los derivados de GMAH se han preparado por tratamiento de un 1% p/v de solución de AH derivado de una fermentación (~2 X 106 de peso molecular) en agua destilada con un exceso molar multiplicado por 6, 10 y 20 de metacrilato de glicidilo en presencia de un exceso de trimetilamina y bromuro de tetrabutilamonio durante toda la noche a temperatura ambiente, seguido de una incubación de 1 hora a 60ºC. Por ejemplo el GMAH con un exceso molar multiplicado por seis de GM se preparó mediante la disolución de 1.0 g AH en 100 ml de agua destilada. A la solución se añadió 2.2 ml de trietilamina de, 2.2 ml de metacrilato de glicidilo y 2.2 g de bromuro de tetrabutilamonio y se agitó durante toda la noche, seguido de una incubación a 60ºC durante una hora. Por este proceso se obtuvo un 5% de metacrilación. Utilizando un exceso molar multiplicado por 10 y 20 se obtuvo una acrilación del 7 y 11% (Leach y Schmidt, 2005, Biomaterials 26, 125-135; Yonese et al., 2002, Chem. Pharm. Bull. 50, 1341-1348; Schmidt et al., 2003, Biotechnology and Bioengineering 82(5), 578-589).
Los conjugados de GMAH se han preparado también por disolución de AH en tampón de carbonato a un pH 11.0. Se añadió metacrilato de glicidilo a la solución anterior y la mezcla fue agitada a temperatura ambiente durante 7 días. El pH de la solución resultante se ajustó a 7.0 con HCl. Se filtró y se liofilizó (Yonese, 2001. Journal of Controlled Release 73, 173-181). El conjugado de GMAH se reticuló también con acrilado de hidroxietilo para preparar un hidrogel.
Se han introducido también grupos acrilatados en AH por síntesis de conjugados de N-3-aminopropilo metacrilamida-AH por modificación de los grupos de carboxilo presentes en AH. Tanto el AH nativo y el degradado enzimáticamente fueron usados posteriormente para una modificación química. Ambos AH fueron modificados utilizando metacrilamida N-(3-aminopropilo) como agente acrilante. El grupo aminopropilo reaccionó con un grupo carboxilo de AH en presencia de N-(3-dimetilaminopropilo)-N'-etilcarbodiimida (EDCl) como agente de acoplamiento produciendo la formación de un enlace amido con grupos acrilo pendientes en el otro extremo. En una reacción típica el AH fue disuelto en agua destilada. A la solución se añadió EDCl seguido de metacrilamida N-3-aminopropilo. La mezcla reactiva se incubó a pH 6.5 durante dos horas seguidas de la adición posterior de EDCl y metacrilamida N-3-aminopropilo y fue incubada además durante 2 horas a temperatura ambiente. La solución se filtró, dializó contra NaCl seguido de agua y liofilizado finalmente para formar AH metacrilatado. El grado de acrilación logrado fue de aproximadamente el 10% (Tirelli et al., 2003, Biomaterials, 24, 893-900; Kim and Park 2002, Journal of Controlled Release, 80, 69-77).
El ácido hialurónico metacrilatado (HAMA) ha sido sintetizado por adición de anhídrido metacrílico (~multiplica-do por 20) a una solución de 1% de AH en agua desionizada ajustada a un pH de 8 con NaOH y reaccionada sobre hielo durante 24 horas. El polisacárido modificado fue precipitado y lavado con etanol para eliminar el anhídrido metacrílico. En el proceso se puede conseguir una metacrilación de hasta un 17%. El % reducido de metacrilación (17%) logrado se debía a la reactividad reducida del anhídrido metacrílico con hidroxilos de AH (Smeds and Grinstaff 2001, Journal of Biomedical Materials Research, 54, 115-121; Langer et al., 2005, Biomacmmotecules, 6, 386-391).
Los métodos conocidos para la acrilación de AH son largos y complicados, y se necesita en la técnica un proceso más simple para la acrilación de AH. Es un objeto de la presente invención de proporcionar un proceso simple para la acrilación de ácido hialurónico.
Resumen de la invención
La presente invención se refiere a métodos para producir un ácido hialurónico acrilatado, dicho método incluyendo las etapas que consisten en:
Los procesos de la presente invención son muy rápidos debido a una reactividad muy alta del agente reactivo acrilante utilizado, reduciendo así los tiempos de reacción convencionales. El % de acrilación obtenido es mucho más elevado usando los procesos de la presente invención. Mediante el uso del proceso simple y rápido una acrilación superior al 90% puede ser obtenida en un tiempo de reacción mucho más corto (1-2 horas) en comparación con un 17% divulgado hasta la fecha mediante el uso de procesos complejos. Este es el % máximo de acrilación obtenido sin usar ningún agente de acoplamiento. Además los productos adicionales obtenidos en los procesos de la presente invención son muy inferiores y pueden se eliminados fácilmente en comparación con los protocolos provistos.
Descripción detallada de...
Reivindicaciones:
1. Proceso para la preparación de un producto de ácido hialurónico acrilatado comprendiendo las fases siguientes que consisten en:
2. Proceso según la reivindicación 1, donde la mezcla en la fase c) es realizada por agitación.
3. Proceso según la reivindicación 1, donde la fase a) es mantenida a un pH entre 7 y 11.
4. Proceso según la reivindicación 1, donde el líquido acuoso de la fase a) comprende un tampón de fosfato.
5. Proceso según la reivindicación 4, donde el tampón de fosfato está presente en una cantidad entre 0.1 molar a 1 molar.
6. Proceso según la reivindicación 1, donde la fase c) es mantenida a un pH entre 7 y 11.
7. Proceso según la reivindicación 1, donde la fase c) es mantenida a un pH entre 7 y 11 mediante el uso de un tampón y/o la adición gota a gota de NaOH diluido.
8. Proceso según la reivindicación 1, donde la temperatura es mantenida entre 0ºC y 15ºC durante la fase a).
9. Proceso según la reivindicación 1, donde la temperatura es mantenida entre 0ºC y 5ºC durante la fase c).
10. Proceso según la reivindicación 1, donde el pH del líquido acuoso de la fase a) es ajustado por adición de NaOH gota a gota.
11. Proceso según la reivindicación 1, donde el pH del líquido acuoso de la fase a) es ajustado por un tampón y/o adición de NaOH gota a gota.
12. Proceso según la reivindicación 1, donde la adición de cloruro de acriloilo en la fase c) se consigue mediante el uso de una bomba de jeringa.
13. Proceso según la reivindicación 1, comprendiendo también una fase de recuperación.
14. Proceso según la reivindicación 13, donde la fase de recuperación comprende una fase de precipitación.
15. Proceso según la reivindicación 13, donde la fase de recuperación comprende también una fase de filtración de la mezcla reactiva y una precipitación del filtrado.
Patentes similares o relacionadas:
UTILIZACIÓN DE PRÓTESIS TRIDIMENSIONALES QUE CONTIENEN DERIVADOS DEL ÁCIDO HIALURÓNICO, del 6 de Mayo de 2011, de FIDIA ADVANCED BIOPOLYMERS S.R.L.: Utilización de, como mínimo, una matriz tridimensional que tiene estructura fibrosa y que consiste, como mínimo, de un derivado de ácido hialurónico, […]
 COMPOSICIÓN DE POLISACÁRIDOS RETICULADOS, del 13 de Enero de 2011, de ULTRACEUTICALS R&D PTY LIMITED: Un procedimiento para producir un gel de polisacárido reticulado que comprende: a) poner en contacto un polisacárido mezclado en un medio alcalino […]
COMPOSICIÓN DE POLISACÁRIDOS RETICULADOS, del 13 de Enero de 2011, de ULTRACEUTICALS R&D PTY LIMITED: Un procedimiento para producir un gel de polisacárido reticulado que comprende: a) poner en contacto un polisacárido mezclado en un medio alcalino […]
 POLISACARIDOS DERIVATIZADOS CON ACIDO CITRICO, del 1 de Diciembre de 2010, de SIGEA S.R.L.: Derivados no reticulados de oligo/polisacáridos que tienen la fórmula en la que: X es OH, O-M, NH-R1, O-R1; M: es un metal alcalino o alcalinotérreo, […]
POLISACARIDOS DERIVATIZADOS CON ACIDO CITRICO, del 1 de Diciembre de 2010, de SIGEA S.R.L.: Derivados no reticulados de oligo/polisacáridos que tienen la fórmula en la que: X es OH, O-M, NH-R1, O-R1; M: es un metal alcalino o alcalinotérreo, […]
PROCESO PARA LA PREPARACION DE ESTERES DE DIACEREINA CON ACIDO HIALURONICO Y PREPARACIONES FARMACEUTICAS QUE LOS CONTIENEN, del 18 de Noviembre de 2009, de CBB NET S.A: Proceso para la preparación de ésteres estables de diacereína con ácido hialurónico de una actividad antiinflamatoria prolongada y adecuados […]
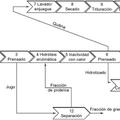 Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
Agente de reticulación de diamina, cuerpo reticulado de polisacárido ácido y material médico, del 15 de Julio de 2020, de SEIKAGAKU CORPORATION: Polisacárido ácido reticulado obtenido formando reticulaciones mediante un enlace amida entre grupos amino primarios en un agente de reticulación de diamina y grupos […]
Procedimiento para la preparación y purificación de la sal de sodio de ácido hialurónico, del 1 de Julio de 2020, de FIDIA FARMACEUTICI S.P.A.: Un procedimiento para la preparación y purificación de la sal de sodio de ácido hialurónico (HA) a partir del caldo de fermentación de Streptococcus o Bacillus o a […]
Procedimiento de reticulación de glicosaminoglicanos, del 10 de Junio de 2020, de GALDERMA RESEARCH & DEVELOPMENT: Glicosaminoglicanos reticulados, donde dichos glicosaminoglicanos están reticulados mediante un anión de éster de alcoxiboronato formado entre una porción de diol […]