Recubrimientos que contienen múltiples fármacos.
Un método de preparación de un stent coronario de elución de multifármacos que comprende:
a. proporcionar una estructura de stent;
b. depositar sobre dicha estructura de stent una primera capa que comprende un primer agente farmacéutico;
c. depositar una segunda capa que comprende un segundo agente farmacéutico;
donde dicho primero y segundo agentes farmacéuticos se seleccionan a partir de dos clases diferentes de agentes farmacéuticos,
en donde los agentes farmacéuticos comprenden un fármaco macrólido inmunosupresor (limus), y en donde dicho fármaco macrólido inmunosupresor es al menos 50% cristalino.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/010227.
Solicitante: MICELL TECHNOLOGIES, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 7516 PRECISION DRIVE RALEIGH, NC 27617 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DEYOUNG,JAMES, TAYLOR,DOUG, MCCLAIN,JIM, SMOKE,CLINT, COLE,MIKE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K9/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
PDF original: ES-2540059_T3.pdf

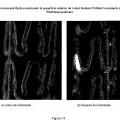



Fragmento de la descripción:
Recubrimientos que contienen múltiples fármacos Antecedentes de la invención
La presente invención como se define en las reivindicaciones se refiere a métodos para preparar un stent coronario capaz de eluir varios fármaco así como a los stents preparados con dicho método.
A menudo es beneficioso proporcionar recubrimientos sobre sustratos, de manera que las superficies de dichos sustratos tengan propiedades o efectos deseados.
Por ejemplo, es útil recubrir implantes biomédicos a fin de proporcionar la administración localizada de agentes farmacéuticos o biológicos destinados a lugares específicos dentro del cuerpo, para beneficio terapéutico o profiláctico. Una de las áreas de especial interés es la de los stents que eluyen fármacos (DES) que han sido recientemente revisados porOng y Serruys en Nat. Clin. Pract. Cardiovasc. Med., (Diciembre 25), volumen 2, n° 12. 647. Por lo general este tipo de agentes farmacéuticos o biológicos se depositan junto con un polímero. Dicha administración localizada de estos agentes evita los problemas de la administración sistémica, que puede estar acompañada de efectos no deseados en otras partes del cuerpo, o porque la administración a la parte del cuerpo afectada requiera una alta concentración de agente farmacéutico o biológico que puede no ser alcanzable por la administración sistémica. El recubrimiento puede proporcionar una liberación controlada, incluyendo a largo plazo o una liberación sostenida, de un producto farmacéutico o agente biológico. Además, los implantes biomédicos pueden recubrirse con materiales que proporcionen propiedades superficiales beneficiosas, tales como una biocompatibilidad o lubricidad mejoradas.
Convencionalmente, los recubrimientos se han aplicado por procesos tales como la inmersión, pulverización, deposición de vapor, polimerización por plasma, y electro-deposición. Aunque estos procesos han sido utilizados para producir recubrimientos satisfactorios, hay inconvenientes asociados con los mismos. Por ejemplo, a menudo es difícil lograr recubrimientos de espesor uniforme y prevenir la aparición de defectos (por ejemplo, puntos desnudos). También, en muchos procesos, múltiples pasos de recubrimiento son con frecuencia necesarios, que por lo general requieren el secado entre o después de las etapas de recubrimiento.
Otra desventaja de la mayoría de los métodos convencionales es que muchos agentes farmacéuticos o biológicos, una vez depositados sobre un sustrato, sufren de una biodisponibilidad mala, reducción de vida útil, estabilidad mala in vivo o tasas de elución incontrolables, a menudo atribuibles a un mal control de la morfología y/o estructura secundaria del agente. Los agentes farmacéuticos presentan retos significativos de control de la morfología cuando se utilizan técnicas de recubrimiento por pulverización existentes, que convencionalmente implican que una solución que contiene los agentes farmacéuticos sea pulverizada sobre un sustrato. A medida que el disolvente se evapora los agentes normalmente permanecen en estado amorfo. La falta de o bajo grado de cristalinidad del agente recubierto por aerosol puede conducir a la disminución de la vida útil y a la elución demasiado rápida del fármaco. Los agentes biológicos se basan típicamente, al menos en parte, en sus estructuras secundarias, terciarias y/o cuaternarias para su actividad. Si bien el uso de técnicas de recubrimiento por pulverización convencionales basadas en disolventes puede resultar con éxito en la deposición de un agente biológico sobre un sustrato, a menudo producirá la pérdida de al menos parte de la estructura secundaria, terciaria y/o cuaternaria del agente y por lo tanto, una pérdida correspondiente de la actividad. Por ejemplo, muchas proteínas pierden actividad cuando se formulan en matrices de soporte como resultado de los métodos de procesamiento.
Los procesos de recubrimiento por pulverización a base de disolventes convencionales también se ven obstaculizados por las ineficiencias relacionadas con la recogida de los constituyentes del recubrimiento sobre el sustrato y la consistencia del recubrimiento final. A medida que el tamaño del sustrato disminuye, y que la complejidad mecánica aumenta, es cada vez más difícil recubrir uniformemente todas las superficies de un sustrato.
Lo que se necesita es un método rentable para depositar polímeros inertes y agentes farmacéuticos o biológicos sobre un sustrato, donde el proceso de recogida es eficiente, el recubrimiento producido es conformado, sustancialmente libre de defectos y uniforme, la composición del recubrimiento puede ser regulada y la morfología y/o estructura secundaria de los agentes farmacéuticos o biológicos pueden ser controladas. El método por lo tanto permitiría la conservación estructural y morfológica de los agentes depositados durante el proceso de recubrimiento.
Compendio de la invención
En el método de la invención, pueden usarse métodos para depositar un recubrimiento que comprende un polímero y un agente farmacéutico sobre un sustrato, que comprenden la descarga de al menos un agente farmacéutico en una morfología terapéuticamente deseable en forma de polvo seco a través de un primer orificio; la descarga de al menos un polímero en forma de polvo seco a través de un segundo orificio; la deposición de las partículas de polímero y/o fármaco sobre dicho sustrato, en donde se mantiene un potencial eléctrico entre el sustrato y las
partículas de polímero y/o fármaco, de tal modo que se forme dicho recubrimiento; y la sinterlzaclón de dicho recubrimiento bajo condiciones que no modifiquen sustancialmente la morfología de dicho agente farmacéutico.
Aunque el tamaño, resistividad y contenido de humedad del polímero y agente farmacéutico pueden variar ampliamente en base a las condiciones usadas, los tamaños de partícula deseados están típicamente en el Intervalo de ,1 pm - 25 pm, y más preferiblemente en el intervalo de ,1 pm -1 pm, la resistividad está típicamente en el Intervalo de aproximadamente 16 Qm a aproximadamente 124 Qm y el contenido de humedad es menor del 5% en peso. En una forma de realización de la invención, el intervalo de peso molecular del polímero es de aproximadamente 5. u.a. a aproximadamente 1. u.a. En otras formas de realización, el primer y segundo orificio se proporciona como un único orificio en el que el agente farmacéutico y el polímero se pueden mezclar juntos antes de ser descargados. En aún otras formas de realización las partículas de polímero y de agente farmacéutico pueden ser descargadas simultáneamente o en sucesión. En otra forma de realización de la Invención el método comprende además descargar un tercer polvo seco que comprende un segundo agente farmacéutico mediante el cual se deposita sobre dicho sustrato un recubrimiento que comprende al menos dos agentes farmacéuticos diferentes, como se define en las reivindicaciones. La morfología terapéuticamente deseable de dicho agente farmacéutico es cristalina o semi-cristalina, en donde según la invención el fármaco macrólldo inmunosupresor en el stent es al menos 5% cristalino. En ciertas otras formas de realización de la Invención el agente farmacéutico se prepara por molienda, molienda de chorro, granulación, secado por pulverización, cristalización o fluidización y en una forma de realización preferida, la morfología terapéuticamente deseable no se cambia sustancialmente después de la etapa de sinterizado del recubrimiento. En una forma de realización adicional, el agente farmacéutico y/o el polímero se vuelve cargado electrostáticamente antes de la deposición, y el sustrato puede ser conectado eléctricamente a tierra. En una forma de realización preferida, el sustrato se carga electrostáticamente. En algunas formas de realización, el polímero y agente farmacéutico se descargan usando un propelente a base de gas, que típicamente comprende dióxido de carbono, óxido nitroso, hidrofluorocarbonos, clorofluorocarbonos, helio, nitrógeno, aire comprimido, argón, o hidrocarburos volátiles con una presión de vapor superior a 1 kPa (75 Torr) a 2° C, y es preferiblemente dióxido de carbono. Según la invención, el stent comprende un primer y un segundo agente farmacéutico seleccionado de dos clases diferentes. El stent puede comprender al menos un fármaco, seleccionado de Sirolimus, Tacrolimus, Everolimus, Zotarolimus, yTaxol. En una forma de realización de la invención, la relación de agente farmacéutico a polímero es de aproximadamente 1:5 a aproximadamente 5:1. En algunas formas de realización, la cantidad de agente farmacéutico dependerá del agente particular que se emplee, el tipo de sustrato, y la condición médica que se está tratando. Típicamente,... [Seguir leyendo]
Reivindicaciones:
1. Un método de preparación de un stent coronario de elución de multifármacos que comprende:
a. proporcionar una estructura de stent;
b. depositar sobre dicha estructura de stent una primera capa que comprende un primer agente
farmacéutico;
c. depositar una segunda capa que comprende un segundo agente farmacéutico;
donde dicho primero y segundo agentes farmacéuticos se seleccionan a partir de dos clases diferentes de agentes farmacéuticos,
en donde los agentes farmacéuticos comprenden un fármaco macrólido inmunosupresor (limus), y en donde dicho 1 fármaco macrólido inmunosupresor es al menos 5% cristalino.
2. El método de la reivindicación 1, en donde dicho fármaco macrólido inmunosupresor es al menos 7%, preferiblemente 9%, cristalino.
3. El método de la reivindicación 1, en donde dicho fármaco macrólido inmunosupresor está en forma de polvo.
4. Un stent coronario de elución de multifármacos preparado por el método de la reivindicación 1.
Patentes similares o relacionadas:
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Granulados secos de polvos de sílice mesoporosa, del 1 de Julio de 2020, de FORMAC PHARMACEUTICALS N.V: Un granulado seco que comprende desde el 50% al 100% p/p de sílice mesoporosa ordenada que tiene una organización bidimensional hexagonalmente […]
Composiciones bucales antimicrobianas basadas en sílice, del 1 de Julio de 2020, de Evonik Operations GmbH: Una composición bucal que comprende: (i) un vehículo; (ii) de 0,02 a 2 % p. de un compuesto antimicrobiano catiónico; y (iii) de 0,1 a 4,5 % p. de […]
Formulaciones de inulina y de acetato de inulina, del 5 de Junio de 2020, de SOUTH DAKOTA STATE UNIVERSITY (100.0%): Una composición que comprende micropartículas o nanopartículas de acetato de inulina (InAc) y una molécula de carga, en la que la molécula de carga está encapsulada […]
Composición farmacéutica que comprende partículas de quelante de fosfato, del 3 de Junio de 2020, de Vifor Fresenius Medical Care Renal Pharma, Ltd: Una composición farmacéutica para administración oral, que comprende un quelante de fosfato, donde dicho quelante de fosfato comprende partículas que tienen una distribución […]
Formulaciones de ganaxolona y procedimientos para la preparación y uso de las mismas, del 3 de Junio de 2020, de Marinus Pharmaceuticals, Inc: Una composición que comprende partículas que comprenden ganaxolona; un polímero hidrófilo; un agente humectante; y un agente complejante, en la que el diámetro medio ponderado […]
Procedimiento de estabilización de tamaño de partícula, del 27 de Mayo de 2020, de INKE, S.A.: Un procedimiento para obtener una sal de glicopirronio estable que comprende las siguientes etapas: a) micronizar la sal de bromuro de glicopirronio, opcionalmente […]
Formulaciones de {2-[(1S)-1-(3-etoxi-4-metoxi-fenil)-2-metanosulfonil-etil]-3-oxo-2,3-dihidro-1H-isoindol-4-il}-amida del ácido ciclopropanocarboxílico, del 20 de Mayo de 2020, de Amgen (Europe) GmbH: Una forma de dosificación oral que comprende: 1) una dispersión sólida amorfa de un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente […]