Endoprótesis para flujo de sangre mejorado.
Endoprótesis (300; 600) expandible por balón para su implantación en una luz de un vaso sanguíneo,
que tiene un diseño de pared que es preferiblemente expandible en algunas ubicaciones dando como resultado una forma expandida predeterminada de la endoprótesis, en la que, en dicha forma expandida predeterminada, dicha endoprótesis (300, 600) comprende:
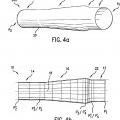
un primer segmento (12) de endoprótesis que tiene una primera área (A1) de sección transversal y un segundo segmento (14) de endoprótesis que tiene una segunda área (A2) de sección transversal y que están longitudinalmente desviados uno con respecto al otro y que tienen cada uno un área de sección transversal constante,
un tercer segmento (16) de endoprótesis configurado para adoptar una configuración de sección decreciente en un estado expandido de la endoprótesis,
un cuarto segmento (22) de endoprótesis que conecta el primer segmento (12) de endoprótesis con el tercer segmento (16) de endoprótesis,
un quinto segmento (24) de endoprótesis que conecta el tercer segmento (16) de endoprótesis con el segundo segmento (14) de endoprótesis,
en la que
dicho cuarto segmento (22) de endoprótesis es un segmento de entrada divergente configurado para adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y primero; y dicho quinto segmento (24) de endoprótesis es un segmento de salida divergente configurado para adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y segundo en el estado expandido de la endoprótesis.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09005594.
Solicitante: MEDINOL LTD..
Nacionalidad solicitante: Israel.
Dirección: Kiryat Atidim, Bldg. 8 Tel Aviv 6158101 ISRAEL.
Inventor/es: EDELMAN,ELAZER, RICHTER,YORAM.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/86 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Stents formados por elementos filiformes; Stents formados por estructuras en forma de red o malla.
- A61F2/95 A61F 2/00 […] › Instrumentos especialmente adaptados para la colocación o eliminación de stents o injertos stent.
PDF original: ES-2546625_T3.pdf
Fragmento de la descripción:
Campo de la invención
La presente invención se refiere de manera general a dispositivos médicos implantables, y más particularmente a endoprótesis implantables para mantener la permeabilidad de una luz.
Antecedentes de la invención
Se conocen muchos factores que pueden contribuir a, y/o empeorar, una oclusión de un vaso o luz corporal. Tales factores incluyen lesión vascular inducida de manera interna, tal como, por ejemplo, lesión vascular provocada por una acumulación de placa en las paredes de la luz, o lesión vascular inducida de manera externa, tal como lesión vascular provocada por el despliegue de una endoprótesis y/o mediante angioplastia. Cuando una luz experimenta una lesión, glóbulos blancos y otras sustancias tienden a converger en la región lesionada de la luz provocando efectos inflamatorios en esa región. Estos efectos inflamatorios tienden a dar como resultado una oclusión de la luz, es decir, un estrechamiento indeseado de la luz o un bloqueo total de la luz. En el caso de una lesión inducida de manera externa que resulta del despliegue de una endoprótesis, los efectos inflamatorios tienden algunas veces a contribuir a lo que se denomina reestenosis, o nueva oclusión de la luz.
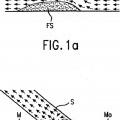
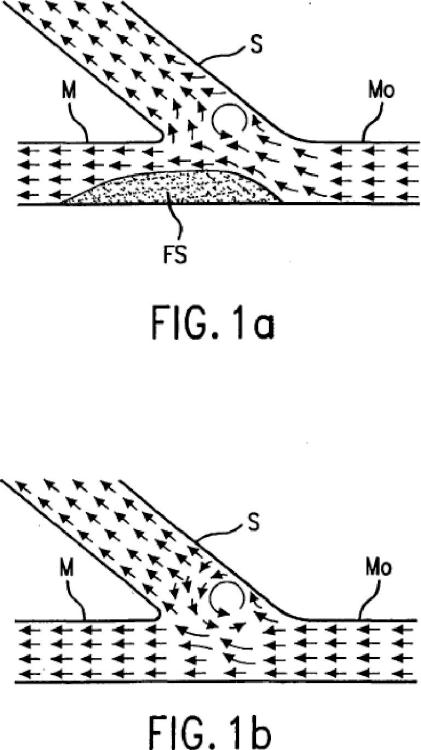
Además, en la luz puede haber zonas con alteraciones de flujo. La vasculatura en el cuerpo humano es un árbol de luces divergentes con patrones divergentes dicotómicos típicos. Los patrones divergentes dicotómicos crean bifurcaciones en el sistema arterial en las que la luz principal se divide en dos luces secundarias. En la mayoría de los casos, una de las ramificaciones secundarias es más grande y es la continuación del vaso principal y la otra es más pequeña y es la ramificación lateral. (El sistema venoso es básicamente la imagen especular de estas bifurcaciones en la que el flujo es desde luces más pequeñas hacia las más grandes, o en el sentido de flujo puede describirse este sistema como convergente en lugar de divergente). La presente invención se basa en parte en una observación de que puede provocarse o empeorarse una lesión vascular, entre otras cosas, por alteraciones de flujo en el flujo de sangre a una región dada de la luz. Estas alteraciones de flujo incluyen zonas de "separación de flujo", en las que se crean vórtices junto a la pared del vaso, haciendo que la sangre quede esencialmente estancada en esas ubicaciones. Tales zonas de separación de flujo son un problema particular en lesiones bifurcadas. Sin embargo, incluso las luces con un diámetro sustancialmente constante pueden tener zonas con separación de flujo indeseable u otras alteraciones de flujo.
Tales alteraciones pueden actuar para aumentar la probabilidad de inflamación aumentando el tiempo de residencia para células inflamatorias cerca de las paredes de la luz, y reduciendo las fuerzas de flujo que podrían empujar de otro modo a esas células aguas abajo. A su vez, esto puede aumentar la probabilidad de que tales glóbulos blancos penetren en la pared e inicien un efecto inflamatorio, lo cual puede dar como resultado un estrechamiento indeseable de la luz. Una alteración de flujo también puede ser un instigador de la disfunción de células endoteliales (ya sea debido a una disminución de la tensión de cizalladura de fluido en la pared, imposición de tensión de cizalladura bidireccional o de otro modo) que entonces fomenta la aparición de una reacción inflamatoria. Finalmente, la alteración de flujo puede provocar o empeorar una lesión vascular fomentando la sedimentación de partículas e inhibiendo un transporte apropiado de materiales residuales desde la pared del vaso al interior de la luz. Aunque no se entiende completamente el mecanismo o los mecanismos precisos mediante los cuales la alteración de flujo acelera el crecimiento de lesiones vasculares, se cree que evitar la alteración de flujo reducirá el riesgo de estrechamiento o nuevo estrechamiento de los vasos.
Además, un procedimiento de angioplastia típico provoca traumatismo a la pared del vaso. El procedimiento de angioplastia se realiza normalmente en la zona de mayor constricción en un vaso, es decir, en la ubicación de una lesión. Si se implanta una endoprótesis en esta zona, pueden presentarse alteraciones de flujo.
Sin limitar el alcance de la presente invención, hay al menos tres factores que pueden influir en la presencia de alteraciones de flujo en zonas de constricción. En primer lugar, es poco probable que la lesión se forme por casualidad, pocas veces las lesiones se forman por casualidad. Debe haber un motivo por el cual la lesión se localiza en un lugar particular. Es más que probable que este lugar sea para empezar un punto de alteración de flujo. En el mejor de los casos, las endoprótesis según la técnica anterior no alteran la geometría de un vaso sino que más bien lo devuelven a la geometría original. Por tanto, hay muchas posibilidades de que la geometría con endoprótesis incluya la alteración de flujo.
Por tanto, un procedimiento de angioplastia o endoprótesis aumenta probablemente los efectos inflamatorios. En primer lugar, tal como se describió anteriormente, cualquier alteración de flujo puede aumentar el tiempo de residencia para células inflamatorias cerca de las paredes del vaso incluso en ausencia de lesión, y/o afectar adversamente a la función de células endoteliales. En segundo lugar, la lesión vascular provocada por la angioplastia y/o el despliegue de endoprótesis potencia la probabilidad de inflamación, incluso en ausencia de alteración de flujo.
Además, al contrario que el despliegue de endoprótesis óptimo comentado anteriormente, con frecuencia las endoprótesis no se despliegan de manera óptima, introduciendo por tanto una nueva alteración de flujo en el sistema. Esto puede ser debido a que no presentan sección decreciente adecuada (lo cual es un problema particular con endoprótesis de bifurcación dedicadas convencionales), o debido a que se despliegan en un vaso curvado y alteran la curvatura, o debido a un soporte inferior al óptimo de una lesión difícil o simplemente debido a la naturaleza del diseño de la endoprótesis, o debido a que la mayoría de las endoprótesis (y particularmente aquellas que son endoprótesis de bifurcación dedicadas) no tienen un ángulo de sección decreciente.
Se conocen endoprótesis que presentan sección decreciente.
El documento US 6.120.534 da a conocer un aparato y métodos para regular el flujo de fluidos a través de un vaso u órgano del organismo mediante una endoprótesis que comprende una malla deformable cubierta con un material biocompatible, teniendo la malla una parte cónica y una región constreñida. La endoprótesis puede colocarse y desplegarse por vía percutánea y transluminal en un vaso. Entonces puede ensancharse selectivamente la región constreñida empleando un dispositivo de dilatación convencional para ajustar la impedancia del flujo creada por la región constreñida. En una realización alternativa, una región constreñida se forma preferiblemente a partir de un material con memoria de forma, de modo que puede recuperarse el grado máximo de constricción calentando el material con memoria de forma. Sin embargo, en esta endoprótesis, sólo las partes de la endoprótesis con los diámetros más grandes, y no las regiones constreñidas, se expanden hasta entrar directamente en contacto con la pared de la arteria. Además, la endoprótesis de Ruiz no altera la forma de la pared de la arteria, y el espacio del vaso encerrado natural, es decir, la luz, no se cambia tras la implantación. Ruiz simplemente crea una nueva forma (tal como se define por las partes interiores de la endoprótesis) dentro del vaso a través de la cual puede fluir la sangre, sin alterar la propia pared del vaso previamente enfermada.
El documento WO 97/17101 da a conocer un balón tal como para dimensionar una endoprótesis tubular implantable que se ha colocado dentro de un ostium. Se coloca dentro del ostium coronario derecho, y el balón de sección decreciente de la presente invención se coloca dentro de la endoprótesis para proporcionar una dilatación hacia fuera radial en el extremo proxlmal de la endoprótesis. El extremo proximal de la endoprótesis se presiona de vuelta contra la pared de la aorta rodeando el ostium coronario derecho, minimizando así cualquier obstrucción para el flujo sanguíneo en la aorta, y reduciendo posiblemente el riesgo de reestenosis en el ostium coronario derecho.
Por ejemplo, la patente estadounidense n.° 5.827.321 concedida a Roubin et al. da a conocer una endoprótesis de sección decreciente. Sin embargo, las endoprótesis dadas a conocer en esa patente presentan sección decreciente para proporcionar un ajuste optimizado entre la geometría original y la sección tratada... [Seguir leyendo]
Reivindicaciones:
1. Endoprótesis (300; 600) expandióle por balón para su implantación en una luz de un vaso sanguíneo, que tiene un diseño de pared que es preferiblemente expandióle en algunas ubicaciones dando como resultado 5 una forma expandida predeterminada de la endoprótesis, en la que, en dicha forma expandida
predeterminada, dicha endoprótesis (300, 600) comprende:
un primer segmento (12) de endoprótesis que tiene una primera área (A1) de sección transversal y un segundo segmento (14) de endoprótesis que tiene una segunda área (A2) de sección transversal y que 10 están longitudinalmente desviados uno con respecto al otro y que tienen cada uno un área de sección
transversal constante,
un tercer segmento (16) de endoprótesis configurado para adoptar una configuración de sección decreciente en un estado expandido de la endoprótesis,
un cuarto segmento (22) de endoprótesis que conecta el primer segmento (12) de endoprótesis con el tercer segmento (16) de endoprótesis,
un quinto segmento (24) de endoprótesis que conecta el tercer segmento (16) de endoprótesis con el 20 segundo segmento (14) de endoprótesis,
en la que
dicho cuarto segmento (22) de endoprótesis es un segmento de entrada divergente configurado para 25 adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de
endoprótesis tercero y primero; y dicho quinto segmento (24) de endoprótesis es un segmento de salida divergente configurado para adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y segundo en el estado expandido de la endoprótesis.
2. Endoprótesis (300; 600) autoexpandible para su implantación en una luz de un vaso sanguíneo, que tiene
una forma expandida predeterminada, en la que, en dicha forma expandida predeterminada, dicha endoprótesis (300, 600) comprende:
un primer segmento (12) de endoprótesis que tiene una primera área (A1) de sección transversal y un 35 segundo segmento (14) de endoprótesis que tiene una segunda área (A2) de sección transversal y que
están longitudinalmente desviados uno con respecto al otro y que tienen cada uno un área de sección transversal constante,
un tercer segmento (16) de endoprótesis configurado para adoptar una configuración de sección 40 decreciente en un estado expandido de la endoprótesis,
un cuarto segmento (22) de endoprótesis que conecta el primer segmento (12) de endoprótesis con el tercer segmento (16) de endoprótesis,
un quinto segmento (24) de endoprótesis que conecta el tercer segmento (16) de endoprótesis con el
segundo segmento (14) de endoprótesis,
en la que
dicho cuarto segmento (22) de endoprótesis es un segmento de entrada divergente configurado para
adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y primero; y dicho quinto segmento (24) de endoprótesis es un segmento de salida divergente configurado para adoptar una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y segundo en el estado expandido de la endoprótesis.
3. Endoprótesis (300) según la reivindicación 1 ó 2, en la que los segmentos (12 y 14) primero y segundo están dotados de diferentes áreas de sección transversal uno en comparación con el otro.
4. Endoprótesis (600) según la reivindicación 1 ó 2, en la que los segmentos (12 y 14) primero y segundo
están dotados de las mismas áreas de sección transversal uno en comparación con el otro.
5. Endoprótesis (300; 600) según la reivindicación 1, en la que dicha endoprótesis está configurada para expandirse sobre un balón (34) de colocación expandióle para obtener una forma no uniforme para configurar dicha endoprótesis tal como para tener una forma no uniforme.
6. Endoprótesis (300; 600) según la reivindicación 1 ó 2, en la que una sección transversal de cualquier
sección de endoprótesis de la endoprótesis en un plano normal a un eje longitudinal de la misma es circular.
Balón (34) de colocación para desplegar la endoprótesis (300; 600) según la reivindicación 1, estando el balón (34) configurado para inflarse para expandir la endoprótesis en una luz de tal manera que, en un estado expandido de la endoprótesis, el primer segmento (12) de endoprótesis tiene la primera área de sección transversal de segmento de endoprótesis, el segundo segmento (14) de endoprótesis tiene la segunda área de sección transversal de segmento de endoprótesis, el tercer segmento (16) de endoprótesis tiene una tercera configuración de sección de segmento de sección decreciente, el cuarto segmento (22) de endoprótesis tiene una cuarta configuración de endoprótesis de sección decreciente, y un quinto segmento (24) de endoprótesis tiene una quinta configuración de endoprótesis de sección decreciente, en el que el balón incluye:
un primer segmento (112) de balón configurado para tener una primera área de sección transversal de segmento de balón en un estado inflado del balón para expandir el primer segmento de endoprótesis a la primera área de sección transversal de segmento (12) de endoprótesis;
un segundo segmento (114) de balón longitudinalmente desviado con respecto al primer segmento (112) de balón y configurado para tener una segunda área de sección transversal de segmento de balón en un estado inflado del balón para expandir el segundo segmento (14) de endoprótesis a la segunda área de sección transversal de segmento de endoprótesis;
un tercer segmento (116) de balón configurado para adoptar una configuración de segmento de balón de sección decreciente en un estado inflado del balón para expandir el tercer segmento (16) de endoprótesis a una tercera configuración de sección de endoprótesis de sección decreciente,
un cuarto segmento (122) de balón configurado para adoptar una configuración de segmento de balón de sección decreciente en un estado inflado del balón para expandir el cuarto segmento (22) de endoprótesis a una cuarta configuración de segmento de endoprótesis de sección decreciente, que es una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y primero, y
un quinto segmento (124) de balón configurado para adoptar una configuración de segmento de balón de sección decreciente en un estado inflado del balón para expandir el quinto segmento (24) de endoprótesis a una quinta configuración de segmento de endoprótesis de sección decreciente, que es una configuración de sección decreciente divergente y coextensiva con los segmentos (16 y 12) de endoprótesis tercero y segundo.
Balón (34) según la reivindicación 7, en el que la segunda área de sección transversal de segmento de balón es diferente de la primera área de sección transversal de segmento de balón.
Balón (34) según la reivindicación 7, en el que la segunda área de sección transversal de segmento de balón es igual a la primera área de sección transversal de segmento de balón.
Kit (33) para desplegar una endoprótesis (300; 600) que comprende la endoprótesis (300; 600) según cualquiera de las reivindicaciones 1 y 3 a 6, incluyendo además el kit (33) el balón (34) de colocación según cualquiera de las reivindicaciones 7 a 9.
Patentes similares o relacionadas:
Dispositivos para formar una anastomosis, del 22 de Julio de 2020, de BOSTON SCIENTIFIC SCIMED, INC.: Un stent que comprende: un cuerpo del stent formado por una trenza de filamentos tejidos que tiene una configuración constreñida, teniendo […]
Anclaje de fijación de dispositivo médico dotado de propiedades de compactación y administración mejoradas, del 6 de Mayo de 2020, de W.L. GORE & ASSOCIATES, INC.: Un dispositivo médico anclable que comprende un anclaje que tiene: a. una parte de sujeción del dispositivo que sujeta el dispositivo al anclaje […]
Un aparato para enderezar y aplanar la pared lateral de un lumen corporal o una cavidad corporal, a fin de proporcionar la exposición tridimensional de una lesión o anormalidad dentro del lumen corporal o la cavidad corporal, y/o para estabilizar un instrumento en relación con los mismos, del 11 de Marzo de 2020, de CORNELL UNIVERSITY (100.0%): Un aparato para enderezar y aplanar una pared lateral de un lumen corporal o una cavidad corporal, a fin de proporcionar la exposición […]
Un diseño de anillo de expansión para el accesorio de trenza, del 11 de Diciembre de 2019, de DePuy Synthes Products, Inc: Un sistema de endoprótesis vascular trenzada, comprendiendo el sistema: un cuerpo de endoprótesis vascular que tiene una luz formada por una pluralidad de miembros […]
Dispositivo de captura dual para el sistema de injerto de stent, del 6 de Noviembre de 2019, de Bolton Medical Inc: Un sistema de administración para administrar y desplegar una prótesis que tiene un stent descubierto proximal que incluye ápices proximales […]
 Stent plegable, del 25 de Septiembre de 2019, de University Hospitals Of Leicester NHS Trust: Un stent que comprende una parte final que, en un estado expandido, delimita una pared de soporte del vaso , que tiene un extremo libre que delimita […]
Stent plegable, del 25 de Septiembre de 2019, de University Hospitals Of Leicester NHS Trust: Un stent que comprende una parte final que, en un estado expandido, delimita una pared de soporte del vaso , que tiene un extremo libre que delimita […]
Anillo de expansión para un ''stent'' trenzado, del 17 de Julio de 2019, de DePuy Synthes Products, Inc: Un sistema de 'stent' trenzado, que comprende: un cuerpo del 'stent' que tiene un conducto formado por diversos miembros o componentes trenzados que contienen […]
Endoprótesis para mejorar el flujo sanguíneo, del 3 de Julio de 2019, de MEDINOL LTD.: Conmutador de protección para la interrupción de corriente continua, en particular de un sistema de cableado de un vehículo , con una vía de corriente […]