Comprimidos bicapa que comprenden elvitegravir, cobicistat, emtricitabina y tenofovir.
Un comprimido que comprende una primera capa y una segunda capa en el que;
a) la primera capa comprende:
un compuesto de Fórmula I:**Fórmula**
y
un compuesto de Fórmula II:**Fórmula**
y opcionalmente un vehículo farmacéuticamente aceptable; y
b) la segunda capa comprende:
un compuesto de Fórmula III:**Fórmula**
y
una sal de fórmula IV:**Fórmula**
y opcionalmente un vehículo farmacéuticamente aceptable.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/023226.
Solicitante: GILEAD SCIENCES, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 333 LAKESIDE DRIVE FOSTER CITY, CA 94404 ESTADOS UNIDOS DE AMERICA.
Inventor/es: OLIYAI, REZA, MENNING,MARK,M, KOZIARA,JOANNA M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/47 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Quinoleínas; Isoquinoleínas.
- A61K31/513 A61K 31/00 […] › teniendo grupos oxo unidos directamente al heterociclo, p. ej. citosina.
- A61K31/522 A61K 31/00 […] › teniendo grupos oxo unidos directamente al heterociclo, p. ej. hipoxantina, guanina, aciclovir.
- A61K31/5377 A61K 31/00 […] › no condensadas y conteniendo otros heterociclos, p. ej. timolol.
- A61K47/24 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › que contienen átomos distintos al carbono, hidrógeno, oxígeno, halógenos, nitrógeno o azufre, p. ej. ciclometicona o fosfolípidos.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61K9/24 A61K 9/00 […] › en dosis unitarias constituidas por capas u hojas.
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
- A61P31/18 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para el VIH.
PDF original: ES-2548886_T3.pdf
Fragmento de la descripción:
Comprimidos bicapa que comprenden elvitegravir, cobicistat, emtricitabina y tenofovir 5 Antecedentes
El documento US 7.176.220 divulga compuestos de los que se dice que son útiles como inhibidores de la integrasa. Un compuesto particular es el compuesto de Fórmula I (es decir, elvitegravir).
CH3
" xh3
h3
10 I
**(Ver fórmula)** **(Ver fórmula)**El documento WO 2005/113508 proporciona ciertas formas cristalinas específicas del compuesto de Fórmula I. Se describe que las formas cristalinas específicas tienen una estabilidad física y química superior en comparación con otras formas físicas del compuesto.
El documento WO 2008/010921 describe compuestos que mejoran la farmacocinética de un fármaco coadministrado mediante la inhibición de la citocromo P450 monooxigenasa. Uno de estos inhibidores es el compuesto de Fórmula
**(Ver fórmula)**El documento WO 2008/010921 también describe composiciones farmacéuticas que comprenden los compuestos y proporciona composiciones que incluyen al menos un agente terapéutico adicional. En las páginas 170 y 174, el documento WO 2008/010921 describe además combinaciones de los compuestos divulgados (por ejemplo, un 25 compuesto de Fórmula II). En la enumeración de los diferentes agentes está incluido el compuesto de Fórmula I (es decir, elvitegravir), el compuesto de Fórmula III (es decir, emtricitabina) y la sal de Fórmula IV (es decir, tenofovir disoproxil fumarato). En las páginas 159-168 también se hace una descripción relativa a las formulaciones de los compuestos.
**(Ver fórmula)**El documento WO 2008/103949 también divulga compuestos de los que se dice que son útiles para modificar la farmacocinética de un fármaco coadministrado mediante la inhibición de la citocromo P450 monooxigenasa. En la página 199 del documento WO 2008/103949 se describe la combinación específica de los compuestos de Fórmula I, 35 Fórmula II, Fórmula III y Fórmula IV. Las formulaciones se describen en las páginas 181-190.
A pesar de estas descripciones, existe actualmente una necesidad de formas farmacéuticas sólidas mejoradas (por ejemplo comprimidos) para la administración de composiciones multi-agente. También hay una necesidad de
mejorar las formas farmacéuticas sólidas que comprenden los compuestos de Fórmulas I, II, III y IV que tienen una estabilidad quimica, estabilidad física, características de liberación o uniformidad de la dosis mayores o aceptables. También hay una necesidad de procesos mejorados para preparar formas farmacéuticas sólidas de las composiciones que comprenden los compuestos de Fórmulas I, II, III y IV.
Sumario de la invención
La presente invención proporciona formas farmacéuticas sólidas (por ejemplo, comprimidos) que comprenden los compuestos de Fórmula I, Fórmula II, Fórmula III y la sal de Fórmula IV y métodos para preparar las formas farmacéuticas sólidas. El solicitante ha descubierto que los comprimidos preparados a modo bicapa tienen propiedades superiores a los comprimidos estructurados alternativamente. Este descubrimiento representa un avance en el desarrollo de la terapia de combinación para el tratamiento de infecciones virales tales como el VIH.
Por consiguiente, en una realización, la invención proporciona un comprimido que comprende una primera capa y una segunda capa en la que;
a) la primera capa comprende:
un compuesto de Fórmula I:
**(Ver fórmula)**OH
y
un compuesto de Fórmula II:
**(Ver fórmula)**y opcionalmente un vehículo farmacéuticamente aceptable;
b) la segunda capa comprende:
un compuesto de Fórmula III:
**(Ver fórmula)**III
y
una sal de fórmula IV:
**(Ver fórmula)**IV
j
y opcionalmente un vehículo farmacéuticamente aceptable.
En una realización, la Invención proporciona una composición farmacéutica que comprende 150 mg ± 10% del compuesto de Fórmula I; 150 mg ±10 % del compuesto de Fórmula II; 200 mg ± 10 % del compuesto de Fórmula III y 300 mg ± 10 % del compuesto de Fórmula IV.
En una realización, la invención proporciona una composición farmacéutica que comprende 150 mg ± 5% del compuesto de Fórmula I; 150 mg ± 5 % del compuesto de Fórmula II; 200 mg ± 5 % del compuesto de Fórmula III y 300 mg ± 5 % del compuesto de Fórmula IV.
En una realización, la invención proporciona una composición farmacéutica que comprende 150 mg ± 2% del compuesto de Fórmula I; 150 mg ± 2 % del compuesto de Fórmula II; 200 mg ± 2 % del compuesto de Fórmula III y 300 mg ± 2 % del compuesto de Fórmula IV.
En una realización, la invención proporciona una composición farmacéutica que consiste en 150 mg ± 5% del compuesto de Fórmula I; 150 mg ± 5 % del compuesto de Fórmula II; 200 mg ± 5 % del compuesto de Fórmula III y 300 mg ± 5 % del compuesto de fórmula IV como principios farmacéuticamente activos y uno o más vehículos farmacéuticamente aceptables.
En una realización, la invención proporciona una composición farmacéutica que consiste en 150 mg ± 2 % del compuesto de Fórmula I; 150 mg ± 2 % del compuesto de Fórmula II; 200 mg ± 2 % del compuesto de Fórmula III y 300 mg ± 2 % del compuesto de Fórmula IV como principios farmacéuticamente activos; y uno o más vehículos farmacéuticamente aceptables.
En una realización, la invención proporciona un comprimido que consiste en lo siguiente:
| Formulación del Compuesto de Fórmula I1150 mg | ||
| Componentes | % p/p | mg/comprimido |
| Compuesto de Fórmula III | 13,9 | 200,0 |
| Sal de fórmula IV | 20,9 | 300,0 |
| Compuesto de Fórmula I | 10,4 | 150,0 |
| Compuesto de Fórmula II | 10,4 | 150,0 |
| Dióxido de silicio coloidal | 12,0 | 172,5 |
| Lactosa monohidrato | 0,8 | 10,9 |
| Celulosa microcristalina | 20,8 | 299,5 |
| Hidroxipropilcelulosa | 0,5 | 7,5 |
| Hidroxipropilcelulosa | 0,6 | 9,0 |
| Laurilsulfato sódico | 0,8 | 11,3 |
| Croscarmelosa sódica | 7,3 | 104,3 |
| Estearato de magnesio | 22,4 | |
| Total | 1437 |
La invención también proporciona métodos para la preparación de comprimidos de la invención que se describen en la presente memoria, así como composiciones intermedias y artículos que son útiles para preparar composiciones de la invención. Por consiguiente, en una realización, la invención proporciona un método para preparar un comprimido de la invención que comprende: comprimir una composición que comprende el compuesto de fórmula I y el compuesto de fórmula II para proporcionar una primera capa prensada; añadir el compuesto de fórmula III y la sal de fórmula IV a la primera capa prensada y comprimir para proporcionar el comprimido de la invención. En una realización de la invención, la composición que comprende el compuesto de fórmula I y el compuesto de fórmula II
se comprime para proporcionar una capa blanda; se añade una mezcla que comprende el compuesto de fórmula III y la sal de fórmula IV a la capa blanda para proporcionar una combinación final y la combinación final se comprime para proporcionar el comprimido de la invención. En una realización, los métodos de la invención pueden comprender además el recubrimiento del comprimido.
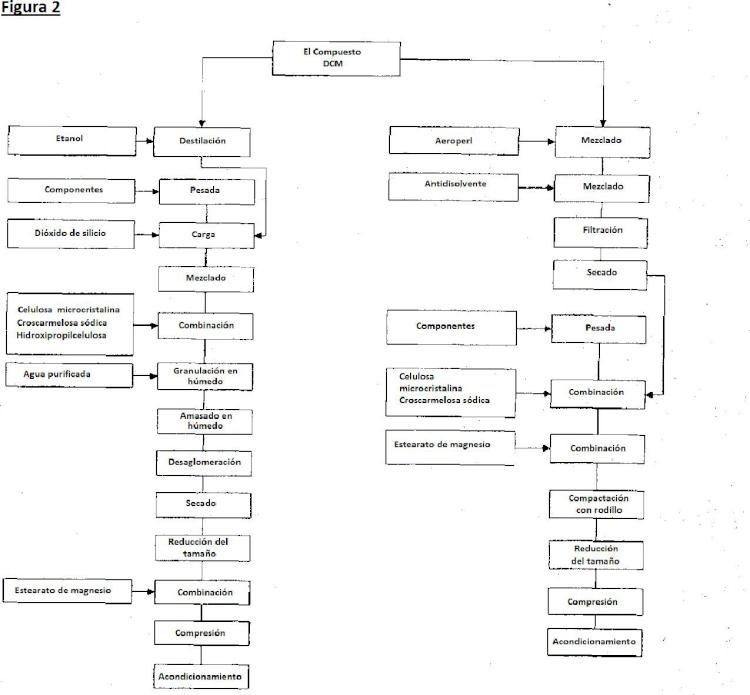
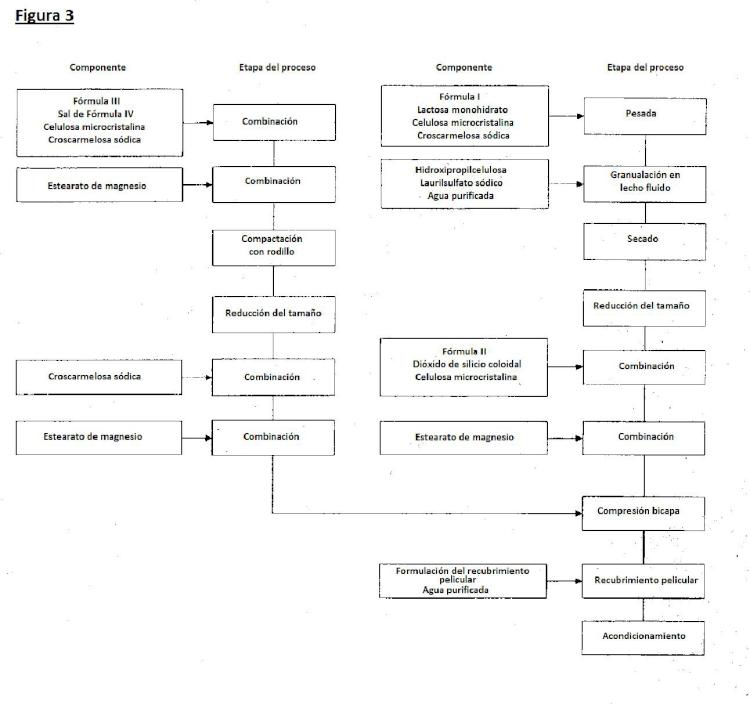
La invención también proporciona los métodos ilustrados en las Figuras 2 y 3 y en los Ejemplos de la presente memoria, que son útiles para la preparación de composiciones intermedias y comprimidos de la invención.
Breve descripción de las figuras
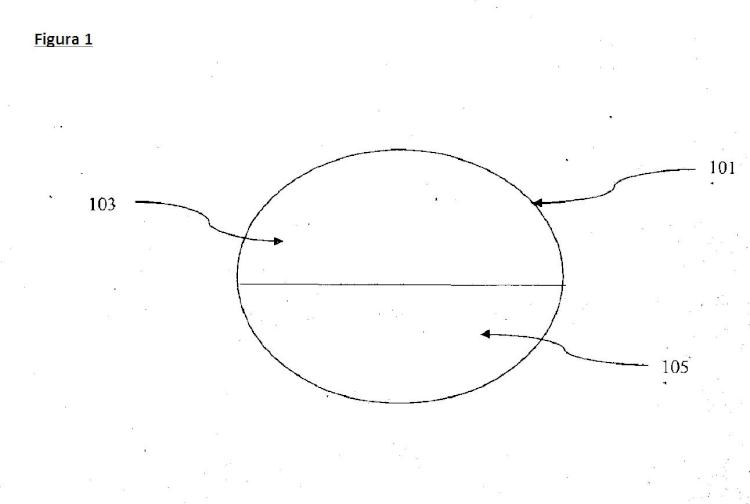
La FIG. 1. ilustra un comprimido de la invención.
La FIG. 2. ilustra la preparación de composiciones de la invención.
La FIG. 3. ilustra la preparación de composiciones de la invención.
Descripción detallada
Los valores específicos enumerados a continuación para los intervalos y términos son sólo ilustrativos, no excluyen otros valores.
... [Seguir leyendo]
Reivindicaciones:
1. Un comprimido que comprende una primera capa y una segunda capa en el que; a) la primera capa comprende: un compuesto de Fórmula I:
**(Ver fórmula)**y opcionalmente un vehículo farmacéuticamente aceptable; y b) la segunda capa comprende:
un compuesto de Fórmula III:
**(Ver fórmula)**y opcionalmente un vehículo farmacéuticamente aceptable.
2. El comprimido de la reivindicación 1 en el que la primera capa está en contacto con la segunda capa.
3. El comprimido de una cualquiera de las reivindicaciones 1-2 en el que la proporción en peso entre el compuesto de Fórmula I y el compuesto de Fórmula II es 1,0 ± 0,5.
4. El comprimido de una cualquiera de las reivindicaciones 1-3 en el que la primera capa comprende además una pluralidad de partículas de sílice.
5. El comprimido de una cualquiera de las reivindicaciones 1-3 en el que el compuesto de Fórmula II está asociado con partículas de sílice.
6. El comprimido de una cualquiera de las reivindicaciones 1-5 que comprende 150 mg ± 10 % del compuesto de Fórmula I; 150 mg ± 10 % del compuesto de Fórmula II; 200 mg ± 10 % del compuesto de Fórmula III y 300 mg ± 10 % del compuesto de Fórmula IV.
7. El comprimido de la reivindicación 6 que comprende 150 mg ± 5 % del compuesto de Fórmula I.
8. El comprimido de la reivindicación 6 que comprende 150 mg ± 2 % del compuesto de Fórmula I.
9. El comprimido de una cualquiera de las reivindicaciones 6-8 que comprende 150 mg ± 5 % del compuesto de Fórmula II.
10. El comprimido de una cualquiera de las reivindicaciones 6-8 que comprende 150 mg ± 2 % del compuesto de Fórmula II.
11. El comprimido de una cualquiera de las reivindicaciones 6-10 que comprende 200 mg ± 5 % del compuesto de Fórmula III.
12. El comprimido de una cualquiera de las reivindicaciones 6-10 que comprende 200 mg ± 2 % del compuesto de Fórmula III.
13. El comprimido de una cualquiera de las reivindicaciones 6-12 que comprende 300 mg ± 5 % de la sal de Fórmula
IV.
14. El comprimido de una cualquiera de las reivindicaciones 6-12 que comprende 300 mg ± 2 % de la sal de Fórmula
IV.
15. El comprimido de una cualquiera de las reivindicaciones 1-14, que comprende además un vehículo farmacéuticamente aceptable.
16. El comprimido de una cualquiera de las reivindicaciones 1-15, que está formulado en una forma farmacéutica unitaria.
17. El comprimido de una cualquiera de las reivindicaciones 1-16, que está formulado para la administración una vez al día.
18. Un método para preparar un comprimido como se describe en la reivindicación 1 que comprende: comprimir una composición que comprende el compuesto de fórmula I y el compuesto de fórmula II para proporcionar una primera capa prensada; añadir el compuesto de fórmula III y la sal de fórmula IV a la primera capa prensada y comprimir para obtener el comprimido.
19. Un comprimido como se describe en la reivindicación 1 que consiste en lo siguiente:
| Componentes | Formulación del Compuesto de Fórmula II 150 mg | |
| % p/p | mg/comprlmido | |
| Compuesto de Fórmula III | 13,9 | 200,0 |
| Sal de fórmula IV | 20,9 | 300,0 |
| Compuesto de Fórmula I | 10,4 | 150,0 |
| Compuesto de Fórmula II | 10,4 | 150,0 |
| Dióxido de silicio coloidal | 12,0 | 172,5 |
| Lactosa monohidrato | 0,8 | 10,9 |
| Celulosa microcristalina | 20,8 | 299,5 |
| Hidroxipropilcelulosa | 0,5 | 7,5 |
| Hidroxipropilcelulosa | 0,6 | 9,0 |
| Laurilsulfato sódico | 0,8 | 11,3 |
| Croscarmelosa sódica | 7,3 | 104,3 |
| Estearato de magnesio | 22,4 | |
| Total | 1437, |
20. Un comprimido preparado como se describe en la reivindicación 18.
Patentes similares o relacionadas:
Sal de sodio del inhibidor del transportador de ácido úrico y de su forma cristalina, del 1 de Julio de 2020, de Jiangsu Hengrui Medicine Co., Ltd: 1-((6-bromoquinolin-4-il)tio)ciclobutano-1-carboxilato de sodio de fórmula (I), **(Ver fórmula)**
Anticuerpo anti-Notch 4 humano, del 1 de Julio de 2020, de EISAI R&D MANAGEMENT CO., LTD: Un anticuerpo anti-Notch4 o un fragmento de unión a Notch4 de este, donde dicho anticuerpo o un fragmento de unión a Notch4 de este comprende cadenas pesadas y ligeras y […]
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular, del 27 de Mayo de 2020, de Global Blood Therapeutics, Inc: Un compuesto de Fórmula (I): **(Ver fórmula)** o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento […]
Proteínas de unión a antígeno para proproteína convertasa subtilisina kexina tipo 9 (PCSK9), del 6 de Mayo de 2020, de AMGEN INC.: Una proteína de unión a antígeno, donde dicha proteína de unión a antígeno (i) comprende (a) un dominio variable de cadena ligera que comprende una secuencia […]
Composiciones congeladas fluidas que comprenden un agente terapéutico, del 8 de Abril de 2020, de Tavakoli, Zahra: Una composición fluida congelada que comprende un agente terapéutico y al menos un agente aromatizante para su uso en terapia, donde dicha composición […]
COMBINACIÓN FARMACÉUTICA SINÉRGICA DE UN ANTAGONISTA DE LOS RECEPTORES DE LEUCOTRIENOS Y UN AGONISTA INVERSO DE LA HISTAMINA H1, del 2 de Abril de 2020, de AMEZCUA AMEZCUA, Federico: La presente invención se refiere a una composición farmacéutica que comprende la combinación sinérgica de un antagonista de los receptores de […]
Moduladores de la ruta de hedgehog, del 1 de Abril de 2020, de NOVARTIS AG: Un compuesto que tiene la estructura seleccionada de: **(Ver fórmula)** en la que: L1 se selecciona de un enlace, -O-, -O(CR14R14)m-, -(CR14R14)mO- […]
Formulación compuesta, que comprende un comprimido esferoidal de múltiples unidades (MUST) encapsulado en una cápsula dura y un método para preparar el mismo, del 19 de Febrero de 2020, de HANMI PHARM. CO., LTD.: Una formulación compuesta de cápsula dura, que comprende dos o más principios farmacéuticamente activos, en donde cada principio farmacéuticamente […]