Procedimiento para la preparación de carbonato de diarilo.
El procedimiento para la preparación de un carbonato de diario por transesterificación de un alcohol aromático con un carbonato de dialquilo en presencia de un catalizador de transesterificación durante un periodo de tiempo [ta],
en que el resto arilo se selecciona a partir de grupos fenilo no sustituido y fenilo mono, di y tri-sustituido, en que el resto alquilo se selecciona de grupos alquilo C2 a C4 lineales y ramificados,
en que la concentración de catalizador se designa [ca], expresado como gramo de catalizador por gramo de alcohol aromático y carbonato de dialquilo,
en que el periodo de tiempo [tm] y la concentración de catalizador [cm] se determinan para llegar a una aproximación preestablecida al equilibrio para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol,
en que el producto [ca]*ta es al menos 1,5*[cm]*tm, bajo por lo demás las mismas condiciones de reacción.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/050604.
Solicitante: SHELL INTERNATIONALE RESEARCH MAATSCHAPPIJ B.V..
Nacionalidad solicitante: Países Bajos.
Dirección: CAREL VAN BYLANDTLAAN 30 2596 HR DEN HAAG PAISES BAJOS.
Inventor/es: NISBET, TIMOTHY, MICHAEL, VAPORCIYAN,GARO,GARBIS, VAN DER HEIDE,EVERT, VROUWENVELDER,CORNELIS LEONARDO MARIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C68/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 68/00 Preparación de ésteres de los ácidos carbónico o halofórmico. › a partir de carbonatos orgánicos.
- C07C69/96 C07C […] › C07C 69/00 Esteres de ácidos carboxílicos; Esteres del ácido carbónico o del ácido halofórmico. › Esteres de los ácidos carbónico o halofórmico.
PDF original: ES-2546187_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de carbonato de diarilo
La presente invención se refiere a un procedimiento para la preparación de un carbonato de diarilo por transesterificación de un alcohol aromático con un carbonato de dialquilo en presencia de un catalizador de transesterificación.
Dicho procedimiento se conoce a partir del documento US-A 5.344.954. El documento describe un procedimiento en que el carbonato de dialquilo se convierte en dos etapas. En una primera etapa la transesterificación del carbonato de dialquilo con el alcohol aromático tiene lugar para dar carbonato de alquilarilo y el correspondiente alcohol de alquilo. El alcohol de alquilo se descarga después de la primera etapa y el carbonato de alquilarilo se manda a la segunda etapa donde tiene lugar la desproporción para dar carbonato de diarilo que se recupera por el fondo y el carbonato de dialquilo que se recupera por arriba del reactor en que se realiza la segunda etapa. En la segunda etapa también tiene lugar la transesterificación adicional del carbonato de alquilarilo con cualquier alcohol aromático que esté aún presente en la mezcla de reacción para dar carbonato de diarilo y alcohol de alquilo. El carbonato de dialquilo y el alcohol de alquilo que se recuperan en la segunda etapa se pasan a la primera etapa de manera que el carbonato de dialquilo puede hacerse reaccionar de nuevo y el alcohol de alquilo puede descargarse desde la primera etapa.
Como se describe en el documento US-A 5.344.954, se sabe que la reacción de transesterificación de carbonato de dialquilo y alcohol aromático es una reacción de equilibrio. El equilibrio de reacción limita la conversión, incluso a largos tiempos de residencia. Un desplazamiento del equilibrio puede por ejemplo, conseguirse eliminando producto de reacción. Por lo tanto las etapas se llevan a cabo como transesterificación contracorriente y destilación reactiva.
El documento US-A 5.344.954 describe una transesterificación contracorriente de carbonatos de dialquilo con alcohol aromático, en cuya transesterificación los carbonatos de dialquilo pueden ser carbonato de dimetilo y dietilo. El alcohol aromático se muestra como fenol. Los ejemplos muestran que bajo condiciones de reacción comparables la transesterificación del carbonato de dimetilo da por resultado una mayor conversión de fenol que la transesterificación de carbonato de dietilo. Por ejemplo, en los Ejemplos 2 y 8 se aplicaron condiciones de reacción similares en el mismo aparato en la transesterificación de carbonato de dimetilo y carbonato de dietilo, respectivamente. Bajo las condiciones mostradas la conversión de fenol fue significativamente mayor en el caso de carbonato de dimetilo que en el caso de carbonato de dietilo.
Los Ejemplos del documento US-A 4.554.11 también describen una transesterificación de carbonatos de dialquilo con fenol como el alcohol aromático, en cuya transesterificación los carbonatos de dialquilo son carbonato de dimetilo y carbonato de dietilo. Los Ejemplos del documento US-A 4.554.11 se tratan adicionalmente a continuación.
Es un objeto de la invención proveer al experto con herramientas para llegar a una mayor conversión del alcohol aromático cuando se usa un carbonato de dialquilo (C2-C4) en comparación a cuando se usa carbonato de dimetilo.
Sorprendentemente se ha encontrado actualmente que la conversión de carbonatos de dialquilo (C2-C4) puede aumentarse más que la conversión de carbonato de dimetilo si la concentración de catalizador y/o el tiempo de residencia se eligen de manera que el producto de dicha concentración de catalizador y dicho tiempo de residencia (indicándose dicho producto como Pa) es al menos 1,5 veces el producto de la concentración de catalizador y el tiempo de residencia para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol (indicándose dicho último producto como Pm) a una cierta aproximación preestablecida al equilibrio (o porcentaje de equilibrio) para la última reacción de transesterificación. Se tratan a continuación ventajas adicionales de la presente invención, incluyendo los Ejemplos.
Por consiguiente, la presente invención proporciona un procedimiento para la preparación de un carbonato de diarilo por transesterificación de un alcohol aromático con un carbonato de dialquilo en presencia de un catalizador de transesterificación durante un periodo de tiempo [y,
en que el resto arilo se selecciona de grupos fenilo no sustituido y fenilo mono, di y tri-sustituido, en que el resto alquilo se selecciona de grupos alquilo C2 a C4 lineales o ramificados,
en que la concentración de catalizador se designa [ca], expresada como gramo de catalizador por gramo de alcohol aromático y carbonato de dialquilo,
en que el periodo de tiempo [tm] y la concentración de catalizador [cm] se determinan para llegar a una aproximación preestablecida al equilibrio para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol,
en que el producto [ca]*ta es al menos 1,5*[cm]*tm, bajo por lo demás las mismas condiciones de reacción.
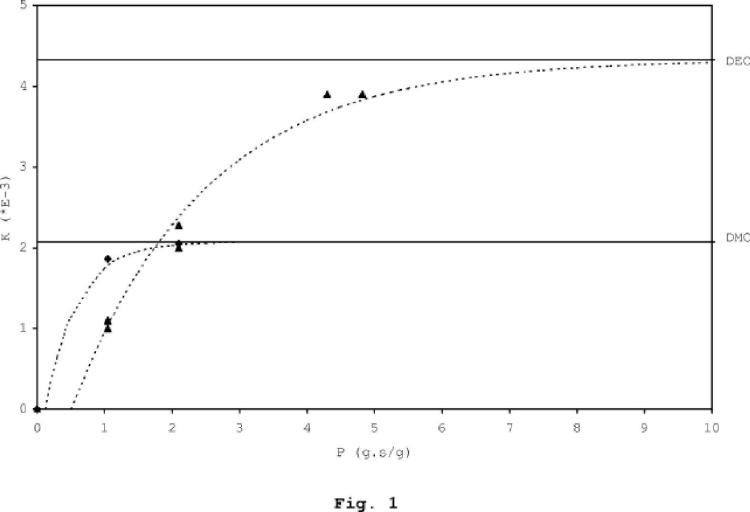
Se encontró que el producto [cm]*tm (en adelante denominado como Pm) influye en la conversión de carbonato de dimetilo, como se demuestra en los Ejemplos posteriores. Si Pm se multiplica por un cierto factor (>1) la conversión aumenta. Además la conversión de carbonatas de dialquilo (C2-C4) está influida por el producto [ca]*ta (en adelante denominado como Pa), como también se demuestra en los Ejemplos posteriores. Sorprendentemente, se encontró que cuando Pa y Pm tenían el mismo valor y Pa se multiplicaba por el mismo factor (>1), el aumento en la conversión del carbonato de dialquilo (C2-C4) es proporcionalmente mayor, más específicamente a valores P relativamente altos.
La invención provee al experto con herramientas para llegar a una mayor conversión del alcohol aromático cuando se usa un carbonato de dialquilo (C2-C4). Esto es muy sorprendente ya que la técnica anterior (por ejemplo, el documento US-A 5.344.954 mencionado anteriormente) sugiere que la conversión de alcohol aromático es significativamente menor cuando dicho carbonato de alquilo se usa en vez de carbonato de dimetilo.
De acuerdo con la invención, Pa es al menos 1,5*Pm. Además, según la invención, dicho Pm se determina para llegar a una aproximación preestablecida al equilibrio para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol.
La reacción entre un alcohol aromático y un carbonato de dialquilo tiene lugar en dos etapas. La primera etapa es la transesterificación del alcohol aromático con carbonato de dialquilo a carbonato de alquiladlo y alcanol. Esta reacción está seguida por la desproporción del carbonato de alquiladlo a carbonato de diarilo y alcanol. La primera reacción (transesterificación) tiene el equilibrio más desfavorable.
Con dicho término "aproximación preestablecida al equilibrio" se entiende el porcentaje de equilibrio para la reacción de transesterificación en cuestión, que es decir la extensión (en %) al que el equilibrio debería alcanzarse para dicha reacción. En otras palabras, dicha aproximación preestablecida al equilibrio presenta la siguiente fórmula:
Porcentaje de equilibrio (%) = (K/Keq)*1.
Para la reacción específica anterior, en donde se usa carbonato de dimetilo, dicha K tiene la siguiente definición:
K = ([carbonato de metilarilo] * [metanol]) / ([carbonato de dimetilo] * [alcohol aromático]).
Dicha K y la conversión de reactivos están relacionados. A mayor K, más productos se forman y por consiguiente mayor es la conversión. Keq es la constante de equilibrio que es K al equilibrio. A partir de la constante de equilibrio puede determinarse la conversión máxima de los reactivos.
Se sabe que la reacción del alcohol aromático, por ejemplo, fenol, con carbonato de dimetilo es una reacción de equilibrio. La constante de equilibrio se ha determinado y se ha descrito en diversas publicaciones. Por ejemplo, el documento US 5.426.27 describe la producción de carbonato de diarilo ejemplificado por la producción de carbonato de dlfenllo por la reacción de fenol con carbonato de dimetilo. Para la reacción de transesterificación de fenol con carbonato de dimetilo a carbonato de metilfenilo y metanol esta memoria describe como un valor típico de la constante de equilibrio un resultado de 2,6*1'3. Para la reacción de desproporción se describe un valor típico de 2,35*1'1. El artículo científico en Ind. Eng. Chem. Res., 24, 43, 1897-1914 por W B Kim et al., describe que la constante de equilibrio para esta reacción de transesterificación... [Seguir leyendo]
Reivindicaciones:
1. El procedimiento para la preparación de un carbonato de diario portransesterificación de un alcohol aromático con un carbonato de dialquilo en presencia de un catalizador de transesterificación durante un periodo de tiempo [ta],
en que el resto arilo se selecciona a partir de grupos fenilo no sustituido y fenilo mono, di y tri-sustituido, en que el resto alquilo se selecciona de grupos alquilo C2 a 64 lineales y ramificados,
en que la concentración de catalizador se designa [ca], expresado como gramo de catalizador por gramo de alcohol aromático y carbonato de dialquilo,
en que el periodo de tiempo [tm] y la concentración de catalizador [cm] se determinan para llegar a una aproximación preestablecida al equilibrio para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol,
en que el producto [ca]*ta es al menos 1,5*[cm]*tm, bajo por lo demás las mismas condiciones de reacción.
2. El procedimiento según la reivindicación 1, en que la aproximación preestablecida al equilibrio para la transesterificación del alcohol aromático con carbonato de dimetilo a carbonato de metilarilo y metanol oscila de 7 a 1%.
3. El procedimiento según la reivindicación 1 o 2, en que [ca]*ta es el producto de [cm]*tm con un factor tal que la reacción se hace marchar a al menos el 5 por ciento del equilibrio.
4. El procedimiento según cualquiera de las reivindicaciones 1 a 3, en el que la concentración de catalizador ca oscila de ,1 a 2% en peso, en base al peso total de los reactivos.
5. El procedimiento según cualquiera de las reivindicaciones 1 a 4, en el que el periodo de tiempo ta oscila de 2 minutos (12 s) a 5 horas (18*13 s).
6. El procedimiento según cualquiera de las reivindicaciones 1 a 5, en el que el producto [ca]*ta oscila de ,1 a 1, preferiblemente de ,5 a 5, expresándose ca en g/g y ta en segundos.
7. El procedimiento según cualquiera de las reivindicaciones 1 a 6, que se lleva a cabo como un proceso continuo.
8. El procedimiento según cualquiera de las reivindicaciones 1 a 7, que se lleva a cabo en un modo de destilación reactiva.
9. El procedimiento según cualquiera de las reivindicaciones 1 a 8, en que el alcohol aromático es fenol.
1. El procedimiento según cualquiera de las reivindicaciones 1 a 9, en que el resto alquilo C2 a C4 se selecciona del grupo que consiste en etilo e isopropilo.
11. El procedimiento según cualquiera de las reivindicaciones 1 a 1, en el que las condiciones de reacción incluyen una presión que oscila de ,1 a 1 bar (1 kPa a 1 MPa), preferiblemente de 1 a 5 bar, y una temperatura de reacción que oscila de 5 a 35°C, preferiblemente de 12 a 28°C.
12. El procedimiento según cualquiera de las reivindicaciones 1 a 11, en que el producto [ca]*ta es 1,5 a 5 veces [Cm]*tm, y por lo demás bajo las mismas condiciones de reacción.
13. El procedimiento según la reivindicación 12, en que el producto [ca]*ta es al menos 3*[Cm]*tm cuando el carbonato de dialquilo es carbonato de dietilo.
14. El procedimiento según la reivindicación 12, en que el producto [ca]*ta es preferiblemente al menos 2*[cm]*tm cuando el carbonato de dialquilo es carbonato de diisopropilo.
Patentes similares o relacionadas:
Carbonatos de dialquilo, procedimientos para su producción y uso, del 29 de Julio de 2020, de HUNTSMAN PETROCHEMICAL LLC: Un carbonato de dialquilo de un alcohol C16-C17 primario ramificado con monometilo que tiene la siguiente estructura: **(Ver fórmula)** en la que la ramificación en […]
Procedimiento de síntesis de ésteres carbónicos lineales de glicerol alfa/alfa prima alcoxilados, del 17 de Junio de 2020, de CHRYSO: Procedimiento de síntesis de ésteres carbónicos lineales de glicerol α/α'-alcoxilados en el que se ponen en contacto: i. una cantidad de […]
Proceso para preparar un carbonato de diarilo, del 2 de Octubre de 2019, de SHELL INTERNATIONALE RESEARCH MAATSCHAPPIJ B.V.: Un proceso para preparar un carbonato de diarilo a partir de un carbonato de dialquilo y un alcohol arílico que comprende: una primera etapa en donde el […]
Procedimiento de preparación de 3-cloro-2-vinilfenilsulfonatos, del 27 de Marzo de 2019, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Procedimiento de preparación de derivados de 3-cloro-2-vinilfenilsulfonato de la fórmula (I),**Fórmula** en la cual R1 representa alquilo C1-C6, fenilo, 4-metilfenilo […]
Procedimiento para la preparación de carbonato de diarilo, del 27 de Febrero de 2019, de Covestro Deutschland AG: Procedimiento para la preparación de carbonato de diarilo mediante reacción de al menos un monofenol con fosgeno y/o al menos un éster arílico […]
Intermedio para la síntesis de 1-(2-desoxi-2-fluoro-4-tio-beta-d-arabinofuranosil)citosina, intermedio para la síntesis de tionucleósido y métodos para producir estos intermedios, del 27 de Febrero de 2019, de FUJIFILM CORPORATION: Un metodo para producir un compuesto representado por la formula [1E] siguiente:**Fórmula** en donde R1A, R1B, R2A, R2B, R3A y R3B tienen los mismos significados […]
Derivados de tetrahidro-isohumulona, métodos para su preparación y uso, del 13 de Febrero de 2019, de Kindex Pharmaceuticals, Inc: Un compuesto de fórmula V o VI:**Fórmula** en donde R1 se selecciona entre isopropilo, isobutilo y sec-butilo; R2, se selecciona entre cualquier […]
Un procedimiento para producir carbonatos aromáticos, del 30 de Mayo de 2018, de SHELL INTERNATIONALE RESEARCH MAATSCHAPPIJ B.V.: Un método para producir un carbonato de alquilarilo que comprende: a) poner en contacto una corriente que comprende un hidroxicompuesto aromático y agua […]