Diagnóstico de la EPOC.
Procedimiento para el diagnóstico de la enfermedad pulmonar obstructiva crónica (EPOC) en un sujeto humano que comprende las etapas de:
- determinar la cantidad de proteína de choque térmico 27 (HSP27) en una muestra de sangre, suero o plasma de un sujeto humano,
- diagnosticar la EPOC cuando la cantidad de HSP27 está aumentada en comparación con la cantidad de HSP27 en sujetos humanos sanos.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11159730.
Solicitante: Aposcience AG.
Nacionalidad solicitante: Austria.
Dirección: Rauhensteingasse 4/3 1010 Wien AUSTRIA.
Inventor/es: ANKERSMIT, JAN, HENDRIK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/68 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen proteínas, péptidos o aminoácidos.
PDF original: ES-2510390_T3.pdf




Fragmento de la descripción:
Diagnóstico de la EPOC
La presente invención se refiere a procedimientos para el diagnóstico de la EPOC en un sujeto humano.
La enfermedad pulmonar obstructiva crónica (EPOC) es una de las principales causas de muerte a nivel mundial. En 2020, sólo la cardiopatía isquémica y las enfermedades cerebrovasculares serán responsables de una mortalidad más elevada entre la población mundial. Las tasas de prevalencia y hospitalización han crecido drásticamente durante los últimos años. Varios estudios han mostrado una fuerte correlación entre el tabaquismo y el desarrollo de la EPOC aunque no todos los fumadores desarrollan las características clínicas de la EPOC (Higenbottam T y col. (1980) Lancet 315:409-411) . La patogénesis se caracteriza por obstrucción del flujo respiratorio debido a la remodelación de las vías respiratorias y una inflamación aberrante. La EPOC abarca bronquitis crónica y enfisema, ambas afecciones caracterizadas por destrucción del tejido. La limitación del flujo respiratorio progresa lentamente, 15 lo que lleva a disnea y a limitaciones de la capacidad para realizar ejercicio físico. Sin embargo, la deficiencia no se limita a los pulmones ya que los pacientes con la EPOC también presentan un riesgo mayor de insuficiencias sistémicas que incluyen enfermedades cardiovasculares. El diagnóstico de la obstrucción de las vías respiratorias según las directrices de la Iniciativa Global para las enfermedades pulmonares obstructivas crónicas (GOLD, por sus siglas en inglés) requiere del uso de espirometría. Una relación VEF1/CVF (volumen espiratorio forzado en un seguro/capacidad vital forzada) postbroncodilatador menor del 70% indica una obstrucción de las vías respiratorias irreversible y, por tanto, se considera que es el principal parámetro para el diagnóstico de la EPOC (Global Strategy for Diagnosis, Management, and Prevention of COPD. Global Initiative FOR Chronic Obstructive Lung Disease, 2007, www.goldcopd.com) . Actualmente, los pacientes se clasifican dentro de los estadios GOLD según los datos de espirometría y la presentación clínica. La detección de los marcadores séricos que indican la actividad de la enfermedad es de interés especial en el proceso diagnóstico y terapéutico.
Aunque está ampliamente aceptado que el tabaquismo es el principal factor de riesgo para el desarrollo de la EPOC, las descripciones de la ruta patogénica específica y los mecanismos implicados siguen siendo vagas. El estrés oxidativo en el parénquima pulmonar parece estar implicado en el inicio de la respuesta inflamatoria a la exposición al humo del tabaco. Los neutrófilos y macrófagos, como parte de la inmunidad innata, se consideraron fundamentales en el proceso de remodelación de las vías respiratorias en la EPOC. Este proceso de remodelación es consecuencia de la inducción de apoptosis crónica en los pulmones de los pacientes con la EPOC o en fumadores. El término apoptosis hace referencia a la alteración morfológica mostrada por células que mueren "de forma activa" lo que incluye disminución del volumen celular, formación de ampollas en la membrana, condensación de la cromatina y fragmentación del ADN. La apoptosis afecta a las células epiteliales alveolares y bronquiales así como a las células endoteliales del parénquima. La apoptosis controlada es un proceso deseado y crítico para la hemostasis celular. Sin embargo, un desencadenamiento excesivo de apoptosis y un aumento del recambio de las células alveolares puede llevar a la destrucción del tejido.
Las observaciones de inmunohistoquímica en tejido pulmonar derivo de pacientes con la EPOC mostraron infiltrados inflamatorios compuestos por linfocitos T y macrófagos, con cantidades variables de mastocitos, neutrófilos y eosinófilos. Los avances en las reacciones inmunes han mostrado que un desequilibrio entre linfocitos T colaboradores de tipo 1 (TH1) y linfocitos T colaboradores de tipo 2 (TH2) tiene una función en la respuesta inflamatoria de diversas enfermedades. Los estudios han mostrado un patrón predominante de citoquinas TH1 en la 45 inflamación intersticial infiltrante en la EPOC. El epitelio de las vías respiratorias es un componente crítico de la reacción inmune, produciendo citoquinas proinflamatorias como el factor de necrosis tumoral alfa (TNFα) , interleuquina-1-beta (IL-1β) y quimioquinas. Las células epiteliales del pulmón también modulan las exacerbaciones agudas y las reacciones a patógenos que son frecuentes en pacientes que padecen la EPOC.
El único procedimiento utilizado en la práctica clínica para el diagnóstico de la EPOC es la espirometría, que es una prueba de la función pulmonar en la que se mide dicha función pulmonar, específicamente, la medición de la cantidad (volumen) y/o velocidad (flujo) de aire que puede inhalarse y exhalarse. Sin embargo, estas pruebas también se usan para diagnosticar otras enfermedades pulmonares como el asma y la fibrosis pulmonar. Por tanto, este procedimiento no puede funcionar como la única prueba para un diagnóstico fiable de la EPOC. En 55 consecuencia, los médicos consideran también síntomas como disnea, tos crónica y producción de esputo y/o antecedentes de exposición a factores de riesgo en el diagnóstico de la EPOC. Es evidente que el uso de estos procedimientos en el diagnóstico de la EPOC o en la discriminación entre diversas formas de la EPOC puede dar lugar a un falso diagnóstico, por lo que el paciente no pueda utilizar la mejor forma de tratamiento justo desde el inicio de la enfermedad.
Por tanto, es un objeto de la presente invención proporcionar procedimientos y medidas que permitan un diagnóstico inequívoco de la EPOC en un sujeto humano desde el inicio de la enfermedad o incluso determinar el riesgo de que un sujeto humano desarrolle la EPOC.
La presente invención se refiere a un procedimiento para diagnosticar la enfermedad pulmonar obstructiva crónica (EPOC) en un sujeto humano que comprende las etapas de:
- determinar la cantidad de proteína de choque térmico 27 (HSP27) en una muestra de sangre, suero o plasma de un sujeto humano, -diagnosticar la EPOC cuando la cantidad de HSP27 esté aumentada en comparación con la cantidad de HSP27 en sujetos humanos sanos.
Según una realización preferida de la presente invención adicionalmente la concentración de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas (histonas) , HSP70 y/o HSP90 alfa está aumentada en comparación con la cantidad de receptores 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP70 y/o HSP90 alfa en humanos sanos.
Se vio que la concentración de HSP27, opcionalmente en combinación con ccCK-18, histonas, HSP70 y/o HSP90 alfa en una muestra de un humano puede funcionar como marcador que permita diagnosticar la EPOC, en particular, los estadios I/II y III/IV de la EPOC en dicho sujeto humano. Los marcadores incluso permiten determinar el riesgo de que un sujeto humano desarrolle la EPOC en el futuro. No todos los humanos que se considera están en riesgo de desarrollar la EPOC debido a su estilo de vida (por ejemplo, humanos expuestos a humos, fumadores, etc.) enfermarán de la EPOC. Por tanto, el diagnóstico de que un sujeto humano está en riesgo de desarrollar la EPOC es muy útil para la prevención de la EPOC.
Los marcadores utilizados en el procedimiento de la presente descripción pueden usarse por separado o en combinación, por lo que adicionalmente puede determinarse la concentración de receptor 4 de la interleuquina-1, en el que se diagnostica la EPOC cuando la concentración de receptor 4 de la interleuquina-1 está aumentada en comparación con la cantidad de receptor 4 de la interleuquina-1 en sujetos humanos sanos o en el que el riesgo de desarrollar la EPOC se diagnostica cuando la cantidad de receptor 4 de la interleuquina-1 está reducida en comparación con la cantidad de receptor 4 de la interleuquina 1 en humanos sanos. Entre las combinaciones preferidas se incluyen el receptor 4 de la interleuquina-1 y ccCK-18, receptor 4 de la interleuquina-1 e histonas, ccCK-18 e histonas, receptor 4 de la interleuquina-1, HSP27, HSP70 y/o HSP90 alfa.
Para clasificar la gravedad de la EPOC se utilizan los parámetros espirométricos. Estos parámetros permiten clasificar la gravedad de la EPOC en cuatro estadios (véase la tabla A) . La espirometría es esencial para el diagnóstico y proporciona una descripción útil de la gravedad de los cambios patológicos de la EPOC. Los puntos de corte espirométricos específicos (por ejemplo, relación VEF1/CVF postbroncodilatador < 0, 70 o VEF1 <80, 50 o 30% del previsto) se usan para determinar los estadios I a IV de la EPOC.
Tabla A: clasificación espirométrica de la EPOC (según www.goldcopd.com)... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para el diagnóstico de la enfermedad pulmonar obstructiva crónica (EPOC) en un sujeto humano que comprende las etapas de:
- determinar la cantidad de proteína de choque térmico 27 (HSP27) en una muestra de sangre, suero o plasma de un sujeto humano, -diagnosticar la EPOC cuando la cantidad de HSP27 está aumentada en comparación con la cantidad de HSP27 en sujetos humanos sanos.
2. Procedimiento según la reivindicación 1, caracterizado por que además se determina la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, proteína de choque térmico 70 (HSP70) y/o proteína de choque térmico 90 alfa (HSP90 alfa) , en el que se diagnostica la EPOC cuando la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP70 y/o HSP90 alfa está aumentada en comparación con la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP70 y/o HSP90 alfa en sujetos humanos sanos.
3. Procedimiento según la reivindicación 1 o 2, caracterizado por que la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, proteína de choque térmico 27 (HSP27) , proteína de choque térmico 70 (HSP70) y/o proteína de choque térmico 90 alfa (HSP90 alfa) se determina mediante un inmunoensayo seleccionado a partir de grupo que consiste de ensayo de inmunoabsorción ligado a enzima (ELISA) , radioinmunoensayo (RIA) e inmunotransferencia.
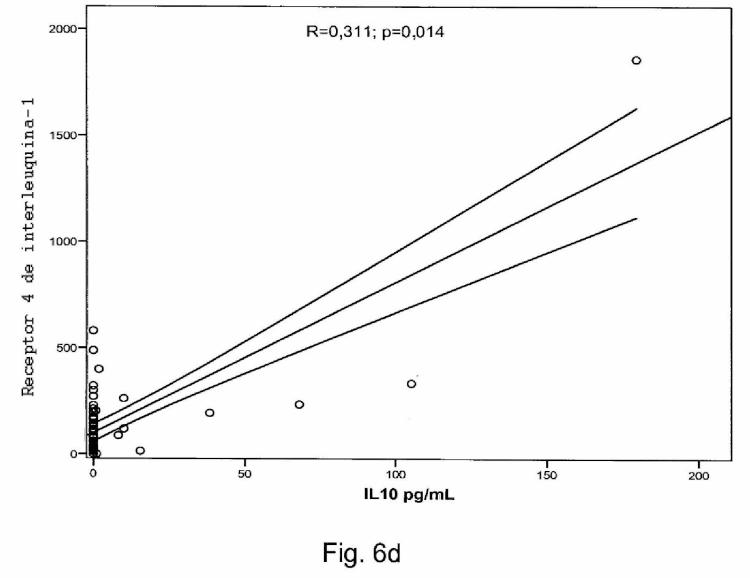
4. Procedimiento según la reivindicación 2 o 3, caracterizado por que la cantidad de receptor 4 de la interleuquina-1 en muestras de sangre de un sujeto humano sano oscila preferiblemente entre 50 y 150 pg/ml, preferiblemente entre 60 y 140 pg/ml, más preferiblemente entre 70 y 130 pg/ml.
5. Procedimiento según la reivindicación 2 o 3, caracterizado por que la cantidad de fragmento de ADN asociado a histonas en muestras de sangre de un sujeto humano sano es del 20 al 50% menor, preferiblemente del 25 al 40% menor, que en muestras de sangre de un sujeto humano que padece la EPOC.
6. Procedimiento según una cualquiera de las reivindicaciones 1 a 5, caracterizado por que la cantidad de proteína
de choque térmico 27 (HSP27) en muestras de sangre de un sujeto humano sano oscila entre 1500 y 2000 pg/ml, 35 preferiblemente entre 1600 y 2400 pg/ml, más preferiblemente entre 1700 y 2300 pg/ml.
7. Procedimiento según la reivindicación 2 o 3, caracterizado por que la cantidad de proteína de choque térmico 70 (HSP70) , en muestras de sangre de un sujeto humano sano oscila entre 50 y 200 pg/ml, preferiblemente entre 70 y 190 pg/ml, más preferiblemente entre 80 y 180 pg/ml.
8. Procedimiento según la reivindicación 2 o 3, caracterizado por que la concentración de proteína de choque térmico 90 alfa (HSP90 alfa) , en una muestra de sangre de un sujeto humano sano oscila entre 10 000 y 15 000 pg/ml, preferiblemente entre 11 000 y 14 500 pg/ml, más preferiblemente entre 12 000 y 14 000 pg/ml.
9. Procedimiento según una cualquiera de las reivindicaciones 1 a 8, caracterizado por que se diagnostica la EPOC cuando la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP27, HSP70 y/o HSP90 alfa en la muestra está al menos el 10%, preferiblemente al menos el 20%, aumentada en comparación con la cantidad de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP27, HSP70 y/o HSP90 alfa en sujetos humanos sanos.
10. Procedimiento según una cualquiera de las reivindicaciones 1 a 8, caracterizado por que se diagnostica el riesgo de desarrollar la EPOC cuando la concentración de receptor 4 de la interleuquina-1, fragmento de ADN asociado a histonas, HSP27, HSP70 y/o HSP90 alfa en la muestra está al menos el 10%, preferiblemente al menos el 20%, reducida en comparación con la concentración de receptor 4 de la interleuquina-1, fragmento de ADN asociado a 55 histonas, HSP27, HSP70 y/o HSP90 alfa en sujetos humanos sanos.
11. Procedimiento para discriminar entre la EPOC en estadios I/II y la EPOC en estadios III/IV en un sujeto humano que comprende las etapas de:
- determinar la cantidad de proteína de choque término 27 (HSP27) en una muestra de sangre, suero o plasma de un sujeto humano que padece la EPOC, -diagnosticar la EPOC en estadios I/II cuando la cantidad de HSP27 está reducida en comparación con la cantidad de HPS27 determinada en una muestra de un sujeto humano que padece la EPOC en estadios III/IV, o 65 -diagnosticar la EPOC en estadios III/IV cuando la cantidad de HSP27 está aumentada en comparación con la
cantidad de HPS27 determinada en una muestra de un sujeto humano que padece la EPOC en estadios I/II.
12. Procedimiento según la reivindicación 11, caracterizado por que además se determina la cantidad de receptor 4
de la interleuquina-1, citoqueratina-18 escindida por caspasas (ccCK-18) , histonas y/o proteína de choque térmico 5 70 (HSP70) , en el que se diagnostica la EPOC en estadios I/II cuando la cantidad de receptor 4 de la interleuquina-1
o HSP70 está aumentada en comparación con la cantidad de receptor 4 de la interleuquina-1 o HSP70 determinada en una muestra de un sujeto humano que padece la EPOC en estadios III/IV y/o cuando la cantidad de ccCK-18 o fragmento de ADN asociado a histonas está reducida en comparación con la cantidad de ccCK-18 o fragmento de ADN asociado a histonas determinado en una muestra de un sujeto humano que padece la EPOC en estadios III/IV, o en el que se diagnostica la EPOC en estadios III/IV cuando la cantidad de receptor 4 de la interleuquina-1 o HSP70 está reducida en comparación con la concentración de receptor 4 de la interleuquina-1 o HSP70 determinada en una muestra de un sujeto humano que padece la EPOC en estadios I/II y/o cuando la cantidad de ccCK-18 o histonas está aumentada en comparación con la concentración de ccCK-18 o fragmento de ADN asociado a histonas determinado en una muestra de un sujeto humano que padece la EPOC en estadios I/II.
Patentes similares o relacionadas:
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Inmunomoduladores, del 29 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la fórmula (I) **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de **(Ver fórmula)** en donde: […]
Métodos y composiciones para el diagnóstico y pronóstico de lesión renal e insuficiencia renal, del 29 de Julio de 2020, de Astute Medical, Inc: Un método para evaluar el estado renal en un sujeto, que comprende: realizar una pluralidad de ensayos configurados para detectar una […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Método para llevar a cabo el seguimiento de la enfermedad de Gaucher, del 15 de Julio de 2020, de Centogene GmbH: Un método para determinar la evolución de la enfermedad de Gaucher en un sujeto, que comprende la etapa de determinar en varios puntos en el […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
Biomarcadores de pronóstico y predictivos y aplicaciones biológicas de los mismos, del 1 de Julio de 2020, de INSTITUT GUSTAVE ROUSSY: Un método para evaluar la sensibilidad o la resistencia de un tumor frente a un agente antitumoral, que comprende evaluar la cantidad de complejo eiF4E-eiF4G (complejo Cap-ON) […]
Evaluación asistida del pronóstico en la enfermedad inflamatoria, del 24 de Junio de 2020, de KINGS COLLEGE LONDON: Un método in vitro de recopilación de información útil para predecir el resultado clínico en un sujeto, en donde el sujeto tiene o se sospecha que tiene una enfermedad […]