Vectores adenovirales que expresan la interleucina-12 de cadena sencilla y el ligando 4-1BB.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2003/011252.
Solicitante: PROVECS MEDICAL GMBH.
Inventor/es: WÄHLER,REINHARD, SCHNIEDERS,FRANK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/54 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Interleuquinas (IL).
- C07K14/55 C07K 14/00 […] › IL-2.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C12N15/861 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores adenovirales.
PDF original: ES-2440951_T3.pdf
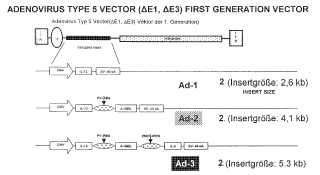
Fragmento de la descripción:
Vectores adenovirales que expresan la interleucina-12 de cadena sencilla y el ligando 4-1BB.
La presente invención se refiere a vectores adenovirales, que comprenden secuencias de acido nucleico que codifican para interleucina (lL) -12 de cadena sencilla (lL-12 de cadena sencilla, "single chain IL-12" o sclL-12) y la proteina coestimuladora 4-1BB, asi como la utilización de estos vectores para la terapia genica, en particular para el tratamiento de tumores. Las enfermedades cancerosas siguen representando una de las causas de muerte mas frecuentes de los seres humanos en los paises industrializados. El carcinoma hepatocelular (HCC) es, por ejemplo, una enfermedad cancerosa con un tiempo de supervivencia medio de 6 meses en caso del diagnóstico de uno o varios tumores grandes (Llovet J.M. et al., Hepatology, 1999, 29:62-67) . Si bien los enfoques terapeuticos utilizados en la actualidad, que comprenden ablación por radiofrecuencia, quimioterapia e inyección percutanea de etanol (PEl) ,
presentan un cierto exito en el caso de tumores pequenos, sin embargo demuestran ser insuficientes en la lucha contra tumores grandes. Por tanto, en el estado de la tecnica se propuso tratar HCC mediante terapia genica. Los procedimientos de tratamiento con terapia genica se basan en la administración de un acido nucleico, que normalmente se absorbe en la celula tumoral y que presenta secuencias que destruyen la celula tumoral. A este respecto se desarrollaron un gran numero de estrategias alternativas, por medio de las cuales las secuencias de acido nucleico transferidas pueden provocar una destrucción de las celulas tumorales. Un resumen de las estrategias correspondientes para el tratamiento del HCC se encuentra en Ruiz et al. (Dig.Dis. 2001, 19: 324-332) . En esta publicación se clasifican los acidos nucleicos que se estudian hoy en dia en ensayos clinicos para un tratamiento del HCC en el ser humano segun la estrategia de tratamiento en uno de los 4 grupos siguientes:
(1) Transferencia de supresores tumorales:
Esta estrategia se basa en que el acido nucleico utilizado para la terapia genica contiene un gen, cuyo producto genico inhibe el crecimiento del tumor o induce apoptosis en las celulas tumorales. La mayoria de los ensayos clinicos se basan en una transferencia del gen p53.
(2) lnmunoterapia genica:
Esta estrategia se basa en que el acido nucleico utilizado para la terapia genica comprende secuencias, cuyos productos genicos activan el sistema inmunitario del paciente y desencadenan una reacción inmunitaria dirigida contra las celulas tumorales. La propia reacción inmunitaria conduce entonces a la destrucción del tumor. Se han propuesto numerosas citocinas, moleculas coestimuladoras y moleculas especificas de tumor para una inmunoterapia genica. Lieschke et al. expresan interleucina-12 en celulas tumorales CMS-5.
(3) Terapia genica suicida:
En este modo de proceder el acido nucleico utilizado para la terapia genica codifica para un producto genico, por ejemplo para una enzima, que transforma una sustancia activa no t6xica en un agente citot6xico para la celula tumoral.
(4) Transferencia de virus oncoliticos:
Para esta forma de terapia genica se utilizan vectores de acido nucleico basados en secuencias virales. Los vectores con secuencias virales oncoliticas presentan un promotor especifico de tumor, que controla la replicación del virus, de modo que se posibilita un crecimiento selectivo de los virus en las celulas tumorales.
Por tanto, en la inmunoterapia genica relevante para la presente solicitud (tambien denominada inmunoterapia) se administran acidos nucleicos que comprenden secuencias que activan el sistema inmunitario y lo dirigen al tumor. Basicamente, el sistema inmunitario reconoce ademas de antigenos tambien estructuras especificas de tumor en celulas tumorales. Por tanto, la activación del sistema inmunitario puede conducir a una destrucción del tumor mediante los componentes del sistema inmunitario. El documento WO 00/41508 describe una terapia de combinación de cancer mediante activación de moleculas coestimuladoras de las celulas inmunitarias, por medio de dos vectores adenovirales que codifican o bien para las dos subunidades diferentes de lL-12 o bien para ligando 4-1BB.
En el estado de la tecnica se conocen numerosas moleculas que estimulan el sistema inmunitario o modulan una reacción inmunitaria, en particular las citocinas. Ya hace tiempo se estableci6 que las citocinas tambien presentan actividades antitumorales. Por ejemplo se inform6 que lL-12 es un estimulador de la inmunidad celular y presenta una fuerte actividad antitumoral (Brunda et al, J. Exp. Med. 1993, 178:1223-1230) . Sin embargo, la administración de la propia proteina lL-12 recombinante como agente antitumoral fracas6 porque la citocina presenta efectos secundarios t6xicos en la dosificación terapeutica (Lotze et al., Ann.N.Y.Acad.Sci., 1997, 795:440-454; y Cohen J. Science, 1995, 270:908) .
Por tanto, se propuso introducir en el tumor un acido nucleico que codifica para una citocina y con ello posibilitar una activación local del sistema inmunitario. Hock et al. (Proc. Natl. Acad.Sci. USA, 1993, 90: 2774-2778) describen, por ejemplo, latransferenciadelgen de interleucina-2 (lL-2) , interleucina-4 (lL-4) , interleucina-7 (lL-7) , TNF olFN-γ en lineas de celulas tumorales y la utilización de las lineas de celulas tumorales para la inducción de tumores en animales. Todas las lineas de celulas tumorales transgenicas generan una reacción de rechazo contra las celulas tumorales, estando implicadas, en función de la citocina utilizada, diferentes celulas del sistema inmunitario de los animales de ensayo en la reacción de rechazo (CD4+, CD8+, CD3+) .
Tambien se estudiaron vectores que codifican para lL-12, para determinar su idoneidad para la inmunoterapia. La lL-12, que tambien se denomina CMLF ("cytotoxic lymphocyte maturation factor", factor de maduración de linfocitos citot6xicos) o NKSF ("natural killer cell stimulator y factor", factor estimulador de celulas citoliticas naturales) , es una citocina heterodimerica que se forma de manera natural por linfocitos B perifericos tras su activación. La proteina consta de dos subunidades con pesos moleculares relativos de 40 y 35 kDa, que estan unidas entre si a traves de puentes disulfuro. Los puentes disulfuro son esenciales para la actividad biológica. Tal como ya se indica mediante los diferentes nombres, la proteina estimula la proliferación de linfoblastos humanos activados y activa las celulas citoliticas naturales.
En Putzer et al. se expresaron interleucina-12 y B7-1 mediante un vector adenoviral en celulas tumorales. En Carrol et al. se utilizaron virus vaccinia para la expresión de B7-1 e interleucina-12.
Vectores que codifican para las diferentes subunidades de esta proteina, se utilizaron para el tratamiento de tumores (Barajas et al., Hepatology, 2001, 33: 52-61; Mazzolini et al., Cancer Gene Therapy, 1999, 6: 514-522) . Ademas, estos vectores se utilizaron en combinación con otras secuencias para la terapia inmunitaria, en particular en combinación con secuencias para una proteina coestimuladora, que se encontraban en el mismo o en otro vector, para el tratamiento de tumores (Gyorffy et al., J.lmmunology, 2001, 166: 6212-6217; Martinet et al., Gene Therapy, 2002, 9: 786-792; Martinet et al., Journal of National Cancer lnstitute, 2000, 92: 931-936; Guinn et al., J. lmmunology, 1999, 162: 5003-5010; y Emtage et al., J. lmmunology, 1998, 160: 2531-2538) .
Anderson et al. usaron virus adenoasociados que expresan en las celulas una proteina de fusión de interleucina-12 especifica.
La lL-12 se ha expresado ademas ya como lL-12 de cadena sencilla con buena actividad, es decir como proteina en la que se unieron las diferentes subunidades para dar una proteina de fusión (Lieschke et al., Nature Biotechnology, 1997, 15: 35-40) . En un procedimiento terapeutico adicional se propuso extraer del paciente celulas tumorales y tratarlas in vitro con un plasmido, que codifica para lL-12 de cadena sencilla o lL-12 y un coestimulador (documento US2002/0018767) . Tras este tratamiento in vitro las celulas tumorales deben reimplantarse. Por consiguiente, el procedimiento comprende varias intervenciones en el paciente y una reimplantación de celulas tumorales en los pacientes, lo que podria hacer que muchos pacientes se negaran a un tratamiento correspondiente.
Ninguno de los acidos nucleicos utilizados hasta el momento ha podido imponerse para el tratamiento de mamiferos, preferentemente para el tratamiento del ser humano. Aunque, por ejemplo, los procedimientos de tratamiento descritos en la publicación de Ruiz et al. (citada anteriormente) parten de una dosificación muy alta del vector... [Seguir leyendo]
Reivindicaciones:
1. Vector adenoviral, que comprende secuencias de acido nucleico que codifican para interleucina (lL) -12 de cadena sencilla y la proteina coestimuladora ligando 4-1BB.
2. Vector segun la reivindicación 1, caracterizado porque la expresión de la secuencia que codifica para la proteina coestimuladora ligando 4-1BB en una celula humana provoca que la proteina coestimuladora ligando 4-1BB se encuentre en la superficie de la celula y que puedan unirse especificamente a la misma receptores existentes en la superficie de celulas T.
3. Vector segun la reivindicación 1 6 2, caracterizado porque la proteina coestimuladora ligando 4-1BB presenta una homologia de secuencia de por lo menos el 70%, por lo menos el 80% o por lo menos el 90% con la SEC lD NO. 4, y presenta la capacidad de unirse especificamente a celulas T y de potenciar la reacción inmunitaria.
4. Vector segun una de las reivindicaciones 1 a 3, caracterizado porque la lL-12 de cadena sencilla presenta una homologia de secuencia de por lo menos el 70%, por lo menos el 80% o por lo menos el 90% con la SEC lD NO. 2 y SEC lD NO. 3, y presenta una actividad inmunoestimulante.
5. Vector segun una de las reivindicaciones 1 a 4, caracterizado porque el acido nucleico comprende ademas unas secuencias, que codifican para citocinas, para proteinas con actividad citocina y/o para proteinas coestimuladoras.
6. Vector segun una de las reivindicaciones 1 a 5, caracterizado porque el acido nucleico comprende ademas una secuencia que codifica para lL-2, presentando esta secuencia una homologia de secuencia de por lo menos el 70%, por lo menos el 80% o por lo menos el 90% con la SEC lD NO. 5, y presentando la proteina codificada por la secuencia una actividad inmunoestimulante.
7. Vector segun una de las reivindicaciones 1 a 6, caracterizado porque el acido nucleico comprende ademas unas secuencias, que codifican para una o varias proteinas coestimuladoras, presentando esta secuencia una homologia de secuencia de por lo menos el 70%, por lo menos el 80% o por lo menos el 90% con la SEC lD NO. 6 (B7-1) o SEC lD NO. 7 (B7-2) , y presentando la proteina codificada por la secuencia la capacidad de unirse especificamente a celulas T y de potenciar la reacción inmunitaria.
8. Vector segun una de las reivindicaciones 1 a 7, caracterizado porque el acido nucleico comprende unas secuencias, que presentan una homologia de secuencia de por lo menos el 90% con la secuencia mostrada en la SEC lD NO. 2 y 3 (lL-12) , en la SEC lD NO. 4 (ligando 4-1BB) , en la SEC lD NO. 5 (lL-2) y una de las mostradas en la SEC lD NO. 6 (B7-1) o 7 (B7-2) y codifican, respectivamente, para una proteina, que presenta la actividad de la proteina natural correspondiente.
9. Vector segun una de las reivindicaciones 1 a 8, caracterizado porque el acido nucleico comprende ademas uno o varios promotores y uno o varios sitios de entrada de ribosoma.
10.Vector segun una de las reivindicaciones 1 a 9, caracterizado porque en el caso del vector adenoviral se trata de un vector adenoviral de primera o segunda generación (deleción en E1, E2, E3, E4, etc.) o de un vector adenoviral dependiente de un auxiliar.
11.Vector segun la reivindicación 6, caracterizado porque el vector contiene secuencias de acido nucleico que presentan una homologia de secuencia de por lo menos el 90% con la SEC lD NO. 2 y 3, SEC lD NO. 4, SEC. lD NO. 5 y dado el caso SEC lD NO. 6 o 7 y codifican, respectivamente, para una proteina que presenta la actividad de la proteina natural correspondiente.
12.Vector segun la reivindicación 11, caracterizado ademas porque comprende las siguientes caracteristicas:
(a) el vector presenta un promotor no especifico de tumor, que provoca la expresión de todas las secuencias genicas que codifican para proteinas inmunoestimuladoras; y
(b) el vector presenta antes de cada secuencia genica, que no se encuentra directamente detras del promotor mencionado en (a) , una secuencia lRES.
13.Particula viral, caracterizada porque la particula viral comprende vectores segun una de las reivindicaciones 1 a 12.
14.Farmaco, caracterizado porque comprende vectores segun una de las reivindicaciones 1 a 12 o particulas virales segun la reivindicación 13.
15.Farmaco segun la reivindicación 14, caracterizado porque el vector se encuentra en una concentración de no mas de 1 x 1011, preferentemente no mas de 1 x 1010, no mas de 1 x 109, 1 x 107 o 1 x 106, por unidad de dosificación.
16.Farmaco segun la reivindicación 14 o 15, caracterizado porque el farmaco esta formulado como disolución para inyección intratumoral o como material de soporte, que libera el vector tras la implantación en el tumor a lo largo de 5 un determinado periodo de tiempo.
17.Farmaco, caracterizado porque comprende vectores segun una de las reivindicaciones 1 a 12 o particulas virales segun la reivindicación 13, para el tratamiento de enfermedades infecciosas o enfermedades por priones.
18.Farmaco segun la reivindicación 17 para el tratamiento segun la reivindicación 17, caracterizado porque la infección esta provocada por el virus de la inmunodeficiencia humana (VlH) , por el virus de la hepatitis tipo A, B o C (VHA, VHB, VHC) , por el citomegalovirus (CMV) o por virus de papiloma humano VPH.
Patentes similares o relacionadas:
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Procedimientos de tratamiento del cáncer usando antagonistas de unión al eje de PD-1 e inhibidores de TIGIT, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo antagonista anti-PD-L1 o fragmento de unión a antígeno del mismo y un anticuerpo antagonista anti-TIGIT o fragmento de unión a antígeno del mismo para su uso […]
Uso de CAR basados en ICOS para mejorar la actividad antitumoral y la persistencia del CAR, del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una secuencia de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde el CAR comprende un dominio de unión a antígeno, un dominio transmembrana […]
Péptido derivado de GPC3, composición farmacéutica para el tratamiento o la prevención de cáncer usando el mismo, inductor de inmunidad y método para producir células presentadoras de antígeno, del 17 de Junio de 2020, de CYTLIMIC INC: Composición farmacéutica para su uso en el tratamiento o la prevención de cáncer, que comprende un péptido que consiste en una secuencia de aminoácidos […]
Péptidos inhibidores derivados del transcrito de tipo TREM-1 (TLT-1) y sus usos, del 10 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido de 6 a 16 aminoácidos que comprende al menos 6 aminoácidos consecutivos de la secuencia de aminoácidos sec. con núm. de ident.: 4 para su uso en el tratamiento […]
Dominios coestimuladores para su uso en células genéticamente modificadas, del 3 de Junio de 2020, de Precision Biosciences, Inc: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica un dominio coestimulador que comprende una secuencia de aminoácidos establecida […]
Fijación eficaz como objetivo de la leucemia humana primaria utilizando células T modificadas con receptor de antígeno quimérico anti-CD123, del 3 de Junio de 2020, de NOVARTIS AG: Una molécula de ácido nucleico aislada que codifica un receptor de antígeno quimérico (CAR), en donde dicho CAR comprende un dominio de unión anti-CD123 humanizado, […]
Método para proporcionar linfocitos T específicos de tumor, del 27 de Mayo de 2020, de HS Diagnomics GmbH: Un método para fabricar un receptor artificial de linfocitos T específicos de tumor, que comprende las etapas de: - proporcionar una preparación de linfocitos […]