Uso de liposomas en un vehículo que comprende una fase hidrofóbica continua como un vehículo para el tratamiento del cáncer.
Una composición que comprende:
- un vehículo que comprende una fase continua de una sustancia hidrofóbica;
- liposomas; y
- al menos un antígeno capaz de inducir una respuesta de linfocitos T citotóxicos (CTL);
- preferiblemente que comprende además al menos un epítopo de T auxiliar.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2006/001640.
Solicitante: IMMUNOVACCINE TECHNOLOGIES INC.
Nacionalidad solicitante: Canadá.
Dirección: SUITE 303, 1819 GRANVILLE STREET HALIFAX, NOVA SCOTIA B3J 3R1 CANADA.
Inventor/es: DAFTARIAN,PIROUZ M, MANSOUR,MARC, POHAJDAK,BILL, BROWN,ROBERT G, KAST,WIJBE M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/4745 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con sistemas cíclicos teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. fenantrolinas (derivados de la yohimbina, vinblastina A61K 31/475; derivados de la ergolina A61K 31/48).
- A61K38/00 A61K […] › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/12 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos virales.
- A61K9/127 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Liposomas.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
PDF original: ES-2451599_T3.pdf
Fragmento de la descripción:
Uso de liposomas en un vehículo que comprende una fase hidrofóbica continua como un vehículo para el tratamiento del cáncer
La presente solicitud se refiere al uso de una composición que comprende liposomas y una fase hidrofóbica continua como un vehículo para la administración de un antígeno capaz de inducir una respuesta de linfocitos T citotóxicos (CTL) en el tratamiento del cáncer.
En la técnica se han descrito previamente vacunas duraderas que comprenden liposomas y una variedad de antígenos. Se ha mostrado que estas composiciones de vacuna son eficaces en la inducción de una respuesta inmune humoral aumentada (determinada por una producción incrementada de anticuerpos) frente a un antígeno específico, que depende de la función de T auxiliar 2 (Th2) . Sin embargo, para que una composición actúe adversamente sobre el cáncer, debe ser capaz de inducir una respuesta mediada por células (de linfocitos T citotóxicos (CTL) ) . Un CTL es un subgrupo de linfocitos T que es capaz de inducir la muerte de células somáticas infectadas o tumorales; matan (lisan) a las células que están infectadas con virus (u otros patógenos) o que están dañadas de otra manera o son disfuncionales. Una respuesta de CTL está mediada por citoquinas de T auxiliar 1 (Th1) .
En general, las respuestas de CTL son cortas, durando sólo varias semanas (Knutson et al., Clin. Cancer. Res. 8 (5) : 1014-1018, 1990; Dudley et al., J. Immunother. 24 (4) : 363-73, 2002; y Fernando et al., Scand. J. Immunol. 47 (5) : 459-65, 1998) . La recurrencia del cáncer siempre es una preocupación, así la inducción de una respuesta CTL duradera es necesaria para asegurar que los cánceres no recurran.
Richards et al., Immunology and Cell Biology (2004) , describen la actividad adyuvante de una emulsión de aceite en agua en la que liposomas que contienen el lípido A y el antígeno encapsulado funcionan como el agente emulsionante usando gp140 oligomérico derivado de la cubierta de VIH-1 como el antígeno. Los autores concluyeron que las emulsiones de aceite en agua liposomales estables proporcionan medios eficaces para obtener respuestas tanto de anticuerpo como CTL frente a un antígeno de cubierta de VIH.
Así, permanece una necesidad para el desarrollo de composiciones inmuno-terapéuticas duraderas para uso en el tratamiento del cáncer, sin la necesidad de múltiples tratamientos de refuerzo.
En una realización, se proporciona una composición que comprende: un vehículo que comprende una fase continua de una sustancia hidrofóbica; liposomas; y al menos un antígeno capaz de inducir una respuesta de linfocitos T citotóxicos (CTL) CD8+. La composición también comprende preferiblemente al menos un epítopo de T auxiliar.
En las figuras, que ilustran las realizaciones de la invención:
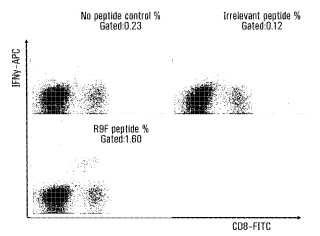
La Figura 1 ilustra la tinción ex vivo de IFN-y intracelular de esplenocitos de ratones expuestos a un epítopo E7 de HPV 16 (péptido R9F; SEQ ID NO: 1) , un péptido irrelevante o sin péptido 14 días después del tratamiento con una composición que comprende oligodesoxinucleótido CpG (CpG ODN) (SEQ ID NO: 12) , y péptido R9F fusionado con PADRE encapsulado en liposomas contenidos en una emulsión de agua en aceite PBS/FIA. Ninguno de los tratamientos control causó la expansión de las células T CD8+/IFN-y por encima de los niveles basales cuando se expusieron a posttratamiento con R9F (datos no mostrados) . Por el contrario, ocurrió un incremento de 12, 9 veces de los CTL que respondían a R9F en esplenocitos de ratones expuestos al péptido R9F comparado con ratones expuestos al péptido irrelevante.
La Figura 2 ilustra la lisis de células EL-4 cargadas con péptido R9F (SEQ ID NO: 1) (cuadrados) y cargadas con péptido irrelevante (diamantes) por esplenocitos de ratones tratados 30 días antes con una composición que comprende péptido R9F fusionado con PADRE (SEQ ID NO: 10) y encapsulado con CpG ODN (SEQ ID NO: 12) en liposomas suspendidos en una emulsión de agua en aceite PBS/FIA.
La Figura 3 ilustra la lisis de células EL-4 por esplenocitos de ratones tratados con una de las composiciones siguientes:
(i) un péptido de fusión (péptido R9F (SEQ ID NO: 1) fusionado con PADRE (SEQ ID NO: 10) ) y CpG ODN (SEQ ID NO: 12) encapsulado en liposomas suspendidos en una emulsión de agua en aceite PBS/FIA (diamantes) ; (ii) péptido de fusión y CpG ODN no encapsulado (SEQ ID NO: 12) en una emulsión de agua en aceite PBS/FIA (triángulos y cruces) , o (iii) péptido de fusión encapsulado en liposomas en una emulsión de agua en aceite PBS/FIA (círculos cerrados) . Los esplenocitos se expusieron al péptido R9F (cruces, diamantes y círculos cerrados) o a un péptido irrelevante (SEQ ID NO: 13) (triángulos y círculos abiertos) 130 días después del tratamiento. Los esplenocitos de ratones tratados con el péptido de fusión solo mostraron niveles basales de lisis de células EL-4 expuestas a R9F o a un péptido irrelevante 130 días después del tratamiento (datos no mostrados) .
La Figura 4 ilustra el efecto de una única administración de una composición que comprende CpG ODN, un péptido de fusión (péptido R9F (SEQ ID NO: 1) fusionado con PADRE (SEQ ID NO: 10) ) encapsulado en liposomas suspendidos en una emulsión de agua en aceite PBS/FIA (cuadrados abiertos) en el tamaño de tumores C3 de 14 días en ratones. Los tumores eran indetectables por palpación hacia el día 30 (16 días después del tratamiento) . Por el contrario, los tumores C3 en ratones a los que se proporcionó un tratamiento control que comprende la composición como se ha descrito anteriormente en ausencia de un péptido de fusión (cuadrados cerrados) continuó incrementando en tamaño. Todos los ratones (n= 10) se pulsaron con 0, 5 x 106 células tumorales C3 14 días antes del tratamiento. La diferencia en tamaño de los tumores en los dos grupos de tratamiento fue estadísticamente significativa (p= 0, 002 en el día 25) .
La Figura 5 ilustra el efecto del tratamiento profiláctico en el porcentaje de ratones que no tienen tumor 61 días después del pulso con 0, 5 x 106 células C3. Los grupos de tratamiento consistieron en ratones tratados con una de las composiciones siguientes que comprenden: (1) PBS; (2) CpG en PBS; (3) péptido de fusión (péptido R9F (SEQ ID NO: 1) fusionado con PADRE (SEQ ID NO: 10) ) en PBS; (4) péptido de fusión encapsulado en liposomas suspendidos en una emulsión de agua en aceite PBS/FIA; (5) péptido de fusión y CpG ODN en una emulsión de agua en aceite; (6) péptido de fusión y CpG ODN encapsulados en liposomas; (7) péptido de fusión y el lipopéptido, Pam3Cys-SKKKK (Pam3c) encapsulado en liposomas suspendidos en una emulsión de agua en aceite.
La Figura 6 ilustra la detección ex vivo de esplenocitos que producen IFN-y específicos de TRP-2 (células formadoras de manchas, SFC) en ratones 8 días después de un único tratamiento con una de los siguientes: (A) una composición que comprende un péptido de proteína relacionada con tirosina 2 (TRP-2) (S9L; SEQ ID NO: 7) con PADRE (SEQ ID NO: 10) y CpG ODN (SEQ ID NO: 12) encapsulado en liposomas suspendidos en una emulsión de agua en aceite PBS/ISA51;
(B) una composición que comprende S9L con PADRE en liposomas suspendidos en una emulsión de agua en aceite; o
(C) una composición que comprende un péptido irrelevante (SEQ ID NO: 13) con CpG en liposomas suspendidos en una emulsión de agua en aceite PBS/ISA51.
La Figura 7 ilustra la detección ex vivo de esplenocitos que producen IFN-y específico de p53 (SFC) en ratones después de un único tratamiento con (A) un péptido p53 modificado (mK9M; SEQ ID NO: 8) con PADRE (SEQ ID NO: 10) y CpG ODN (SEQ ID NO: 12) encapsulados en liposomas y suspendidos en una emulsión de agua en aceite PBS/ISA51, o una de las composiciones control siguientes: (B) mK9M con PADRE en una emulsión de agua en aceite; (C) mK9M con PADRE encapsulado en liposomas y suspendidos en una emulsión de agua en aceite; y (D) un péptido irrelevante (SEQ ID NO: 13) con CpG encapsulado en liposomas y suspendidos en una emulsión de agua en aceite.
La Figura 8 ilustra la detección ex vivo de esplenocitos que producen IFN-y específico de TRP-2 y p53 (SFC) en ratones después de un único tratamiento con una composición que comprende (A) péptidos p53 (péptido mK9M; SEQ ID NO: 8) y TRP-2 (V8L; SEQ ID NO: 6) con PADRE (SEQ ID NO: 10) y CpG ODN (SEQ ID NO: 12) encapsulados en liposomas y suspendidos en una emulsión de agua en aceite PBS/ISA51, o una de las composiciones control siguientes: (B) péptidos p53 y TRP-2 con PADRE encapsulados en liposomas y suspendidos en una emulsión de agua en aceite PBS/ISA51; (C) péptidos p53 y TRP-2 con PADRE y CpG ODN; (D) péptidos p53 y TRP-2... [Seguir leyendo]
Reivindicaciones:
1. Una composición que comprende:
- un vehículo que comprende una fase continua de una sustancia hidrofóbica;
- liposomas; y
- al menos un antígeno capaz de inducir una respuesta de linfocitos T citotóxicos (CTL) ;
- preferiblemente que comprende además al menos un epítopo de T auxiliar.
2. La composición de la reivindicación 1, en la que el epítopo de T auxiliar es una molécula separada del al menos un antígeno o, en la que el antígeno comprende el epítopo de T auxiliar.
3. La composición de la reivindicación 1 o reivindicación 2, en la que el antígeno es un polipéptido.
4. La composición de una cualquiera de las reivindicaciones 1 a 3, en la que el antígeno comprende un epítopo de CTL,
o una combinación de epítopos de CTL, en la que preferiblemente el epítopo de CTL deriva de un virus.
5. La composición de la reivindicación 4, que comprende una pluralidad de epítopos de CTL unidos para formar un único polipéptido y/o en la que el epítopo de CTL deriva de una proteína asociada a tumor.
6. La composición de una cualquiera de las reivindicaciones 1 a 5, en la que el epítopo de T auxiliar es un epítopo de T auxiliar universal.
7. La composición de una cualquiera de las reivindicaciones 1 a 6, en la que el epítopo de T auxiliar está fusionado con el al menos un antígeno.
8. La composición de una cualquiera de las reivindicaciones 1 a 7, en la que la composición es capaz de incrementar las células que producen IFN-y.
9. La composición de una cualquiera de las reivindicaciones 1 a 7, que comprende además un adyuvante, preferiblemente un oligodesoxinucleótido CpG (CpG ODN) y/o un lipopéptido.
10. La composición de una cualquiera de las reivindicaciones 1 a 9 para el tratamiento de cáncer en un sujeto, preferiblemente un mamífero, más preferiblemente un ser humano; y/o preferiblemente un cáncer seleccionado del grupo que consiste en: cervical, vulvar, melanoma, mama, pulmón, ovario, mieloma múltiple, linfoma de células B, hepatoma, sarcoma, vejiga, cáncer de próstata, tiroides, tumores H/N, colon, rectal, renal, pancreático, gástrico, adenocarcinoma, leucemia de células T, linfosarcoma, uterino, esofágico, linfomas no de Hodgkin, endometrial y tumores RCC.
11. La composición de una cualquiera de las reivindicaciones 1 a 9, en la que el liposoma, preferiblemente obtenido de lípidos naturales; lípidos sintéticos que incluyen preferiblemente constituyentes de ácidos grasos seleccionados de lauroil, miristoil, palmitoil, estearoil, araquidoil, oleolil, linoleoil y eurocoil, o combinaciones de éstos; esfingolípidos; lípidos éter; esteroles; cardiolipina; lípidos catiónicos; y lípidos modificados con poli (etilen glicol) y otros polímeros; comprende un fosfolípido y/o un colesterol no esterificado.
12. Una composición producida por un método que comprende combinar en una primera etapa liposomas y un antígeno capaz de inducir una respuesta de linfocitos T citotóxicos (CTL) y en una segunda etapa añadir un vehículo que comprende una fase continua de una sustancia hidrofóbica, en la que preferiblemente dicho antígeno está encapsulado en dichos liposomas.
13. La composición según la reivindicación 12, en la que dicho método comprende además combinar un epítopo de T auxiliar con dichos liposomas y dicho antígeno, antes de añadir dicho vehículo, en la que preferiblemente dicho epítopo de T auxiliar está encapsulado en dichos liposomas, y/o en la que preferiblemente dicho epítopo de T auxiliar es una molécula separada de dicho antígeno o dicho antígeno comprende dicho epítopo de T auxiliar.
14. La composición según la reivindicación 12 ó 13, en la que dicho método comprende además combinar un adyuvante con dichos liposomas, dicho antígeno y dicho vehículo, en la que preferiblemente dicho adyuvante está encapsulado en dichos liposomas.
15. La composición según una cualquiera de las reivindicaciones 12 a 14, en la que dichos liposomas se liofilizan antes de combinarlos con dicho vehículo.
16. La composición según una cualquiera de las reivindicaciones 12 a 15, en la que al menos parte de dicho antígeno no está encapsulada en dichos liposomas, estando dicho antígeno asociado con la superficie externa de dichos liposomas y/o separado de dichos liposomas en dicho vehículo.
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Métodos de tratamiento y prevención de infecciones por staphylococcus aureus y afecciones asociadas, del 15 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición para uso en un método de inmunización de un sujeto contra la infección por S. aureus, comprendiendo dicha composición: (i) un fragmento de polipéptido […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]