Proteína CCN3 para su utilización en el tratamiento y el diagnóstico de enfermedades renales.
Proteína CCN3 de longitud completa para uso en tratar una enfermedad renal en un sujeto.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/000833.
Solicitante: ROSALIND FRANKLIN UNIVERSITY OF MEDICINE AND SCIENCE.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3333 GREEN BAY ROAD NORTH CHICAGO, IL 60064 ESTADOS UNIDOS DE AMERICA.
Inventor/es: RISER,BRUCE L, PERBAL,BERNARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
PDF original: ES-2395260_T3.pdf
Fragmento de la descripción:
Campo de la Invención:
La presente invención es definida en la reivindicaciones 1-18. La CCN3 puede ser una proteína CCN3 de longitud total o un fragmento de la misma, o una isoforma de la CCN3 de longitud completa, o una combinación de las mismas. La CCN3 aislada y purificada puede ser potencialmente usada en el tratamiento de estas enfermedades regulando la expresión y/o actividad de la proteína CCN2. El nivel de CCN3 en tejido o fluidos corporales puede ser también utilizado para predecir, diagnosticar y/o seguir la progresión de las enfermedades asi como para determinar la eficacia de la intervención terapéutica.
La Familia CCN de Genes y Proteínas.
La familia de genes de CCN actualmente consiste de seis elementos distintos que codifican proteínas que participan en procesos biológicos fundamentales tales como la proliferación celular, unión, migración, diferenciación, cicatrización de heridas, angiogénesis, y diversas enfermedades incluyendo fibrosis y tumorigénesis. Las proteínas codificadas por los elementos de la familia génica de CNN son proteínas de 30-40 kDa extremadamente ricas en cisteína (10% en masa) (Perbal B., NOV and the CCN family of genes: structural and functional issues. Molecular Pathology 54: 57-79, 2001) . más recientemente, ha sido informado que algunas formas de las proteínas CCN (CCN3 incluidas) estan en el orden de 35-55 kDa. Son designadas como proteínas 61 ricas en cisteína (CYR-61) , proteínas de factor de crecimiento de tejido conectivo (CTGF) , proteínas sobreexpresadas en nefroblastoma (NOV) , proteínas-1 segregadas inducida por Wnt (WISP-1) , proteínas-2 segregadas inducidas por Wnt (WISP-2) , y proteínas-3 segregadas inducidas por Wnt (WISP-3) . más recientemente, ha sido propuesta una nueva nomenclatura para esta familia de genes y proteínas (ver la Tabla 1) .
Tabla 1: Nombres Propuestos y Nombres Usados Actualmente y Previamente para la Familia CCN de Genes y Proteínas
Nombre Propuesto Nombres usados actualmente o previamente
CCN1 CYR61 (humanoo, ratón, xenopus) , CEF10 (pollo) , IGFBPrP4 (humano) , βIG-M1 (ratón) , CTGF-2, IGFBP10 (humano) , angiopro
CCN2 CTGF (humano, ratón, pollo, xenopus) , βIG-M2 (ratón) , FISP12 (ratón) , IGFBP-rP2 (humano) , Hsc24 (humano) , IGFBP8 (humano) , HBGF-0.8, ecogenin (humano)
CCN3 NOV (humano, rata, pollo, ratón, codorniz) , IGFBP-rP3 (humano) , IGFBP9 (humano) , NOVH (humano) , NOVm, mNOV (ratón) , xNOV (xenopus)
CCN4 WISP-1 (humano) , ELM-1
CCN5 WISP-2 (humano) , CTGF-L, CTGF-3, HICP, rCOP-1 (rata)
CCN6 WISP-3 (humano)
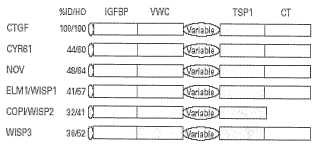
La FIG. 1 muestra la estructura modular de las proteínas CCN. Aunque tienen una organización multimodular muy conservada, con cuatro módulos compartiendo identidad con las proteínas de unión de factor de crecimiento tipo insulina (IGFBPs) , el factor Von Willebrand (VWC) , trombospondina-1 (TSP1) , y una familia de reguladores de crecimiento conteniendo nudo de cisteína (CT) , las proteínas CCN tienen propiedades biológicas distintivas y son reguladas de manera diferencial. Su implicación ha sido mostrada en múltiples sistemas orgánicos. Un órgano que ha sido el foco de un gran númeo de estudios es el riñón. Los mecanismos subyacentes de la acción de las proteínas CCN son todavía mal interpretados. Los intentos para identificar receptores transductores de señales únicas y específicas de alta afinidad no han aportado ningún fruto. (Brigstock D. R. Regulation of angiogénesis and endothelial cell function by connective tissue growth factor. FEBS Letters 327: 125-130, 2003) .
El Gen CCN2 y su Proteína Codificada [0004] De los seis elementos de la familia CCN, la CCN2 ha emergido como una importante jugadora en sus papeles en la regulación de ciertas funciones celulares importantes en el crecimiento esqueletico y angiogénesis placentaria, asi como sus papeles en ciertas enfermedades incluyendo la fibrosis (fibrosis renal y asociada con la diabetes) y quizás la tumorigénesis.
Estudios con el sistema renal han proporcionado pruebas del papel de CCN2 como un importante factor patogénico en la fibrosis/esclerosis en un número de modelos de renopatía crónica (CKD) . Informes tempranos sugirieron un posible papel interactivo con los factores de crecimiento transformantes beta (CTGF-β) en fibrosis dérmica y esclerodermia (Bradham DM et al, Connective tissue growth factor: a cysteine-rich mitogen secreted by human vascular endothelial cells is related to SCR-induced immediate early gene product CEF-10. Journal of Cell Biology, 114:1285-1294, 1991) .
La formación de esclerosis o fibrosis en el riñón es una respuesta común para formas crónicas o severas de lesión. Al menos en enfermedades crónicas renales (CKD) , parece haber tres factores causales predominantes: metabólico, genético, y hemodinámico. Todos estos factores pueden interactuar, particularmente en la nefropatía diabética (DN) , para conducir la progresión. CCN2 parece ahora ser un mediador central, posterior de los efectos de estos tres elementos. Por ejemplo, la fuerza tangencial o de estiramiento patológica que resulta de la hipertensión intraglomerular parece estimular la producción de citoquinas incluyendo CCN2. Esta misma fuerza resulta ser responsable de la permeabilidad vascular aumentada llevando tanto a la proteinuria como a una producción incrementada de hormonas vasoactivas tales como la angiotensina (AG) II y endotelina, la cuales a su vez también elevan CCN2 y ademas aumentan la fuerza mecánica. La acumulación anormal de productos finales de glicosilación mejorada (AGEs) que sucede con el metabolismo alterado de glucosa en DN puede también funcionar tanto para aimentar directamente la reticulación y la acumulación de la matriz extracelular (ECM) , como para aumentar CCN2. Los antecedentes genéticos del individuo pueden influir en los elementos de hemodinámica y metabolismo, y a su vez las vias resultantes como se ha descrito. Adicionalmente existe una probable influencia de la genética sobre la actividad de la proteína kinasa C (PKC) y producción de hormonas vasoactivas. En todos los casos, la regulación creciente crónica de la actividad de CCN2 es probable que de lugar a un movimiento alterado de ECM y acumulación creciente de ECM, produciendo fibrosis o esclerosis. Estos hallazgos apoyan el postulado de que CCN2 es un elemento central aguas abajo en la progresión de la fibrosis renal, y como tal proporciona un objetivo razonable y novedoso para fines tanto diagnósticos como terapeúticos.
CCN2 es estrógeno-inducible y sobreexpresada en tumores uterinos o de mama dependientes de esteroides (Tsai et al., Expression and function of CYR61, an angiogenic factor, in breast cancer cell lines and tumor biopsies. Cancer Research 60: 5602-5607, 2000; Tsai et al., Expression and regulation of Cyr61 in humano breast cancer cell lines. Oncogene 21: 964-974, 2000; Sampath et al. Cyr61, a member of the CCN family, is required for MCF-7 cell proliferataion: regulation by 17 beta-estradiol and overexpression in humano breast cancer. Endocrinology 142: 25402548, 2001; Sampath et al., Aberrant expression of Cyr 61, a member of the CCN family (i.e. CCN1) , and dysregulation by 17 beta-estradiol and basic fibroblast growth factor in humano uterine leiomyomas.. Journal of Clínical Endocrinology and Metabolism, 86: 1707-1715, 2001; Sampath et al, The angiogenic factor Cyr61 is induced by progestin R5020 and is necessar y for mammar y adenocarcinorma cell growth. Endocrine, 18: 147-150, 2002; Xie et al., Breast cancer, Cyr61 is overexpressed, estrogen-inducible, and associated with more advanced disease. Journal of Biological Chemistr y , 276: 14187-14194, 2001; Xie et al., Elevated levels of connective tissue growth factor, WISP-1, and CYR61 in primar y breast cancers associated with more advanced features. Cancer Research, 61: 8917-8923, 2002) . CCN2 y otros elementos de la familia de CCN son importantes mediadores aguas abajo del crecimiento celular regulado por progesterona y estrógeno. La CCN2 y otras proteínas CCN pueden también impactar otras vías eguladoras de crecimiento celular en celulas de cancer mamario. La CCN2 uterina es regulada tanto por el estrógeno como la progesterona y parece ser importante para el mantenimiento y remodelación de la ECM estromal (Rageh et al., Steroidal regulation of connective tissue growth factor (CCN2; CTGF) synthesis in the ratón uterus. Molecular Pathology, 56: 80-85, 2001; Cheon et al., A genomic approach to identify novel progesterona receptor regulated pathways in the uterus during implantation. Molecular Endocrinology, 16: 2853-2871, 2002) . En el ovario, CCN2 es regulado por gonadotropinas o factor transformante de crecimiento beta (CTGF-β) y se asocia con reclutamiento y mitosis de células tecales,... [Seguir leyendo]
Reivindicaciones:
1. Proteína CCN3 de longitud completa para uso en tratar una enfermedad renal en un sujeto.
2. Proteína CCN3 de longitud completa para uso según la reivindicación 1 en donde la enfermedad renal es enfermedad crónica renal, fibrosis renal o esclerosis renal.
3. Proteína CCN3 de longitud completa para uso según la reivindicación 1 o 2 en donde el sujeto es un sujeto humano.
4. Proteína CCN3 de longitud completa para uso según a la Reivindicación 1 en donde el sujeto ha sido diagnosticado de enfermedad renal detectando el nivel o actividad de CCN3 en una muestra de tejido o fluido corporal del sujeto y comparando el nivel o actividad de CCN3 en la muestra con un nivel o actividad normal de CCN3 en un sujeto sano.
5. Proteína CCN3 de longitud completa para uso según la reivindicación 4, en donde el sujeto es diagnosticado de enfermedad renal detectando el nivel o actividad de CCN2 en una muestra de tejido o fluido corporal del sujeto y comparando el nivel o actividad de CCN2 en la muestra con un nivel o actividad normal de CCN2 en un sujeto sano.
6. Proteína CCN3 de longitud completa para uso según la reivindicación 1, en donde el nivel o actividad de CCN3 en una muestra de tejido o fluido corporal del sujeto es usada para seguir la progresión de la enfermedad renal, o para determinar la eficacia de la intervención terapéutica, en el sujeto.
7. Proteína CCN3 de longitud completa para uso según cualquiera de las reivindicaciones 4-6, en donde la muestra de fluido corporal es orina, sangre, suero, plasma o lavado peritoneal.
8. Proteína CCN3 de longitud completa para uso según cualquiera de las reivindicaciones 4-7, en donde el nivel de CCN3 o CCN2 es detectado por un inmunoensayo.
9. Proteína CCN3 de longitud completa para uso según la reivindicación 2, en donde la fibrosis renal o esclerosis renal está asociada con proliferación celular incrementada.
10. Proteína CCN3 de longitud completa para uso según la reivindicación 9, en donde la proliferación celular da lugar a enfermedad proliferativa glomerular.
11. Proteína CCN3 de longitud completa para uso según la reivindicación 1, en donde el sujeto se somete a diálisis peritoneal con una solución de diálisis, y la proteína CCN3 de longitud completa se formula para la administración al sujeto en la solución de diálisis.
12. Un método para diagnosticar enfermedad renal en un sujeto, el metodo comprendiendo: detectar el nivel o actividad de CCN3 en una muestra de tejido o fluido corporal del sujeto y comparando el nivel o actividad de CCN3 en la muestra con un nivel o actividad normal de CCN3 en un sujeto sano.
13. El método de la reivindicación 12, en donde la muestra es orina, sangre, suero, plasma o lavado peritoneal.
14. El método de la reivindicación 12, en donde el nivel de actividad CCN3 es detectado por un inmunoensayo.
15. El método de la reivindicación 14 en donde el inmunoensayo utiliza un anticuerpo especifico para CCN3.
16. El método de la reivindicación 15 en donde el anticuerpo es seleccionado de anticuerpos monoclonales o policlonales.
17. Proteína CCN3 de longitud completa para uso según la reivindicación 1, en donde la proteína CCN3 de longitud completa se formula para la administración al sujeto por administración intramuscular, intravenosa, oral, nasal, tópica o transdérmica, o por inhalación.
18. Un método para diagnosticar enfermedad renal en un sujeto, el método comprendiendo comparar un nivel o actividad de CCN3 con CCN2 en una muestra de tejido o fluido corporal del sujeto para diagnosticar la enfermedad renal.
Patentes similares o relacionadas:
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Ratón nuligénico para Pint que muestra un fenotipo asociado a envejecimiento prematuro, del 10 de Junio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón cuyo genoma comprende una inactivación de un locus del ARN no codificante largo (ARNlnc) Pint endógeno, en donde la inactivación (i) da como resultado que el […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]