Producción de glucoproteínas.
Un procedimiento para producir una glucoproteína con un patrón de glucosilación mejorado en un cultivo celular,
que comprende:
cultivar células de mamífero que contienen un gen que codifica una glucoproteína de interés en un medio de cultivo celular que comprende manganeso a entre aproximadamente 10 nM y 600 nM;
mantener el cultivo en un primer intervalo de temperatura durante un primer período de tiempo suficiente para permitir que las células se reproduzcan hasta una densidad celular viable en un intervalo de aproximadamente el 20% - 80% de la densidad celular viable máxima posible si el cultivo se mantiene en el primer intervalo de temperatura; cambiar el cultivo a un segundo intervalo de temperatura, siendo al menos una temperatura del segundo intervalo de temperatura menor que la temperatura menor del primer intervalo de temperatura;
mantener el cultivo durante un segundo período de tiempo en las condiciones y el tiempo suficientes para permitir la expresión de la glucoproteína, en el que el patrón de glucosilación de la glucoproteína expresada es más amplio que el patrón de glucosilación observado en unas condiciones por lo demás idénticas en un medio por lo demás idéntico que carezca de manganeso.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/015767.
Solicitante: WYETH LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LASKO,DANIEL R, KOZA,STEPHAN M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00).
PDF original: ES-2440487_T3.pdf
Fragmento de la descripción:
Producción de glucoproteínas Esta invención se refiere a un procedimiento para producir una glucoproteína en un medio de cultivo celular que que comprende manganeso, y a un medio de cultivo celular para su uso en dicho procedimiento.
Antecedentes de la invención Las proteínas y las polipéptidos se han convertido en unos agentes terapéuticos cada vez más importantes. En la mayoría de los casos, estas proteínas y polipéptidos se producen en un cultivo celular a partir de células que han sido modificadas por ingeniería genética y/o seleccionadas para producir unos niveles inusualmente altos de la proteína o del polipéptido de interés en particular. El control y la optimización de las condiciones de cultivo celular son críticamente importantes para el éxito de la producción comercial de proteínas y polipéptidos.
Muchas proteínas y polipéptidos producidos en cultivo celular son glucoproteínas que contienen estructuras de carbohidratos unidos covalentemente, incluidas cadenas de oligosacáridos. Estas cadenas de oligosacáridos son unidas a la proteína en el retículo endoplásmico y en el aparato de Golgi a través de enlaces de N o de enlaces de O. Las cadenas de oligosacáridos pueden comprender una porción significativa de la masa de la glucoproteína. Se cree que las cadenas de oligosacáridos juegan unos papeles clave en la función de la glucoproteína, incluyendo facilitar un correcto plegamiento de la glucoproteína, mediar en las interacciones proteína-proteína, conferir estabilidad, conferir unas propiedades farmacodinámicas y/o farmacocinéticas ventajosas, inhibir la digestión proteolítica, dirigir la glucoproteína a la vía de secreción adecuada y dirigir la glucoproteína a un órgano u órganos en particular.
Generalmente, las cadenas de oligosacáridos unidas por N se añaden a la proteína emergente en translocación en la luz del retículo endoplásmico (véase Molecular Biology of the Cell, de Alberts y col., 1994) . El oligosacárido es añadido al grupo amino de la cadena lateral de un residuo de asparragina contenido en la secuencia consenso objetivo de Asn-X-Ser/Thr, donde X puede ser cualquier aminoácido excepto prolina. La cadena inicial de oligosacáridos habitualmente es recortada por unas enzimas específicas de glucosidasa en el retículo endoplásmico, dando como resultado un núcleo de oligosacárido corto y ramificado formado por dos residuos de Nacetilglucosamina y tres de manosa.
Después del procesado inicial en el retículo endoplásmico, la glucoproteína es trasladada a través de vesículas pequeñas al aparato de Golgi, donde la cadena de oligosacárido experimenta un procesado adicional antes de ser secretada a la superficie celular. La cadena de oligosacárido recortada unida por N puede ser modificada mediante la adición de varios residuos de manosa, dando como resultado un oligosacárido con un alto contenido en manosa. Alternativamente, pueden añadirse una o más unidades de N-acetilglucosamina de los monosacáridos a las subunidades de manosa de núcleo para formar oligosacáridos complejos. Puede añadirse galactosa a las subunidades de N-acetilglucosamina, y pueden añadirse subunidades de ácido siálico a las subunidades de galactosa, dando como resultado cadenas que terminan en cualquiera de un residuo de ácido siálico, de galactosa o de N-acetilglucosamina. Adicionalmente, puede añadirse un residuo de fucosa a un residuo de N-acetilglucosamina del oligosacárido de núcleo. Cada una de estas adiciones está catalizada por glucosiltransferasas específicas.
Además de ser modificadas mediante la vía de glucosilación unida por N, las glucoproteínas también pueden ser modificadas mediante la adición de cadenas de oligosacáridos unidas por O a residuos específicos de serina o de treonina según son procesadas en el aparato de Golgi. Los residuos de un oligosacárido unido por O se añaden uno por uno, y la adición de cada residuo está catalizada por una enzima específica. Al contrario que la glucosilación unida por N, la secuencia consenso de aminoácidos para la unión por O no está tan bien definida.
La calidad y el grado finales de glucosilación de la proteína pueden verse drásticamente afectados por las condiciones del cultivo celular. Por ejemplo, los procesos de cultivo tradicionales por lotes y semicontinuos se han centrado en el nivel final de péptido producido, y a menudo dan como resultado una producción de una glucoproteína con un patrón de glucosilación menos extenso y/o un patrón de glucosilación cuyos residuos de azúcar de la cadenas de oligosacáridos reflejan muy poco los residuos de azúcar que están presentes en la forma natural de la glucoproteína. El aumento de la extensión de la glucosilación y/o el ajuste de la composición de los residuos de azúcar para que reflejen más fielmente el nivel y la composición de la glucosilación que están presentes en la forma natural de la glucoproteína, podrían dar potencialmente como resultado un agente de una glucoproteína terapéutica con una mayor potencia, unas propiedades farmacodinámicas y/o farmacocinéticas mejoradas y menos efectos secundarios. Aunque se han realizado algunos esfuerzos para mejorar la calidad y la cantidad de la glucosilación de las glucoproteínas producidas en cultivo celular, permanece una necesidad de mejoras adicionales. Existe una necesidad en particular de desarrollar sistemas para la producción de glucoproteínas con unos patrones de glucosilación mejorados mediante el cultivo celular en medio defmed.
Sumario de la invención Los procedimientos y las composiciones de la presente invención proporcionan un sistema mejorado para la producción a gran escala de glucoproteínas con unos patrones de glucosilación mejorados en cultivo celular. Por
ejemplo, en ciertas formas de realización, la presente invención proporciona procedimientos de cultivo a escala comercial (por ejemplo, de 500 l o más) que utilizan un medio que contiene una concentración molar acumulativa de manganeso de entre aproximadamente 10 y 600 nM. En ciertas formas de realización, la concentración molar acumulativa de glutamina en el medio es menor de aproximadamente 8 mM. En ciertas formas de realización, la concentración molar acumulativa de glutamina en el medio es menor de aproximadamente 4 mM. Debería entenderse que "acumulativo", según se usó anteriormente, se refiere a la cantidad total de un componente o componentes en particular añadidos durante el transcurso del cultivo celular, incluyendo los componentes añadidos al comienzo del cultivo y los componentes añadidos subsiguientemente. En ciertas formas de realización de la invención, es deseable minimizar las "aportaciones" en el cultivo con el tiempo, por lo que es deseable maximizar las cantidades presentes inicialmente. Por supuesto, los componentes del medio son metabolizados durante el cultivo, por lo que cultivos con las mismas cantidades acumulativas de unos componentes dados tendrán diferentes niveles absolutos si sus componentes son añadidos en momentos diferentes (por ejemplo, todos los presentes inicialmente frente a algunos añadidos mediante aportaciones) .
Según la presente invención, el uso de dicho medio permite la producción de glucoproteínas que contienen unos patrones de glucosilación deseables. En algunas formas de realización, las glucoproteínas pueden tener un patrón de glucosilación más amplio y/o pueden tener una distribución de las cadenas de oligosacáridos que se parezca más a la distribución de las cadenas de oligosacáridos aplicada a la glucoproteína por la célula hospedadora natural. En algunas formas de realización, el uso del sistema inventivo puede dar como resultado la producción de una glucoproteína con un patrón de glucosilación similar o idéntico al patrón de glucosilación que estaría presente si la glucoproteína fuera expresada en una célula humana endógena.
El experto habitual en la técnica comprenderá que las formulaciones de los medios de la presente invención engloban tanto medios definidos como complejos. En ciertas formas de realización, el medio de cultivo es un medio definido en el que la composición del medio es conocida y está controlada.
Los cultivos celulares de la presente invención pueden estar opcionalmente complementados con nutrientes y/u otros componentes de medios que incluyen hormonas y/u otros factores de crecimiento, en particular iones (tales como sodio, cloruro, calcio, magnesio y fosfato) , tampones, vitaminas, nucleósidos o nucleótidos, oligoelementos (compuestos inorgánicos presentes habitualmente a unas concentraciones finales muy bajas) , aminoácidos, lípidos o glucosa u otra fuente de energía. En ciertas formas de realización, puede ser beneficioso complementar el medio... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para producir una glucoproteína con un patrón de glucosilación mejorado en un cultivo celular, que comprende:
cultivar células de mamífero que contienen un gen que codifica una glucoproteína de interés en un medio de cultivo celular que comprende manganeso a entre aproximadamente 10 nM y 600 nM; mantener el cultivo en un primer intervalo de temperatura durante un primer período de tiempo suficiente para permitir que las células se reproduzcan hasta una densidad celular viable en un intervalo de aproximadamente el 20% -80% de la densidad celular viable máxima posible si el cultivo se mantiene en el primer intervalo de temperatura; cambiar el cultivo a un segundo intervalo de temperatura, siendo al menos una temperatura del segundo intervalo de temperatura menor que la temperatura menor del primer intervalo de temperatura; mantener el cultivo durante un segundo período de tiempo en las condiciones y el tiempo suficientes para permitir la expresión de la glucoproteína, en el que el patrón de glucosilación de la glucoproteína expresada es más amplio que el patrón de glucosilación observado en unas condiciones por lo demás idénticas en un medio por lo demás idéntico que carezca de manganeso.
2. El procedimiento de la reivindicación 1, en el que el primer intervalo de temperatura comprende un intervalo de temperatura que es de aproximadamente 30 a 42 grados Celsius.
3. El procedimiento de la reivindicación 2, en el que el primer intervalo de temperatura comprende una temperatura que es de aproximadamente 37 grados Celsius.
4. El procedimiento según una cualquiera de las reivindicaciones 1 a 3, en el que el segundo intervalo de temperatura comprende un intervalo de temperatura que es de aproximadamente 25 a 41 grados Celsius.
5. El procedimiento de la reivindicación 4, en el que el segundo intervalo de temperatura comprende una temperatura que es de aproximadamente 31 grados Celsius.
6. El procedimiento según una cualquiera de las reivindicaciones 1 a 5, que comprende adicionalmente una segunda etapa de cambio subsiguiente a la primera etapa de cambio que comprende cambiar el cultivo a una tercera temperatura o intervalo de temperatura, siendo al menos una temperatura del tercer intervalo de temperatura menor que la menor temperatura del segundo intervalo de temperatura.
7. El procedimiento según una cualquiera de las reivindicaciones 1 a 6, en el que el medio de cultivo celular comprende entre aproximadamente 20 y 200 nM de manganeso.
8. El procedimiento de la reivindicación 7, en el que el medio de cultivo celular comprende aproximadamente 40 nM de manganeso.
9. El procedimiento según una cualquiera de las reivindicaciones 1 a 8, en el que el medio de cultivo celular comprende glutamina a una concentración inicial que es menor que o igual a aproximadamente 8 mM.
10. El procedimiento de la reivindicación 9, en el que la concentración inicial de glutamina del medio de cultivo celular es menor que o igual a aproximadamente 4 mM.
11. El procedimiento según una cualquiera de las reivindicaciones 1 a 10, en el que el volumen del cultivo celular es de al menos aproximadamente 500 l.
12. El procedimiento según una cualquiera de las reivindicaciones 1 a 11, en el que el cultivo celular se provee adicionalmente con un medio de alimentación tras el comienzo del cultivo celular inicial.
13. El procedimiento según una cualquiera de las reivindicaciones 1 a 12, en el que el cultivo celular se provee adicionalmente con componentes complementarios.
14. El procedimiento de la reivindicación 13 en el que los componentes complementarios se eligen de entre el grupo constituido por hormonas y/u otros factores de crecimiento, iones inorgánicos, tampones, vitaminas, nucleósidos o nucleótidos, oligoelementos, aminoácidos, lípidos, glucosa u otras fuentes de energía, y combinaciones de los mismos.
15. El procedimiento de la reivindicación 14, en el que el cultivo celular es complementado con aproximadamente 2 gramos por litro de glucosa.
16. El procedimiento según una cualquiera de las reivindicaciones 1 a 15, en el que el medio de cultivo celular está definido.
17. El procedimiento según una cualquiera de las reivindicaciones 1 a 16, en el que la glucoproteína de interés comprende el factor de coagulación IX.
18. El procedimiento de la reivindicación 17, en el que el factor de coagulación IX es factor de coagulación IX humano recombinante.
19. El procedimiento según una cualquiera de las reivindicaciones 1 a 16, en el que la glucoproteína de interés comprende un anticuerpo anti-ABeta.
20. El procedimiento de la reivindicación 19, en el que el anticuerpo anti-ABeta es un anticuerpo monoclonal.
21. El procedimiento de la reivindicación 20, en el que el anticuerpo anti-ABeta es un anticuerpo monoclonal humanizado de un péptido anti-ABeta de IgG1.
Patentes similares o relacionadas:
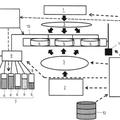 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Composiciones mejoradas para hidrogeles, del 22 de Julio de 2020, de Biogelx Limited: Una composición de hidrogel, que comprende una mezcla de los derivados peptídicos primero y segundo en una proporción de 1:4 a 4:1, en donde los primeros derivados […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Producción de tapsigarginas por cultivo en suspensión de células de Thapsia, del 6 de Mayo de 2020, de PHYTON HOLDINGS, LLC: Método de producción de lactonas sesquiterpénicas de la familia de tapsigargina, comprendiendo el método las etapas de: (a) cultivar células vegetales […]
Composición de medio para preparar toxina botulínica, del 6 de Mayo de 2020, de Daewoong Co., Ltd: Una composición de medio libre de EET para su uso en el cultivo de Clostridium botulinum, la composición de medio comprende: peptonas de origen […]
Células virales resistentes y sus usos, del 22 de Abril de 2020, de Sigma-Aldrich Co. LLC: Una línea celular de ovario de hámster chino (CHO) modificada genéticamente en la que la entrada y/o propagación del virus diminuto del ratón (MVM) […]
Composiciones de cultivo de células con antioxidantes y procedimientos para la producción de polipéptidos, del 15 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento de producción de un anticuerpo o un fragmento del mismo producido recombinantemente que comprende la etapa de cultivar una célula que comprende […]