Modificación de Factor VIII.
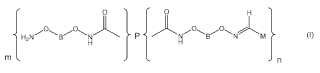
Derivado de Factor VIII de la fórmula (I):
donde:
B representa un alquileno C2 a C10;
m representa 0 o un número entero de 1 a 19, n representa un número entero de 1 a 20 y la suma de m y n esde 1 a 20;
P representa un mono o polirradical de Factor VIII obtenido por eliminación de los grupos de carbamoil m + n apartir de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII; y
M representa una fracción (M1) que aumenta la vida media en plasma del derivado de Factor VIII o una fracciónindicadora (M2);
o una sal derivada farmacéuticamente aceptable.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/052022.
Solicitante: NOVO NORDISK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: Novo Allé 2880 Bagsværd DINAMARCA.
Inventor/es: MADSEN, KJELD, PESCHKE, BERND, ZUNDEL,MAGALI, KARPF,DITTE MARIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/37 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores VIII.
- C07K14/755 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factores VIII.
- C12P21/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › que tienen una secuencia conocida de varios aminoácidos, p. ej. glutation.
PDF original: ES-2401965_T3.pdf
Fragmento de la descripción:
Campo de la invención [0001] La presente invención se refiere a los derivados del Factor VIII, los procesos para preparar dichos derivados y el 10 uso de dichos derivados en tratamientos.
Antecedentes de la invención [0002] El Factor VIII es una proteína importante en la cascada de coagulación sanguínea. Una deficiencia de Factor VIII
causa la enfermedad de la coagulación sanguínea hemofilia A. La hemofilia A se puede tratar mediante la administración de Factor VIII a un paciente cuando es necesario. El tratamiento profiláctico adecuado y efectivo de la hemofilia A con Factor VIII no es posible actualmente debido a que la vida media en plasma de Factor VIII es baja. Por lo tanto, es difícil mantener suficiente actividad de Factor VIII durante largos períodos de tiempo. Por lo tanto, la identificación de nuevos derivados de Factor VIII con vida media en plasma más larga podría ofrecer un tratamiento profiláctico adecuado y seguro para la hemofilia A.
A veces es posible aumentar la vida media en plasma de una proteína introduciendo fracciones químicas adecuadas que protejan la proteína en posiciones importantes para la eliminación de la proteína de la sangre. También puede ser ventajoso introducir fracciones químicas que actúan como grupos indicadores en una proteína. No obstante,
si tales fracciones químicas se introducen de forma no selectiva, entonces la actividad biológica de la proteína puede reducirse o destruirse. La introducción regioselectiva de fracciones químicas en proteínas es, por lo tanto, deseable. No obstante, es difícil conseguir la introducción regioselectiva de fracciones químicas en proteínas grandes, tales como el Factor VIII.
Por lo tanto, existe la necesidad de técnicas nuevas para la introducción regioselectiva de fracciones químicas en el Factor VIII.
Resumen de la invención [0005] Los presentes inventores han descubierto sorprendentemente que las enzimas de transglutaminasa se dirigen selectivamente a un número limitado de residuos de glutamina presentes en el Factor VIII. Así, el uso de una transglutaminasa en la síntesis de los derivados de Factor VIII permite la introducción regioselectiva de fracciones químicas en el Factor VIII. Estos métodos se han usado para preparar una nueva clase de derivados de Factor VIII.
Así, la presente invención se refiere a un derivado de Factor VIII de la fórmula (I) :
donde:
B representa un alquileno de C2 a C10; m representa 0 o un número entero de 1 a 19, n representa un número entero de 1 a 20, y la suma de m y n es de 1 a 20; P representa un mono o polirradical de Factor VIII obtenido por eliminación de los grupos de carbamoil m + n de las cadenas laterales de residuos de glutamina presentes en el Factor VIII; y
M representa una fracción (M1) que aumenta la vida media en plasma del derivado de Factor VIII o una fracción indicadora (M2) ;
o una sal derivada farmacéuticamente aceptable.
La invención además proporciona: 55 - una composición farmacéutica que comprende un derivado de Factor VIII, tal y como se ha definido anteriormente, y un portador o diluyente farmacéuticamente aceptable;
- un derivado de Factor VIII, tal y como se ha definido anteriormente, para su uso en el tratamiento del cuerpo humano o 5 animal mediante terapia;
- un derivado de Factor VIII, tal y como se ha definido anteriormente, para su uso en el tratamiento de la hemofilia A;
- uso de un derivado de Factor VIII, tal y como se ha definido anteriormente, en la producción de un medicamento para 10 el tratamiento de la hemofilia A;
- un método para tratar a un paciente con hemofilia A, este método comprende la administración a dicho paciente de un derivado de Factor VIII en una cantidad terapéuticamente eficaz, tal y como se ha definido anteriormente, o de una composición farmacéutica, tal y como se ha definido anteriormente;
- un derivado de Factor VIII de la fórmula (II) :
donde:
B representa un alquileno C2 a C10; q representa un número entero de 1 a 20 y P' representa un mono o polirradical de Factor VIII obtenido eliminando grupos de carbamoil q de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII,
o una sal derivada farmacéuticamente aceptable; 25
- un método para preparar un derivado de Factor VIII de la fórmula (II) , tal y como se ha definido anteriormente, este método comprende reaccionar Factor VIII con un compuesto de la fórmula (III) :
H2N-O-B-O-NH2 (III) 30 en presencia de una transglutaminasa, donde B es tal y como se ha definido anteriormente; y
- un método para preparar un derivado de Factor VIII de la fórmula (I) , tal y como se ha definido anteriormente, este
método comprende la reacción de un derivado de Factor VIII de la fórmula (II) , tal y como se ha definido anteriormente, 35 con un aldehído de la fórmula (IV) :
donde M es tal y como se ha definido anteriormente.
Descripción detallada de la invención [0008] La presente invención proporciona nuevos derivados de Factor VIII que portan sustituyentes a un número limitado de sitios en la proteína. La sustitución regioselectiva del Factor VIII se controla mediante el método de preparación. Un paso importante del método de la invención es el uso de la enzima transglutaminasa (TGase) . La 45 transglutaminasa también se conoce como proteína-glutamina-y-glutamiltransferasa. La transglutaminasa cataliza la reacción general:
El grupo -CH2-CH2-C (O) -NH2 de la proteína ilustrada anteriormente es la cadena lateral de un residuo de glutamina de la proteína.
Los presentes inventores han descubierto sorprendentemente que la transglutaminasa se dirige de forma selectiva a un número limitado de residuos de glutamina presentes en el Factor VIII. Las secuencias de los derivados de Factor VIII contienen 64-70 residuos de glutamina. No obstante, la transglutaminasa sólo se dirige a una minoría de estos residuos de glutamina. Típicamente, la transglutaminasa se dirige a 1-20 residuos de glutamina, preferiblemente de 1 a 15, más preferiblemente de 1 a 10 y de la forma más preferible de 1 a 7. De la forma más preferible, el derivado de FVIII es el compuesto de Factor VIII con el dominio B eliminado al que un péptido con la secuencia de SFSQNSRHPSQNPPVLKRHQR se fija al C-término de la cadena pesada. Este Factor VIII análogo tiene 66 residuos de glutamina. La transglutaminasa es la transglutaminasa de Streptomyces mobaraense y el número de residuos de glutamina previstos por la enzima está entre 1 y 20.
El primer paso del método de la presente invención implica la reacción del Factor VIII con un compuesto de dihidroxilamina de la fórmula (III) :
H2N-O-B-O-NH2 (III)
en presencia de una transglutaminasa. La transglutaminasa cataliza la reacción de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII con los grupos de amina en el compuesto de dihidroxilamina de la fórmula (III) , para dar un derivado de Factor VIII de la fórmula (II) :
donde: B representa un alquileno C2 a C10; q representa un número entero en el intervalo de 1 a 20 y
P' representa un mono o polirradical de Factor VIII obtenido por eliminación de los grupos de carbamoil q a partir de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII.
En una forma de realización B es -CH2 -CH2 -CH2-.
Como será evidente para un experto en la técnica, la formación del derivado de Factor VIII de la fórmula (II) implica la reacción de las cadenas laterales "q" de los residuos de glutamina presentes en el Factor VIII. Cada molécula de Factor VIII reacciona, por lo tanto, con moléculas "q" del compuesto de dihidroxilamina.
Típicamente, este paso de reacción se lleva a cabo en una solución acuosa, preferiblemente una solución acuosa 40 tamponada. Las soluciones tampón adecuadas son conocidas por los expertos en la técnica. La temperatura de dicha solución es típicamente de 0°C a 60°C, preferiblemente de 20°C a 40°C.
El número de residuos de glutamina modificados se pueden controlar por la concentración de cada uno de los reactivos que son, por un lado, FVIII o un análogo de FVIII y, por otro lado, el reactivo de bishidroxilamina. Asimismo, la 45 concentración de enzima (medida en actividad) y el origen de la transglutaminasa se pueden utilizar para controlar la extensión de la reacción, el sitio o sitios de modificación y la velocidad de reacción.
El producto bruto se purifica generalmente por técnicas conocidas, tales como el intercambio iónico y/o la ultrafiltración.
La segunda fase del método de la presente invención... [Seguir leyendo]
Reivindicaciones:
1. Derivado de Factor VIII de la fórmula (I) :
donde:
B representa un alquileno C2 a C10; m representa 0 o un número entero de 1 a 19, n representa un número entero de 1 a 20 y la suma de m y n es de 1 a 20; P representa un mono o polirradical de Factor VIII obtenido por eliminación de los grupos de carbamoil m + n a partir de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII; y M representa una fracción (M1) que aumenta la vida media en plasma del derivado de Factor VIII o una fracción indicadora (M2) ;
o una sal derivada farmacéuticamente aceptable.
2. Derivado de Factor VIII según la reivindicación 1, donde dicha fracción M1 comprende una o más fracciones de polietilenoglicol (PEG) , polipéptidos o ligantes de proteína plasmática.
3. Derivado de Factor VIII según la reivindicación 2, donde dicho péptido es albúmina o un anticuerpo o fragmento de la misma. 25
4. Derivado de Factor VIII según la reivindicación 2, donde dicho ligante de proteína plasmática es un ligante de albúmina.
5. Derivado de Factor VIII según la reivindicación 2, donde dicha fracción M1 comprende una fracción de polietilenoglicol 30 (PEG) .
6. Derivado de Factor VIII según la reivindicación 1, donde:
B representa un alquileno C2 a C4;
m representa 0 o un número entero de 1 a 5, n representa un número entero de 1 a 6 y la suma de m y n es de 1 a 6; y M representa una fracción (M1) que comprende una fracción de polietilenoglicol (PEG) y/o un ligante de albúmina.
7. Derivado de Factor VIII según la reivindicación 1, donde:
B representa un alquileno C2 a C4; m representa 0 o un número entero de 1 a 5, n representa un número entero de 1 a 6 y la suma de m y n es de 1 a 6 y
M representa una fracción (M2) que comprende biotina o un marcador fluorescente.
8. Derivado de Factor VIII según la reivindicación 6 o 7 donde B representa un alquileno C3.
9. Composición farmacéutica que comprende un derivado de Factor VIII tal y como se define en cualquiera de las 50 reivindicaciones precedentes y un portador o diluyente farmacéuticamente aceptable.
10. Derivado de Factor VIII tal y como se define en cualquiera de las reivindicaciones 1 a 8 para su uso en el tratamiento del cuerpo humano o animal mediante terapia.
11. Derivado de Factor VIII según la reivindicación 10 para su uso en el tratamiento de la hemofilia A.
12. Derivado de Factor VIII de la fórmula (II) :
donde:
B representa un alquileno C2 a C10; q representa un número entero de 1 a 20 y 10 P' representa un mono o polirradical de Factor VIII obtenido por eliminación de los grupos de carbamoil q a partir de las cadenas laterales de los residuos de glutamina presentes en el Factor VIII;
o una sal derivada farmacéuticamente aceptable.
13. Método para preparar un derivado de Factor VIII de la fórmula (II) tal y como se define en la reivindicación 12, este 15método comprende la reacción de Factor VIII con un compuesto de la fórmula (III) :
H2N-O-B-O-NH2 (III)
en presencia de una transglutaminasa, donde B es tal y como se define en cualquiera de las reivindicaciones 1 a 8. 20
14. Método según la reivindicación 13, donde la transglutaminasa es transglutaminasa de Streptomyces mobaraense.
15. Método para preparar un derivado de Factor VIII de la fórmula (I) , tal y como se define en cualquiera de las
reivindicaciones 1 a 8, que comprende la reacción de un derivado de Factor VIII de la fórmula (II) , tal y como se define 25 en la reivindicación 12, con un aldehído de la fórmula (IV) :
donde M es tal y como se define en cualquiera de las reivindicaciones 1 a 6 o 7.
Patentes similares o relacionadas:
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
PROCEDIMIENTO DE OBTENCIÓN DE SUBPRODUCTOS A PARTIR DE RESIDUOS DE CAFÉ Y APLICACIONES DE LOS MISMOS, del 13 de Julio de 2020, de UNIVERSIDAD DE GRANADA: Procedimiento de obtención de subproductos a partir de residuos de café y aplicaciones de los mismos. La presente invención consiste en un proceso […]
Biblioteca de péptidos y su uso, del 8 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Una biblioteca de péptidos que comprende una pluralidad de péptidos diferentes en la que los péptidos comprenden cada uno una secuencia de aminoácidos […]
Métodos para controlar la producción de proteasas, del 1 de Julio de 2020, de ROAL OY: Una célula hospedadora que comprende al menos un gen cromosómico inactivado en donde el gen cromosómico inactivado comprende una secuencia de ácido nucleico que codifica un […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Lipopéptidos de alta pureza, micelas de lipopéptidos y procesos para preparar los mismos, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina a partir de moléculas o agregados de alto peso molecular, en donde la daptomicina se proporciona en forma micelar, dicho […]
Proceso para la purificación de daptomicina, del 6 de Mayo de 2020, de Cubist Pharmaceuticals LLC: Un método para purificar daptomicina que comprende: a) someter a la daptomicina a condiciones en las que una solución micelar de daptomicina se forma alterando el pH; y […]
Métodos para ajustar los niveles de producción de carotenoides y composiciones en géneros de Rhodosporidium y Rhodotorula, del 15 de Abril de 2020, de TEMASEK LIFE SCIENCES LABORATORY LIMITED: Un método para ajustar el nivel de producción y la composición de carotenoides en un huésped fúngico que comprende: (a) manipular genéticamente […]