Intercambio de casete de región variable de inmunoglobulina.
Un método de modificación por ingeniería genética de un anticuerpo que conserva la especificidad de unión de unanticuerpo de referencia por un antígeno diana,
comprendiendo el método:
(a) obtener una región variable a partir del anticuerpo de referencia;
(b) reemplazar al menos un casete de intercambio, seleccionado entre el grupo que consiste en FR1-CDR1,FR1-FR2-CDR1, FR2-CDR2-FR3 y CDR2-FR3 de la región variable del anticuerpo de referencia con unabiblioteca de casetes de intercambio correspondientes a partir de segmentos V humanos, generando de esemodo una biblioteca de regiones V híbridas que comprenden miembros en los cuales el al menos un casete deintercambio de la región variable del anticuerpo de referencia se reemplaza con casetes de intercambiocorrespondientes humanos codificados por diferentes genes, donde la CDR del al menos un casete deintercambio de la región variable del anticuerpo de referencia es una CDR intacta o una CDR parcial que esuna subregión de la CDR que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDRintacta y cada región flanqueante (FR) del al menos un casete de intercambio de la región variable delanticuerpo de referencia es una FR intacta o una FR parcial que es al menos el 30%, el 40%, el 50%, el 60%,el 70%, el 80% o el 90% de la FR intacta;
(c) emparejar la biblioteca de regiones V híbridas de (b) con una región V complementaria; y
(d) seleccionar un anticuerpo que comprende una región V híbrida que tiene al menos un casete intercambiadogenerado en la etapa (b) que tiene una afinidad de unión por el antígeno diana.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/041825.
Solicitante: KaloBios Pharmaceuticals, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 260 E. Grand Avenue South San Francisco, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BEBBINGTON,CHRISTOPHER,R, YARRANTON,GEOFFREY,T, LUEHRSEN,KENNETH R.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C12N5/06
- C12P21/06 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- C40B40/10 C […] › C40 TECNOLOGIA COMBINATORIA. › C40B QUIMICA COMBINATORIA; BIBLIOTECAS, p. ej. QUIMIOTECAS (bibliotecas combinatorias in silico de ácidos nucleicos, proteínas o péptidos G16B 35/00; química combinatoria in silico G16C 20/60). › C40B 40/00 Bibliotecas per se , p. ej. arrays, mezclas. › Bibliotecas que contienen péptidos o polipéptidos, o sus derivados.
PDF original: ES-2429541_T3.pdf
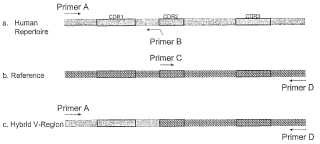
Fragmento de la descripción:
Intercambio de casete de región variable de inmunoglobulina
Antecedentes de la invención Los restos de unión a antígeno de anticuerpos comprenden típicamente dos dominios de inmunoglobulina, un dominio de cadena variable pesada (VH) y un dominio de cadena variable ligera (VL) . Cada dominio tiene tres bucles de secuencia variable que forman las regiones determinantes de complementariedad (CDR) . Las seis CDR (tres de VH y tres de VL) se extienden desde una cara de la estructura de región variable para formar el sitio de unión a antígeno. En la mayoría de los anticuerpos, la asociación apropiada de las dos cadenas es necesaria para unir antígeno con afinidad significativa. Por tanto un dominio VH y uno VL juntos forman la unidad de unión a antígeno mínima.
Se ha hecho uso extendido de anticuerpos monoclonales, particularmente aquellos obtenidos a partir de roedores incluyendo ratones. Sin embargo, estos generan con frecuencia una respuesta inmune en el uso clínico humano (por ejemplo, Miller, R.A. et al., Blood 62: 988-995 (1983) ; Schroff, R.W. et al., Cancer Res. 45: 879-885 (1985) ) . La técnica ha intentado superar este problema construyendo anticuerpos “quiméricos” en los cuales un dominio variable de unión a antígeno animal se acopla a un dominio constante humano (Patente de Estados Unidos Nº 4.816.567; Morrison, S.L. et al., Proc. Natl. Acad. Sci. USA 81: 6851-6855 (1984) ; Boulianne, G.L. et al., Nature 312: 643-646 (1984) ; Neuberger, M.S. et al., Nature 314: 268-270 (1985) ) .
En un esfuerzo adicional para minimizar el uso de secuencias heterólogas en anticuerpos humanos, se han descrito varios enfoques de humanización (por ejemplo, Jones, P.T. et al., Nature 321: 522-525 (1986) ; Riechmann, L. et al., 25 Nature 33-2: 323-327 (1988) ; Verhoeyen, M. et al., Science 239: 1534-1536 (1988) ; Queen et al, Proc Natl Acad Sci USA. 86: 10029-33 (1989) ; Patentes de Estados Unidos Nº 5.693.762 y 5.585.089) . En tales técnicas, las CDR de una inmunoglobulina donadora se insertan en un armazón humano. Típicamente, los restos adicionales en los armazones del anticuerpo aceptor humano también se sustituyen con restos de roedor para conservar la conformación nativa de las CDR de roedor necesarias para recuperar la actividad de unión completa. Por tanto, los anticuerpos humanizados con frecuencia conservan seis CDR del anticuerpo de roedor y varios restos de roedor adicionales en las regiones flanqueantes. Mediante la transferencia de seis CDR desde el anticuerpo de roedor hasta armazones humanos, la especificidad del anticuerpo de partida típicamente se conserva en el anticuerpo humanizado pero la afinidad del anticuerpo humanizado está, en muchos casos, reducida en comparación con el anticuerpo de partida. Por consiguiente, pueden ser necesarias varias repeticiones de los procesos de humanización, en los cuales se construyen y ensayan combinaciones alternativas de retro-mutaciones en las regiones flanqueantes, con el fin de obtener afinidades de unión adecuadas. Incluso después de múltiples repeticiones, no siempre es posible identificar anticuerpos con CDR injertada con afinidades equivalentes al anticuerpo de partida.
Los anticuerpos humanos también se han aislado in vitro mediante expresión de repertorios de genes de anticuerpo en sistemas de expresión microbiana. Existen varias tecnologías de presentación en las cuales los fragmentos de anticuerpo expresados se presentan como proteínas de fusión ancladas a la superficie de una célula microbiana o un bacteriófago. El fago o célula hospedadora sirve como un paquete de presentación genética replicable (rgdp, por sus siglas en inglés) y los rgdp que se unen a un antígeno especificado se pueden seleccionar y expandir en cultivo 45 para aislar genes que codifican anticuerpos frente al antígeno seleccionante. Los fragmentos de anticuerpo se pueden aislar de esta manera a partir de la expresión en la superficie de levadura (Feldhaus et al, Nat. Biotechnol. 21: 163-70, 2003) , células bacterianas (Daugherty et al., Protein Eng. 12: 613-21, 1999) o, más comúnmente, en fagos. La presentación en fago permite explorar bibliotecas combinatorias grandes para determinar anticuerpos de unión a antígeno raros (Hoogenboom y Winter, J. Mol. Biol. 227: 381, 1992; Marks et al., J Mol Biol. 222: 581, 1991; Winter et al., Annu Rev. Immunol. 12: 433-55, 1994) . Las bibliotecas combinatorias grandes de agentes de unión potenciales se pueden crear a partir de dos bibliotecas más pequeñas para selección de la combinación deseada. Por ejemplo, se puede crear y presentar en un bacteriófago una primera biblioteca de 107 cadenas H. Una segunda biblioteca de 107 cadenas L, en la cual las secuencias codificantes de estas cadenas ligeras están dentro de un vector de plásmido, se expresan en el espacio periplásmico de una bacteria 55 hospedadora. Las bibliotecas de cadena H y cadena L se combinan para proporcionar 1014 combinaciones de cadenas H y L en la superficie del fago resultante en el sobrenadante bacteriano.
En la técnica se conocen diversos métodos para aumentar la diversidad en bibliotecas de fago-anticuerpo. Un método de este tipo implica combinar surtidos aleatorios de secuencias de CDR codificadas por línea germinal en un conjunto de regiones flanqueantes humanas con el fin de generar bibliotecas artificiales de anticuerpos humanos (“combinación de CDR”) . Véase, por ejemplo, Jirholt et al., Gene 215: 471, 1998; Soderlind et al., Nat. Biotechnol. 18: 852-6, 2000) .
La presentación en fago también se puede usar para identificar anticuerpos humanos con la especificidad de unión 65 de un anticuerpo de roedor mediante un proceso de dos etapas de selección guiada en el cual una biblioteca de cadenas VL humanas se empareja con la cadena VH del anticuerpo de roedor y se seleccionan anticuerpos medio humanos para unión a antígeno. Las cadenas humanas identificadas posteriormente se emparejan con una biblioteca de cadenas VH humanas con el fin de identificar pares VH -VL capaces de unirse a antígeno (por ejemplo, Patente de Estados Unidos Nº 5.565.332; Jespers, et al., Bio/Technology 12: 899-903, 1994; Beiboer et al., J Mol Biol. 296: 833-49, 2000) . En algunos casos la CDR3 de cadena pesada del anticuerpo de roedor se conserva en la selección guiada (Klimka et al., Br J Cancer 83: 252-60, 2000) . En otros casos, tanto la CDRH3 como la CDRL3 del anticuerpo de roedor se conservan en el anticuerpo humanizado final después de selección guiada (por ejemplo, Rader et al., Proc. Natl. Acad. Sci USA 95: 8910-5, 1998) .
En todos estos casos se usan típicamente bibliotecas grandes de diversidad elevada con el fin de identificar anticuerpos con afinidades elevadas. Los anticuerpos humanos obtenidos a partir de las tecnologías en la técnica, por lo tanto, tienden a tener un número significativo de diferencias de aminoácidos con respecto a la secuencia de línea germinal más cercana. Tal mutación somática contribuye a la generación de anticuerpos de afinidad elevada en anticuerpos naturales (por ejemplo, England et al., J. Immunol. 162: 2129, 1999) y generalmente se ha considerado importante para la generación de anticuerpos de afinidad elevada en anticuerpos generados a partir
de bibliotecas in vitro. Sin embargo, tales mutaciones generan nuevas secuencias de proteína que se pueden reconocer como extrañas por el sistema inmune del organismo. Se espera que el sistema inmune no sea sensible (que sea “tolerante”) a inmunoglobulinas expresadas de forma general durante el desarrollo, es decir, secuencias encontradas en la forma no mutada de línea germinal, pero las mutaciones en estas secuencias pueden permitir que el sistema inmune identifique a estas como proteínas extrañas. Por tanto se puede esperar que los anticuerpos con numerosas diferencias con respecto a las secuencias de línea germinal sean inmunogénicos cuando se usan de forma terapéutica en seres humanos.
Por lo tanto existe una necesidad de métodos mejorados para humanizar anticuerpos de roedor con el fin de reducir adicionalmente el potencial de inmunogenicidad mientras que se conserva la especificidad y afinidad de unión del
anticuerpo de partida. Existe también una necesidad de métodos para identificar anticuerpos humanos con la especificidad de un anticuerpo de referencia de partida, por ejemplo, un anticuerpo de ratón, pero que utilizan secuencias de inmunoglobulina humanas que son de línea germinal o cercanas a línea germinal. La invención aborda esta necesidad.
La invención proporciona además soluciones a problemas de fiabilidad inherente en tecnologías de humanización de anticuerpo que incluyen selección guiada por cadena e injerto de CDR. Las tecnologías de injerto de CDR proporcionan anticuerpos con... [Seguir leyendo]
Reivindicaciones:
1. Un método de modificación por ingeniería genética de un anticuerpo que conserva la especificidad de unión de un anticuerpo de referencia por un antígeno diana, comprendiendo el método: 5
(a) obtener una región variable a partir del anticuerpo de referencia;
(b) reemplazar al menos un casete de intercambio, seleccionado entre el grupo que consiste en FR1-CDR1, FR1-FR2-CDR1, FR2-CDR2-FR3 y CDR2-FR3 de la región variable del anticuerpo de referencia con una biblioteca de casetes de intercambio correspondientes a partir de segmentos V humanos, generando de ese modo una biblioteca de regiones V híbridas que comprenden miembros en los cuales el al menos un casete de intercambio de la región variable del anticuerpo de referencia se reemplaza con casetes de intercambio correspondientes humanos codificados por diferentes genes, donde la CDR del al menos un casete de intercambio de la región variable del anticuerpo de referencia es una CDR intacta o una CDR parcial que es una subregión de la CDR que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR
intacta y cada región flanqueante (FR) del al menos un casete de intercambio de la región variable del anticuerpo de referencia es una FR intacta o una FR parcial que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la FR intacta;
(c) emparejar la biblioteca de regiones V híbridas de (b) con una región V complementaria; y
(d) seleccionar un anticuerpo que comprende una región V híbrida que tiene al menos un casete intercambiado generado en la etapa (b) que tiene una afinidad de unión por el antígeno diana.
2. El método de la reivindicación 1, comprendiendo además:
(e) reemplazar un segundo casete de intercambio, que comprende al menos una CDR o una CDR parcial que es una subregión de la CDR que es al menos el 30%, el 40%, el 50%, el 60% , el 70%, el 80% o el 90% de la CDR intacta, unida a al menos una región flanqueante (FR) o una FR parcial que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la FR intacta que están juntas de forma natural, de la región V del anticuerpo de referencia con una biblioteca de casetes de intercambio correspondientes a partir de segmentos de genes V humanos para crear una segunda biblioteca híbrida de regiones V híbridas;
(f) emparejar la segunda biblioteca de regiones V híbridas con una región V complementaria;
(g) seleccionar un anticuerpo que comprende una segunda región V híbrida, anticuerpo que tiene una afinidad de unión por el antígeno diana; y
(h) combinar el casete de intercambio humano del anticuerpo modificado por ingeniería genética de (d) con el segundo casete de intercambio humano del anticuerpo de (g) , para obtener un anticuerpo con la especificidad
de unión del anticuerpo de referencia, donde el anticuerpo tiene una región V híbrida que comprende al menos dos casetes de intercambio humanos.
3. El método de la reivindicación 2, comprendiendo además una etapa de reemplazo de la CDR3-FR4 de la región V híbrida con una biblioteca de regiones CDR3-FR4, emparejar la región variable con una región variable complementaria y seleccionar un anticuerpo que conserve la especificidad de unión por el antígeno diana.
4. El método de la reivindicación 2, comprendiendo además una etapa de reemplazo de la FR4 de la región V híbrida con una biblioteca de secuencias FR4.
5. El método de una cualquiera de las reivindicaciones 1 a 4, donde al menos una de las CDR del casete de intercambio de (b) o (e) es una secuencia de CDR parcial que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR intacta o donde al menos una de las FR del casete de intercambio de (b) o (e) es una secuencia de FR parcial que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la FR intacta.
6. El método de una cualquiera de las reivindicaciones 1 a 5, donde la región V complementaria de (c) o (f) tiene un segmento V de origen natural o tiene un segmento V de línea germinal o es una región V híbrida o es una región V híbrida que es un miembro de una biblioteca que comprende diferentes regiones V híbridas.
7. Un método de modificación por ingeniería genética de un anticuerpo que conserva la especificidad de unión de un 55 anticuerpo de referencia por un antígeno diana, comprendiendo el método:
(a) obtener una región variable de un anticuerpo de referencia que tiene una especificidad de unión deseada;
(b) reemplazar la FR1-CDR1-FR2 de la región variable del anticuerpo de referencia con una biblioteca de regiones FR1-CDR1-FR2 humanas para crear una biblioteca de regiones variables híbridas, emparejar las regiones variables híbridas con una región variable complementaria y seleccionar un anticuerpo que tenga una afinidad detectable por el antígeno diana;
(c) reemplazar la FR2-CDR2-FR3 de la región variable del anticuerpo de referencia con una biblioteca de regiones FR2-CDR2-FR3 humanas para crear una biblioteca de regiones variables híbridas, emparejar las regiones variables híbridas con una región variable complementaria y seleccionar un anticuerpo que tenga una
afinidad detectable por el antígeno diana; y
(d) combinar la FR1-CDR1-FR2 de la región variable híbrida del anticuerpo seleccionado en (b) con la FR2CDR2-FR3 de la región variable híbrida del anticuerpo seleccionado en (c) para obtener un anticuerpo con un segmento V de región variable humano, anticuerpo que tiene la especificidad de unión del anticuerpo de referencia.
8. El método de la reivindicación 7, donde (b) y (c) se llevan a cabo de forma secuencial.
9. El método de la reivindicación 7 u 8, donde la región variable complementaria de (b) o (c) comprende un segmento V de origen natural o es una región V híbrida o tiene un segmento V de línea germinal o es un miembro de una biblioteca de regiones V híbridas.
10. El método de una cualquiera de las reivindicaciones precedentes, donde la región variable del anticuerpo de referencia es una región variable de cadena pesada.
11. El método de una cualquiera de las reivindicaciones 1 a 9, donde la región variable del anticuerpo de referencia 15 es una región variable de cadena ligera.
12. El método de la reivindicación 7 u 8, donde la combinación de la FR1-CDR1-FR2 con la FR2-CDR2-FR3 comprende combinar las regiones FR2 en una región de homología.
13. El método de la reivindicación 7 u 8, donde la combinación de la FR1-CDR1-FR2 con la FR2-CDR2-FR3 comprende reemplazar la FR2 de FR1-CDR1-FR2 con la FR2 de FR2-CDR2-FR3 o reemplazar la FR2 de FR2-CDR2 FR3 con la FR2 de FR1-CDR1-FR2.
14. El método de la reivindicación 7 u 8, comprendiendo además una etapa de reemplazo de la CDR3-FR4 de la
región variable híbrida con una biblioteca de regiones CDR3-FR4 humanas, emparejar la región variable con una región variable complementaria y seleccionar un anticuerpo que se une al antígeno diana.
15. El método de la reivindicación 14, donde las regiones CDR3 de la biblioteca de regiones CDR3-FR4 humanas son regiones CDR3 parciales que son al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR3 intacta.
16. El método de la reivindicación 7 u 8, comprendiendo además:
(e) reemplazar la FR3-CDR3-FR4 de la región variable que comprende el segmento V humano de (d) con una biblioteca de regiones FR3-CDR3-FR4, emparejar la región variable con una región variable complementaria y seleccionar un anticuerpo que tiene una afinidad detectable por el antígeno diana; y
(f) combinar la FR3-CDR3-FR4 de la región variable híbrida del anticuerpo seleccionado en (e) con la FR2CDR2-FR3 de la región variable híbrida del anticuerpo seleccionado en (d) para obtener un anticuerpo con un segmento V de región variable humano, anticuerpo que tiene la especificidad de unión del anticuerpo de referencia.
17. El método de la reivindicación 7 u 8, donde las regiones FR1-CDR1-FR2 humanas y/o las regiones FR2-CDR2-FR3 humanas son de línea germinal.
18. Un método para modificar por ingeniería genética un anticuerpo que conserva la especificidad de unión de un anticuerpo de referencia por un antígeno diana, comprendiendo el método:
(a) obtener una región variable de un anticuerpo de referencia que tiene una especificidad de unión deseada;
(b) reemplazar la FR1-CDR1-FR2 de la región variable del anticuerpo de referencia con una biblioteca de regiones FR1-CDR1-FR2 humanas para crear una biblioteca de regiones variables híbridas, emparejar las regiones variables híbridas con una región variable complementaria y seleccionar un anticuerpo que tenga una afinidad detectable por el antígeno diana;
(c) reemplazar la CDR2-FR3 de la región variable del anticuerpo de referencia con una biblioteca de regiones CDR2-FR3 humanas para crear una biblioteca de regiones variables híbridas, donde la CDR2 de la CDR2-FR3
del anticuerpo de referencia es una CDR2 parcial que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR2 intacta y la biblioteca de secuencias CDR2-FR3 humanas comprende secuencias CDR2-FR3 parciales correspondientes, emparejar las regiones variables híbridas con una región complementaria y seleccionar un anticuerpo que tenga una afinidad detectable por el antígeno diana; y
(d) combinar la FR1-CDR1-FR2 de la región variable del anticuerpo seleccionado en (b) con la CDR2-FR3 de la región variable híbrida del anticuerpo seleccionado en (c) para obtener un anticuerpo con un segmento V de región variable humano, anticuerpo que tiene la especificidad de unión del anticuerpo de referencia.
19. El método de la reivindicación 18, comprendiendo además una etapa de reemplazo de la CDR3-FR4 del
anticuerpo de referencia con una biblioteca de regiones CDR3-FR4 humanas, emparejar la región variable con una 65 región variable complementaria y seleccionar un anticuerpo que se une al antígeno diana.
20. El método de la reivindicación 19, donde las regiones CDR3 de la biblioteca de regiones CDR3-FR4 humanas son regiones CDR3 parciales que son al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR3 intacta.
21. El método de la reivindicación 18, comprendiendo además:
(e) reemplazar la FR4 de la región variable del anticuerpo de referencia con una biblioteca de regiones FR4, emparejar la región variable con una región variable complementaria y seleccionar un anticuerpo que tiene una afinidad detectable por el antígeno diana.
22. El método de la reivindicación 18, donde las regiones FR1-CDR1-FR2 humanas y/o las regiones CDR2-FR3 humanas son de línea germinal.
23. El método de una cualquiera de las reivindicaciones precedentes, donde el anticuerpo es un fragmento Fv, un 15 Fab, un Fab', un F (ab') 2 o un scFv.
24. El método de una cualquiera de las reivindicaciones precedentes, donde los anticuerpos se expresan y secretan en forma soluble a partir de una célula hospedadora y se unen a un antígeno.
25. El método de una cualquiera de las reivindicaciones 1 a 23, donde los anticuerpos se presentan en la superficie de una célula, una espora o un virus.
26. Una biblioteca de regiones V híbridas que comprende miembros que tienen una diversidad de regiones V, donde un miembro tiene al menos una subsecuencia determinante de especificidad de unión esencial mínima (MEBSD) de 25 una CDR a partir de un anticuerpo de referencia y al menos un casete de intercambio a partir de un repertorio de anticuerpo, casete de intercambio que se selecciona entre el grupo que consiste en FR1-CDR1, FR1-FR2-CDR1, FR2-CDR2-FR3 y CDR2-FR3 donde la CDR del casete de intercambio es una CDR intacta o una CDR parcial que es una subregión de la CDR que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la CDR intacta y en cada región flanqueante (FR) existe una FR intacta o una FR parcial que es una subregión de la FR que es al menos el 30%, el 40%, el 50%, el 60%, el 70%, el 80% o el 90% de la FR intacta.
27. La biblioteca de la reivindicación 26, donde el miembro de la biblioteca tiene al menos dos casetes de intercambio de un repertorio humano.
28. La biblioteca de la reivindicación 26, donde el casete de intercambio es una secuencia de línea germinal humana.
29. La biblioteca de la reivindicación 26, donde la MEBSD es de la CDR3 del anticuerpo de referencia.
30. La biblioteca de la reivindicación 29, donde el miembro de la biblioteca tiene una CDR3 del anticuerpo de referencia.
31. La biblioteca de la reivindicación 30, donde el miembro tiene una CDR3 del anticuerpo de referencia y una FR4
humana. 45
32. La biblioteca de la reivindicación 30, donde el miembro tiene una CDR3 en la que el segmento D es del anticuerpo de referencia.
Patentes similares o relacionadas:
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Composición para el tratamiento de enfermedades isquémicas o trastornos inflamatorios neurogénicos, que contienen el secretoma de células progenitoras neurales como ingrediente activo, del 22 de Julio de 2020, de S-BIOMEDICS: Una composición para uso en el tratamiento de enfermedad cerebrovascular isquémica, cardiopatía isquémica, infarto de miocardio, enfermedad de Alzheimer, enfermedad […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Combinación de anticuerpo anti-CD20 e inhibidor selectivo de PI3 quinasa, del 15 de Julio de 2020, de TG Therapeutics Inc: Un metodo in vitro para inhibir la proliferacion de una poblacion celular que comprende poner en contacto la poblacion con una combinacion que comprende […]