Proteínas inmunogénicas de la membrana externa derivada de genoma de leptospira y composiciones y métodos basados en las mismas.
Un vector capaz de expresar ADN recombinante, en el que el ADN recombinante se selecciona del grupo queconsiste en:
(i) un ADN recombinante que codifica una proteína que tiene la secuencia de aminoácidos como se muestra enSEQ ID NO: 2 (LP 1454),
(ii) un ADN recombinante que codifica un epítopo inmunogénico o fragmento inmunológicamente activo de laproteína de (i) anterior, y
(iii) un ADN recombinante que codifica un fragmento de proteína que tiene una longitud de al menos 10%, 20%,30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopoinmunogénico o fragmento inmunológicamente activo de (ii) anterior; y
en el que el ADN recombinante se inserta en el vector de manera que se expresa una proteína recombinante cuandoel vector se proporciona en un huésped apropiado, para uso como una vacuna de ADN recombinante en un métodode vacunación.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/077182.
Solicitante: CORNELL UNIVERSITY .
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 395 PINE TREE ROAD SUITE 310 ITHACA, NY 14850 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHANG, YUNG-FU.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/20 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Spirochaetales (O), p. ej. Treponema, Leptospira.
PDF original: ES-2395548_T3.pdf
Fragmento de la descripción:
Proteínas inmunogénicas de la membrana externa derivada de genoma de leptospira y composiciones y métodos basados en las mismas.
1. CAMPO TÉCNICO
La presente invención se refiere a proteínas de membrana externa de Leptospira (OMPs = Outer Membrane Proteins) y a los anticuerpos dirigidos contra ellas. La invención también se refiere a métodos y composiciones para el tratamiento de enfermedades, trastornos o desordenes provocados por un patógeno de Leptospira inmunogénico transportado por la sangre, que comprende administrar anticuerpos que se unen a OMPs. La invención además se refiere a métodos para utilizar OMPs de Leptospira como vacunas o antígenos de diagnóstico.
2. ANTECEDENTES
Las especies de Leptospira son una espiroqueta gram negativa, el agente causante de leptospisoris, una enfermedad zoonótica de mamíferos, caracterizada por fallo renal y hepático, aborto, uveitis, fallo reproductor, miocarditis, mastitis y hemorragia pulmonar (Kishimoto, et al. 2004. Leptospirosis misdiagnosed as pulmonar y -renal syndrome. Am. J. Med. Sci. 328:1 16-120; Marotto, et al. 1999. Acute lung injur y in leptospirosis: clinical and laborator y features, outcome, and factors associated with mortality. Clin. Infect. Dis. 29:1561-1563; Seijo, et al. 2002. Lethal leptospiral pulmonar y hemorrhage: an emerging disease in Buenos Aires, Argentina. Emerg. Infect. Dis. 8: 1004-1005; Trevejo, et al. 1998. Epidemic leptospirosis associated with pulmonar y hemorrhage-Nicaragua, 1995. J. Infect. Dis. 178:1457-1463; Vinetz, J. M. 2001. Leptospirosis. Curr. Opin. Infect. Dis. 14:527-538) .
Aunque hay 21 genomoespecies de Leptospira, la causa más común de leptospirosis entre el ganado, especialmente en ganado lechero en los E.U.A., es L. borgpetersenii serovar Hardjo, y L. interrogans serovar Pomona (Talpada, M. D., N. Garvey, R. Sprowls, A. K. Eugster, and J. M. Vinetz. 2003. Prevalence of leptospiral infection in Texas cattle: implications for transmission to humans. Vector Borne Zoonotic Dis. 3: 141-147) . M. Vinetz. 2003. 2003. Prevalence of leptospiral infection in Texas cattle: implications for transmission to humans. Vector Borne Zoonotic Dis. 3: 141-147) . El ganado actúa como el hospedero de mantenimiento para esta infección y en ganado crónicamente infectado, las leptospiras persisten en los riñones y tracto genital, conduciendo a aborto (Ellis, W. A., and S. W. Michna. 1976. Bovine leptospirosis: demonstration of leptospires of the Hebdomadis serogroup in aborted fetuses and a premature calf. Vet. Rec. 99:430-432; Ellis, W. A., J. J. O'Brien, D. G. Br y son, and D. P. Mackie. 1985. Bovine leptospirosis: some clinical features of serovar Hardjo infection. Vet. Rec. 117:101-104) y falla renal (Masri, S. A., P. T. Nguyen, S. P. Gale, C. J. Howard, and S. C. Jung. 1997. A polymerase chain reaction assay for the detection of Leptospira spp. in bovine semen. Can. J. Vet. Res. 61:15-20) . Las especies de Leptospira también infectan a cerdos, caballos, perros y humanos (Palaniappan, R.U.M.; Ramanujam, S.; Chang, Y-F. (2007) Leptospirosis: pathogenesis, immunity, and diagnosis. Curr. Opin. Infect. Dis. 20 (3) : 284-292) . Los animales infectados también pueden sobrevivir en forma asintomático al excretar las espiroquetas en forma intermitente en la orina, afectando eventualmente a los otros animales sanos.
El diagnóstico de leptospirosis depende de una prueba serológica estándar, la prueba de aglutinación microscópica (MAT = Microscopic Agglutination Test) . Sin embargo, MAT es consumidora de tiempo, laboriosa y carece de sensibilidad para detectar la infección en una etapa temprana. Pruebas serológicas para diagnóstico tales como ensayo de tiras reactivas, ensayo de hemaglutinación indirecta y ensayo de inmunoabsorción con enzimas ligadas (ELISA = Enzyme Linked Immunosorbent Assay) , son métodos alternos para rápido diagnóstico, pero solo pocos ensayos se han evaluados sistemáticamente con base en los títulos de MAT (Palaniappan, et al. 2004. Expression of leptospiral immunoglobulin-like protein by Leptospira interrogans and evaluation of its diagnostic potential in a kinetic ELISA. J. Med. Microbiol. 53:975-984) . Esta información es crucial para muchos laboratorios de diagnóstico para elegir el ensayo conveniente para diagnóstico de leptospirosis.
Vacunas monovalentes o pentavalentes comercialmente disponibles proporcionan solo inmunidad a corto plazo y son ineficaces contra serovares de Leptospira. Recientemente, una nueva vacuna que contiene proteínas de células enteras del serovar Hardjo de L. borgpetersenii se ha encontrado que protege incluso la transmisión de infección de madre a feto en ganado (Ribeiro, M. A., C. C. Souza, and S. H. Almeida. 1995. Dot-ELISA for human leptospirosis employing immunodominant antigen. J. Trop. Med. Hyg. 98:452-456; Smith, C. R., P. J. Ketterer, M. R. McGowan, and B. G. Corney. 1994. A review of laborator y techniques and their use in the diagnosis of Leptospira interrogans serovar Hardjo infection in cattle. Aust. Vet. J. 71:290- 294) . En forma notable, estas vacunas incrementan el título de anticuerpo contra antígenos leptospirales en animales, y este aumento no puede ser diferenciado por la prueba de aglutinación microscópica (MAT) estándar. Además, si estos animales vacunados también se someten a infección de otros serovares de Leptospira, es imposible distinguir vacunación de infección utilizando MAT.
Por lo tanto hay necesidad en la técnica para una vacuna para leptospirosis. Hay también necesidad por distinguir vacunación de leptospirosis de infección.
La cita o identificación de cualquier referencia en la Sección 2, o en cualquier otra sección de esta solicitud, no habrá de considerarse como una admisión de que dicha referencia está disponible como técnica previa para la presente invención.
3. COMPENDIO DE LA INVENCIÓN
La proteína de membrana externa de Leptospira (OMP) rLP1454 (SEQ ID NOS: 1-2) , se proporciona, que puede servir como herramienta para desarrollar vacunas efectivas o métodos de diagnóstico para leptospirosis. En una modalidad, se proporcionan fragmentos de proteína de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%
o 95% de longitud de la secuencia de aminoácidos de cualquiera de los anteriores.
Las propiedades antigénicas de OMP de Leptospira LP1454 pueden emplearse para crear, fabricar o mejorar vacunas. Vacunas, incluyendo pero no limitadas a vacunas de ADN, vacunas recombinantes y vacunas de epítopo de célula T con base en las OMPs anteriores, además se proporcionan. Métodos para producir estas vacunas, también se proporcionan.
En una modalidad, la vacuna se basa en la proteína de membrana externa de Leptospira (OMP) rLP1454 (SEQ ID NOS: 1-2)
Se proporcionan métodos para utilizar los genes OMP de Leptospira, proteínas y anticuerpos, para técnicas de diagnóstico serológico.
Un plásmido también se proporciona que comprende un ADN recombinante que codifica una OMP LP1454 o un epítopo de su variante conservada, o un fragmento péptido inmunológicamente reactivo de la misma.
También se proporciona un vector de expresión.
También se proporcionan epítopos inmunogénicos de OMP de Leptospira , o un epítopo de una variante conservada de la misma, o un fragmento péptido inmunológicamente reactivo de la misma.
Se proporcionan métodos para utilizar el epítopo inmunogénico (por ejemplo, un epítopo de célula T) como una vacuna (o para mejorar una vacuna) para mamíferos, incluyendo pero no limitados a vacas, cerdos, perros, ovejas y caballos.
También se proporcionan métodos para utilizar el epítopo inmunogénico (por ejemplo, un epítopo de célula T) como un antígeno de diagnóstico serológico. En un aspecto, el epítopo se reconoce específicamente por un anticuerpo.
También se proporcionan formulaciones de vacuna para administración farmacológica.
Formulaciones de vacuna pueden ser formulaciones de vacuna de ADN, formulaciones de vacuna recombinante o formulaciones de vacuna de epítopo de célula T.
También se proporcionan anticuerpos aislados y purificados de OMP de Leptospira LP1454, o a un epítopo inmunogénico (por ejemplo, un epítopo de célula T) , epítopo de una variante conservada o su fragmento péptido inmunológicamente reactivo. Estos anticuerpos incluyen, pero no están limitados a anticuerpos policlonales, anticuerpos monoclonales (mAbs) , anticuerpos humanos, humanizados o quiméricos, anticuerpos de cadena sencilla, fragmentos Fab, fragmentos F (ab') 2, fragmentos producidos por una biblioteca de expresión Fab, anticuerpos anti-idiotípicos (anti-Id) y fragmentos de enlace de epítopo de cualquiera de los anteriores.
En una modalidad, un anticuerpo... [Seguir leyendo]
Reivindicaciones:
1. Un vector capaz de expresar ADN recombinante, en el que el ADN recombinante se selecciona del grupo que consiste en:
(i) un ADN recombinante que codifica una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP 1454) ,
(ii) un ADN recombinante que codifica un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un ADN recombinante que codifica un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior; y
en el que el ADN recombinante se inserta en el vector de manera que se expresa una proteína recombinante cuando el vector se proporciona en un huésped apropiado, para uso como una vacuna de ADN recombinante en un método de vacunación.
2. Un método para producir una vacuna frente a un trastorno relacionado con Leptospira que comprende:
a) proporcionar un ADN recombinante, en el que el ADN recombinante se selecciona del grupo que consiste en:
(i) un ADN recombinante que codifica una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP 1454) , (ii) un ADN recombinante que codifica un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un ADN recombinante que codifica un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i)
o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior;
b) proporcionar un vector capaz de expresar el ADN recombinante cuando el ADN recombinante se inserta en el vector, e c) insertar el ADN recombinante en el vector, en el que el ADN recombinante se inserta en el vector de manera que se expresa una proteína recombinante cuando el vector se proporciona en un huésped apropiado.
3. Un método para producir una vacuna frente a un trastorno relacionado con Leptospira que comprende:
a) proporcionar un ADN recombinante, en el que el ADN recombinante se selecciona del grupo que consiste en:
(i) un ADN recombinante que codifica una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP 1454) , (ii) un ADN recombinante que codifica un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un ADN recombinante que codifica un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i)
o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior;
b) construir un vector de expresión que comprende un plásmido, en el que el plásmido comprende el ADN recombinante; e c) inocular un huésped con el vector de expresión, en el que el ADN recombinante se expresa en el huésped para producir una proteína recombinante y en el que la proteína expresada incita una respuesta inmune en el huésped.
4. Una vacuna que comprende una proteína recombinante, en la que la proteína recombinante se selecciona del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP 1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de anteriormente, para uso como una vacuna recombinante en un método de vacunación.
5. Un método para producir una vacuna frente a un trastorno relacionado con Leptospira que comprende:
a) proporcionar un ADN recombinante, en el que el ADN recombinante se selecciona del grupo que consiste en:
(i) un ADN recombinante que codifica una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP 1454) , (ii) un ADN recombinante que codifica un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un ADN recombinante que codifica un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i)
o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior;
b) proporcionar un vector capaz de expresar el ADN recombinante cuando el ADN recombinante se inserta en el vector; c) insertar el ADN recombinante en el vector, d) proporcionar una cepa bacteriana; e) transformar el vector en la cepa bacteriana de manera que se expresa una proteína recombinante cuando el
vector se transforma en la cepa bacteriana; y f) recoger la proteína recombinante de la cepa bacteriana.
6. Una vacuna de epítopo de célula T que comprende una proteína recombinante, en la que la proteína recombinante comprende un epítopo de célula T, y en la que el epítopo de célula T comprende un fragmento peptídico de aminoácidos de una proteína seleccionada del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior.
7. La vacuna de la reivindicación 6, caracterizada porque el fragmento peptídico de aminoácidos comprende nueve a veinte aminoácidos.
8. Un método para producir una vacuna de epítopo de célula T que comprende:
a) proporcionar una proteína recombinante que comprende un epítopo de célula T, en el que el epítopo de célula T comprende un fragmento peptídico de aminoácidos de una proteína seleccionada del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior;
b) identificar el epítopo de célula T de la proteína;
c) insertar el ADN que codifica el epítopo de célula T en una construcción capaz de expresar el epítopo de célula T como una proteína; y
d) recoger la proteína.
9. El método de la reivindicación 8, caracterizado porque el fragmento peptídico de aminoácidos comprende nueve a veinte aminoácidos.
10. Una vacuna según la reivindicación 6 para uso en la prevención de un trastorno relacionado con Leptospira en un sujeto animal o humano que lo necesita.
11. Una composición farmacéutica que comprende: a) una cantidad terapéuticamente eficaz de la vacuna de la reivindicación 2, 5 ó 7; y
b) un vehículo farmacéuticamente aceptable.
12. Un anticuerpo aislado y purificado dirigido contra una proteína de la membrana externa de Leptospira, en el que la proteína de la membrana externa de Leptospira se selecciona del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior.
13. El anticuerpo de la reivindicación 12, caracterizado porque el anticuerpo está dirigido contra al menos un epítopo de célula T de la proteína de la membrana externa de Leptospira.
14. Un método para producir un anticuerpo dirigido contra una proteína de la membrana externa de Leptospira, comprendiendo el método:
a) proporcionar un animal huésped; e b) inmunizar el animal huésped por inyección con la proteína de la membrana externa de Leptospira, en el que la proteína de la membrana externa de Leptospira se selecciona del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior,
y en el que el anticuerpo reconoce específicamente al menos un epítopo de célula T de la proteína de la membrana externa de Leptospira.
15. Un anticuerpo dirigido contra una proteína de la membrana externa de Leptospira para uso en un método para diagnosticar un trastorno relacionado con Leptospira en un sujeto, en el que la proteína de la membrana externa de Leptospira se selecciona del grupo que consiste en:
(i) una proteína que tiene la secuencia de aminoácidos como se muestra en SEQ ID NO: 2 (LP1454) ,
(ii) un epítopo inmunogénico o fragmento inmunológicamente activo de la proteína de (i) anterior, y
(iii) un fragmento de proteína que tiene una longitud de al menos 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% ó 95% de la secuencia de aminoácidos de la proteína de (i) o el epítopo inmunogénico o fragmento inmunológicamente activo de (ii) anterior.
16. El vector según la reivindicación 1 para uso en la prevención de un trastorno relacionado con Leptospira en un sujeto animal o humano que lo necesita.
17. Una proteína recombinante según la reivindicación 4 para uso en la prevención de un trastorno relacionado con Leptospira en un sujeto animal o humano que lo necesita.
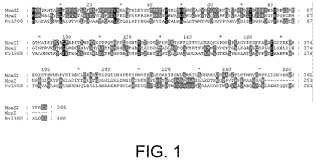
FIG. 1
FIG. 2A
FIG. 2B
FIG. 2C
FIG. 2D
FIG. 3A
FIG. 3B
FIG. 4
FIG. 5
Semejante a CADF 1: atgcgtcctttttctaaattaatttttattctggccttttgtatttttttgcccgttttctctcaacctctaccggaccttccggaaaaacaatttggtcaa cctcttaatacacaaaacgacgaatacaatcctatagtaagcccagatggaagatacatcgtattccagtccaaccgtccaggcggagaag gaggaatggacatttggatttccgagaacattcgctttttagataaggagataccagcagaatggactaaacccgtaaatatgaatcaaaata tttgggaagaattaaaacgtccaccagctgctggagttcgtaaaccaaatctattcaactctaacgcgtttgaaggtggaatttcaattcttttcg attctaacaacgcgccttcggaaatttattttacttctacaattaaccttgctgttgggcgttccggttttgaaggtttgaatatttatagaacaatta aagataaaaaaacaggaagatggacagacccagaacatctcagtgaaattaattccaacttcaatgataagatgcccgcaatttctcccgat ggaaattttttgatcttctcttcggaccgtccggggggttacggtgatttcgatctttggatctcggttcgtaatccaaaaaacggaagttggtcc caacctaaaaatttaggttctcccctcaactcttccgaaagtgaaattcttcctttcattcatcaagacggagaacaactttatttcagttctaatcg agaagacgaaagaaaaaaatttaagatttttagaatattcttaaaatataaatctgctctagacaacatgttagaagacgaagaagaaaccga agaaactcctacaaccaaaccgactgaaattttaattcctaaaattgatcaatcttctttattacttcttcccaaaccgtttaacactgataagtgg gaaggttttgataacgaaggaatcagttttgacaaagacggtatctgggcttatatttcttccaatcgttctggtggagaaggtcaatttgacatt ttccgctttcaagttccggaatctattcgcaactcctatactttaaacttcaaaggtctagttttggatggttccgaaaagacgatgattggattag attctactttaaaaatttatgatggaactaaaccggctaacgtaatcacttcgaaaagaatcggaggagatcttaccaaaggaaaaccttctaa ttttgcaacaactcttcaaaccggaaaggtttataaaatagaaattagttctcctggctttcatcctcaagaggatattttggatttaagaggaaa cataggtaaaaatcgaaaagtttatagaacctacgttcttttaccaattcaagttgaagaaggtaaaacggaagaaacaaaaatagaacaacc catagagaatcaaaaaccaaattctgccgcgttgaaagtcatcgtagcagacgcatctacaaaacaaatcataccagacgctaaagttactc tttttacacctatgaaccgcaaaggagaatctcttgtccaagatgcggataaaaaatcttttcttattaaaaaattaccagataacgattttgaatt atttgcaacagcttcgaaatatatttctgaaagtatcaatattattcaaaaaaatatttccaaaaatggaactgtaacaatttatctgaaagcagaa agcgacgtagatccggtttataatctacgagtttatttcgaatttaataaaacaaaaatcacagaagagaataaaaagttgctagatcctcttgt aggctatcttttgaaaaatgcgtccgataaaattgaaattgggggacataccgacaacgtagcctctaaggaatataacacaagattgagtgc caaaagagcccgtaacgtttacgagtatcttctttcaaaaggaattccggagaaaagaatgagaatcagggcttattggtattcacaaccgga tgcagacaatgagacagaaaccggaagagcaaaaaatagaagagttggttttagaaagctctga
FIG. 6A
Semejante a CADF 2: atgcataccctgctgactctgatcttaagccttttgcttttctctggtcttcagtctgagaataaaaattcttcctcaaaaaaactaagcgactctgc ttcttggattcctaaagaaaattttactcaactcgcatcacaaagagaaaaattcaaaaacgtttctcataacgaaacattaaaactagaaattg gctataaattattaactggaaaaattcttcagtttggaaaattacttagtaccgaaaacgcatacgtccccatcgaatccaacgaaattacttcc gaactttctcaactcaacgacaagaccgtaagaattttatgcagtatgaaaggttccacctgcaatcctatacgttatgaaatttatcccttttggt attcgaaagaaatcaaaccttggacgatcaaaaaaattcctgattacgtaaatcataatatttttgcattcaatcctacagtttccccagacggta aatatcttttttggaccgcttatgtcaaacgaggtaaatccggaactcaaaagatttggtattccaaattagacgaaaaaggtttttgggaagat ggtaaggaaatgaacgctcctttaaataatgaaatgccttccgctgttatctctgcacttcctggtggtaacgaacttttcgtctttggaacgtttg gcgaaaaagaacttttagacgaactcagtaaagattttgaaacgaaggcagacttggccgctcgttcttctaaaaattcaaacgtatatagaa aaaagatagaagaacttagagcagaatatgacgaaaaaacgaaacaaatttcaagcagagttcctctttataaaagttttaaggaaaaagatt cctggtctaaaccaagcatattaaactttcctaatttttataatctttatagaaagagaaacgattcaagccaagaaattttcggtggatctactctt tcttcttcagggagaattttaatctattcttctcaacataaggattccaaaggaaaattggatctttatgttagcaaaatgttaaacgacggaacct ttcctttaggtacaaacttaggagatgtgatcaacacaactcatgaagagatggctccttttttagcaagcgatgatagaaccctttatttttctag cgacggtcataaagggctctctatttatatgacaaaaagaatcggagaaggttgggatcaatggaccaaacctgtcgaggtttccgaaaatc taaaaggtgtaaattttttttcaattcccgcgaatagcgactgggcctatataagcaaagacggccgattgtttatggcttatcttcctaaagaaa tgcgcccagagaaggtcgtgatcataaacggaaaagttttagatacggatggtaaccctctttctgctgacatacattatgaatctttaaagtct cacgaaaagatcggtagcgccaaaagcgatccttctaatggtaatttttcgatcattctccccttcggcgaaaactacggtttttacgcccaga aaaaaggttatcttccagtatcacaaaatttgaatctaagttctaaaaagaaattctctgaaaaagtggaagtaattttacaacttcctccgatcc gagaaagaggttccattcaaatcaataatttattttttgagtccaagagttttcaaatcgctccggaatccgccccagaactggatcgtctcgcg gaaatcgtaaaggaaaatccagatattgaaattcagattgaaggtcataccgacaacattggcaagaaaaaagacaatctaattctttccgaa aaaagagcggcagcggtcgcagaatatctttttcaaaaacattctatttctaagactagaatccaaaccaaaggttttggggacagtgttccttt gagtaaaaatgattccgaagaagcacgcaaaaaaaacagaagggtcaattttacgattttgaaaaaaagtaaataa Semejante a CADF 3: ttggaaagttttttacactttccttatgttttaaaggaatcttacgaaactaaaactatggggaaattttccaatcaaccttcaaaatccaaaatcat aaacagacgtttacgaagaattgtatcatacgtttttattatttctacattgatcggttttacttctacttttccagaagaatcggacaaagttctcttt cgttggaaactaaaaccaggagagaatgtagaattaaacgaatatcatcgagtacaattagtaagtatgggaaagaaaattagaagagaag ataaaaatcgaatcctattacaaaccctttcctgcgaaaataaagaatgtacgttagaaggattttttgatacttacactcgttttcccgaagttga tcctgcgtttcgtaaagataaaacgtttaagagcagatttcaaataacagatttaggtcaatataaagtgccacaggaatacagtatgcctaatc tccgctctcttcctagtttttccgaaaaaccaatttccattggagaagaatggacacaacccgctacggaaagttttcaatttccaggaggaag ggttatgatcacggtttttgcgaaatataagtatcacggtgtagacgaatgggaatatcaaaagttgtccggtaaaggagatcgtatcgaatac aattataatttatattatgattctcaaatgaacagaaccggggttccatttaagatctacggatttgcgcgaggaatggtattttttgatcgcgaac ttggaattccacaatataaaagggttcagttgtcgtacacttttgtctatgaaaatggaatggcgcaagagatgtcgttcgacattcacggagta tataataaaaacgtaaaacttacggatcaagacaaggacaagtttgcggaagaaatccgtaaaattttaggaggagaacttccaactggaat tgaaccagattccgattcaaaaaagaatttaaaaaaaccgaaaaaggaaaccatttcatggccggaagaagaggataatcaagccgcacc agaaagttcgccggtagaaattagaagaacagaagaaggaatcgctatttctttaaattcagtgttgtttgatcacaacagctcagaacttaaa caagaagcaaaattagaattaaaaagaatcgcatccgtattgaaaaaatatgcagatagagaaatcagaattagcgggcatactgacaattc aggcggggaagaatataatcgaaaactttccagagaaagagcactttccgttttgaaggaactcagagatgaacaaggtttggaagaaaaa agaatgtcttacgaaggatatgggaaatcaaaaccgattgcagataactctacgattcaaggtaggcaaaaaaatcgtagggtagatattact attgtaatggaataa
FIG. 6B
Lp0022: atgaaacaatttttatttttactgtgtgtatttctactctttcaaaattgttctgtcaagcccacggaaaatccgtgcgatacgagtacttctctttttta taaatctttgttcttaaattttattttaacttccggcaaaacgagtatttgcggtatgcacacgtcggttcagttgcctccccctacgattctcaacat aaaatcaaaaagtactttgaatacaggatttttaattggtgaaatggatgagtctgcttccggagttcaaatttctttagattcgggtccatttatg gacgctcaaacttctggcaatcagtggaaatttcaacttcctgccgcaggtgtttctactacaattccttcaagtggaatttggagagactgga gtttacatacaatttcggttcgatctacttctaaggaatcaaattctattccgattacaatcactgttcaaaaaggttcaaacaaggatattaacgg cgacggttatccagatgcattgattggttctcaagctgcaaatcgagttagggcttatctttctcttgggaaagcaaagggtttagatttggttcc ggtcactttactaaatggggcaggtggatttggttattccgtcaagttaggcgacatcgatggagatggatacgccgatgcagttgtaggaa gtgcaacaaatacattcgctatttatttaggatcaatcggtgggctttcgacaacggcgattaattatatccctattggtgttggtggtttattgaat gtggatgtaggagatataaacggagacggattttcagacgttttgattggtgtaccttatgacgtaggaaatattgggcgtgtttattcttattttt caaatggagttatggggcaaggtgttacgtttggtcaacaattgaacaatcctggaaatgcaggtagtgctgcattttacggatatgccattac gttaggtgatattaatggagatggtaaatcggatgcgattataggagcggtcggttctggacaggtcggcgcttcttttatttatcttgcgcaag cagcaggggcttttgctgcttattctcaaacaattacgggatcggctgcaaatgaatggtatgcaaattcagcaattgctaccgatataaaccg ggatggatttgcggatttatttgtgggggcttatcaagaatcgggcggcgttggaagagtacatttatatttatctaatttaggaattcttgtgaat accgccaacggtccaatttcaggattggttgggtcacaaactggaacttctgtggcaactggagatgtaaacggtgatggatttttagatcttc ttaccggaggttattcttacacttctacgtttccaaatcaaggttatgcgattactcatttaactacgggtgatacaatgggtttaactgtgaaccc tttaaatcttctaacggttccagtgaatttaggagatatgggaaattcaattgcttcggtagatattaacggtgacggtttaagtgacgttcttgtg ggagctcctagttccgtaggtggaacaaatgttggaaacgtttacctttatatatcaaacggattggacggatatacttcggccccacaaatttt cgtcgaaccagatgtaaacggaacgtttgggacttccgtggatttatga FIG. 6C
Lp1499: ttgaacacatccatccaagttggttttagtcaaaaattggattcttctagtatccaatctcaatcgatccaactaacacaaggaaatacgatcatt ccgggaaatttcacttctacagaaaaaactcttttattcaatccaacgtcttccttggctgcatcaactgtatattccgttagcatttccaaagaca taaaatcaatggacggctcctctctttcagaagactatacttggagctttaccaccaacacgattgttgatttagtcgcgccagacgtatctttaa gaacccctaccataggtgccaatttagttcctaataatacttccgttcaaattgcgtttactgaaacaatgaattgcacttccatcaacattgtaaa ttttacattaaaaaataatgttaccaatgtattagaacctagtaatgtagtttgtttaggatccgttgccacccttacccctaataatcctcttgctttt aatactgtttatcgtgtggatattctttctacagcaaaagatcttgctaataatcctcttgtaaacgcatataactggacttttacaaccggagttgc ccccgatttaacggttccaaccgtctcctttgtaaatcccactcccaatgcacaaaacgttcctatcaacgaaacaatcagtattgcctttagtg aacctatcaattgtgctacgatcatcggaagtattgtcttagatgataatatacttattcctggaagcgtaaacgggaatccgggttgtacaggc acaaccgcatcctttactcctttaggcaatttgacaccaaatacgaattatacggttaccgtctcaaatgcgattacggatttgcaaaacaatcc acttacaccttctacctggagttttacgacggctgctgcagtcgatcagactcaacccacggttacatttactgtaccctccgccaacgcaaac ggcgtagggaccaatgtcaaccctatggtagtttttagcgaacctatgtcttgcgcttccgtgacctccgcatcctttcgattaaagaggcagg caaccggggtttatcttataggaagtgtaaattgttttggaacttccgctacctggaccccagatcctgtaaatccgcttgcctttaatactactta caccgtagaaatcgatcagggtgcattagatacttttaataatcctctcattccaataaattggaactttactacaggcccaggacccgatctaa ctcctcccagtgttgccgtcgttactcccgcaaacgctgcgataggcgttccgaccaacggaggtgtaagtatcgcttttagtgaagccatga attgtggaagtattttaggaggaatcaccctggacgatgatcctacaactccgggtactgtgattccaatcaatatcaattgtaacggaaatact gtctcttttgccccgacaatccctccacttgcctttaatacaacctacacagtaacgattttaaatacggttacggacagtaataataatgcacta aacggaggaaattacgcttggtcttttacaacaggagtggcaccagacctagttcctcctcaagtttctcttgtaagccctctctcgggagcag taggtgtcgcaacaaatgcaaacattacagttgcatttaatgaaaccatcaattgttccaccttgaattttacggttaataacggaatcaatggta ctgtgaactgttcaggatcctctgctacttttattcctagcgctttaacccctctaaatgccggtacaaattatacagcaacaatcctaacagtaa atgatattgtaggaaatccaatcggtgctgcgtttggttggagttttacaaccggagccgctccagatgtgactcctcctgtcgttacgatcca aaatcttagaaataattctatcgtagaaactggtttcgtaattggaacggcaacagatgcaggcacaattacttctgtagaagtttctttggaca atggcgcttttgtgcccgcaaccggaaccaatccttggaaatttaaacttccttcggatataaatacttggaagcaaaactctcaacatacgat cattgcaagagctaaggacttagccaataaccttacaactacagcagccatttcggttcgaaaaggaaacaataaagatataaacggagac ggatacgttgatcttgtatctgcagaatacggacagggtttactttatatttttcattcttccgggaacgctggaatgacaattacaaacgcacaa tccgcaagtaagatcattgtaggagtcgcggcggaagaatttggaagaactgtttctatgggagatttaaacggagatggatttgcagacgt aatttctggtgctcctggttggaacggtgcccaaggtagggtttatatatttcattcttccggaaacgctggagtcaatatttccttttccggttttg ccactaaaacgatcagtggagccaatgcgggagctagatttggagatagtattgttacaggtgatttaaacggagacggctacgcagacct agcatcaggagaacccgtttttaatggttctcagggtagagtctatgtatttcattccgctggagccgctggagttacacaaataaattcggct gctgcaaattctacactcacaggtgaaaacgcaactgatcgtttcggatattcgttgagcactggaaatatgaacggagataattttgcagatc ttgcaattggagcacctggttatggcgctggcgtaggtggaggatttgtagtaaaccaaggtaaagtttatatacatcacggggcggctggt ggattgggaggagtaattacaactcttaccaatgatagcgctggaaatgctggggaatttggtatcagtttatttacagccgattttaacggag acggtaattccgatcttgcaattggaagtccaaatttagggggtggaactggaagagtttccgtatttacgtctgcaggaggtgtaggtataaa tacatctacgattggaaacgctccgcttatgatcaatggaacggctgtgggtaatgcatttggaatttctttaaccgcacaggatttaaatttaga tggaagaccggatttaatttccgcaaccgtaattcccaatagggtattcgttttccacatgccaggtgcaggagctatcggtggatttctaacc actggtaatgcaactacacaaatcacgagtgcatttgcaggaatcggggtttccccaaatgcacctaaaactcctatttccggcggagacat caacggagacggatttccagacttatttgtcgggggaagttctgataatatttttattttccattcttcaacggttggaactggtttattaacaaata ctactgcaaccgctgcaggcgcaattaccagttccggacttgccaatggcttttttggatgtagcgtttattga
FIG. 6D
Lp4337: atgagcctaaaaaataaaaattatgttttatcaaaaaaaaccatattgattctatttttagtatattttgtttttataatttcttttttttctatttactctcag gatttaagtataaatcaaaatcctaaaccagaaaagttaaaaggttctatcaatacgagtctcaatgagtttggaatcagtcttactgatgacgg aaatattttatatttctattctaaaagacaaaattcaaattatacagacatttataagtcaactcgaacgaaagatgaatggacacaaggagagg aaattgaagttctaaattcaaactttgacgaccaaagtcctttcattttaaaccgagaagaaggaattcttttttcatctaatagagatggtgcgac cgaattccaatttgcaaatggaaaaatcggagtttctagagatatttatttttctaaaaaaataaattcttcttggacagaaccggttcttcttccta gagccgtgaatacggaagaaatcgaagaaaatccgtttctatttaataatagattgtattttacccgttatccttttgggcaagtttcagaagcgg acattttcgtttctgtttataaaaataacacttgggaaaaagcaatgagcctccctgatccgattaacaccgtttattcggaaattgcggctacaa ttagtaaagatggaaagacgatttatttttcttctaaccgtccggggggttttggcggttatgatttgtataagtctactttacttgaaaacggaaat tattccgaaccgattaatcttggacccgaaattaacactaccggagatgaggctttttttctggaaacaaacgatagaaagacattctatttttgt agaaggaaagaacgcgattatgatatttattctatcgtttctaacccgtttcaagaactagaaaaaggaaaatctatttctttggatagtatccatt tttctttgggctcttatgaaattctcgaaaattctttttcaattttagataatttgaattcttatcttaaggaaaatttaaatataaaaatcaaaatcacc ggccataccgatcttaatggagattcccaggacaaccttattctcagccgtaatcgtgcaaatgcagtaaaggattatttagttaaaagggga atcgattctcaaagaattatcacggatgggaaaggtagttcggagccaattgttcctatgaaaaatccagagacggattataaaaatagaaga accgaatttcagattatcagtcgttag
Lp328: atggcgaagaaagaaaactactatattactatcaaaggtagaaaatatgatcgtaagttgatccagctcgcggaagagttcacttccggtaa acgggacggtaagatttcgatcaacgacgcaaaacgtcttttaaaaattgtcaaggataacaacgcttatacggatatagaaaaacatacgat cgaatacattcgtgaaaactataagtttaccgaaaaatcggacgaatggttccgttcagaaatccgtaaatgggccgctaaaaaagtgcaag aagcaaaaaagaaaagtgatgtggaatccatcctagtcgatgattctgaagcgccggaaataaattttccttccagttggggagaagacaaa accgaagttgttgaaattacacaaacctctaaaatagattggagagaaaattcaaatttttcatccgcaacgtctcactctaaaaaaaataaaaa gatcattccaactttaatttttctttctggttttttgattcttgtaggtttagtttatttttttcgaaccttattttataaggaagacttggaacaagtagtaa aaacgaattctgagattgtctctaattcaaaagaaaaacaatccgacgtttcgatagaaaaagcagaatctacaaaggaagttcgaaagaaa aacgtaagatctaaaaaagaagaatcggaaattccaaaaaatgctcttacaattctaaaacctcaaaccggaaagaagttagaatctaaatcc ttattctcttcgttgacaaatcaaaattccacagaagaattttcttccaatcctcaatttagagaaattgaatccaatgtaattcgttttgaaaaaaa cagcattcaaattcataaagaatcgagaccaagtctcaaccgtttggctcgctggatgaaacaggattcttcgatccgagtcaaagttatcgg tcatacttctttagagggtagcgaagacgccaatcaaaaagtttctcttcttcgtgcacaaacggttcgaaattatatcgccgggaatggcattt ccaaagatcgttttgagattattcccaaaggcgcaagcgttcctattggcgataattctaaagaagaggggaaggaaatgaatcgtagagtg gaacttagaatctataattga L21: atgaaatataaaataattttaattttatcactaatgttatttcttttcgtttcctgtccggatgaaaaaaaagaaaatgaattgagtacttatattttata tagtgttctcataaacgcaactactcaatacgattgtgttactagttcggaagtagtatcagactcttataacaaaacaacaataaccttcgaaa ataaacctcaatattacaattcacccagtggaaatgtagttccaaaagcaattatgccgattttgattaaaaaggggcagacaattcaagtatc cagtataacgactaacgttaagtatgaagcgacaaaccaagacttaacttttctttttagaaaagatggttgtcacggtacaaactccgaaattg caacctatgcaggagctactaatacaaatgtttttttaggaaacacaaatactgttagcttaactcaatttaaatttaccgccgactataatggga ttatactaatcgttgggaaaaacctaggtgcaagtttacctggagatattcgtgtgaatgtattttaa
FIG. 6E
100
Patentes similares o relacionadas:
Fragmentos mutantes de OspA y métodos y usos relacionados con estos, del 4 de Marzo de 2020, de Valneva Austria GmbH: Un polipéptido que comprende el polipéptido con la secuencia de aminoácidos de la SEQ ID NO: 190; o cualquier variante funcional de dicha secuencia de aminoácidos […]
Fragmentos mutantes de OspA y métodos y usos relacionados con los mismos, del 5 de Junio de 2019, de Valneva Austria GmbH: Un polipéptido que comprende un fragmento de OspA C-terminal híbrido (proteína A de la superficie externa de Borrelia), en el que el fragmento de OspA C-terminal híbrido […]
Péptidos de diagnóstico para la enfermedad de Lyme, del 12 de Febrero de 2019, de Biopeptides Corporation: Una composición que comprende dos o más de los siguientes péptidos aislados en donde al menos uno de los péptidos en la composición es un péptido seleccionado del grupo […]
Fragmentos mutantes de OspA y métodos y usos relacionados con los mismos, del 5 de Septiembre de 2018, de Valneva Austria GmbH: Un polipéptido que comprende el polipéptido con la secuencia de aminoácidos de SEQ ID NO: 186; o cualquier variante funcional de dicha secuencia […]
Antígenos TpN47 de Treponema pallidum inmunorreactivos solubles, del 26 de Febrero de 2016, de F. HOFFMANN-LA ROCHE AG: Un antígeno 47 soluble de Treponema pallidum (antígeno TpN47) que comprende los residuos de aminoácidos 63 a 174 (dominio B) de Swiss Prot P29723 con la condición de que dicho […]
Proteínas utilizadas para el diagnóstico de una borreliosis de Lyme, del 25 de Junio de 2014, de BIOMERIEUX: Proteína quimérica de fusión DbpA-OspC de Borrelia, seleccionada del grupo que consiste en: (a) una proteína cuya secuencia en aminoácidos comprende en su […]
Proteínas utilizadas para el diagnóstico de una borreliosis de Lyme, del 30 de Octubre de 2013, de BIOMERIEUX: Proteína quimérica de Borrelia que comprende al menos una secuencia del dominio extracelular de unaproteína VlsE de una primera especie de Borrelia que corresponde a […]
 Polipéptidos y procedimiento para la detección específica de anticuerpos en pacientes con una infección por Borrelia, del 6 de Septiembre de 2013, de EUROIMMUN MEDIZINISCHE LABORDIAGNOSTIKA AG: Proteína que comprende un primer polipéptido de OspC, caracterizada porque el primer polipéptido de OspC está unidoa través de un puente disulfuro con un segundo polipéptido […]
Polipéptidos y procedimiento para la detección específica de anticuerpos en pacientes con una infección por Borrelia, del 6 de Septiembre de 2013, de EUROIMMUN MEDIZINISCHE LABORDIAGNOSTIKA AG: Proteína que comprende un primer polipéptido de OspC, caracterizada porque el primer polipéptido de OspC está unidoa través de un puente disulfuro con un segundo polipéptido […]