Procedimientos para distinguir entre la glutamina formada por cataplerosis o formada por proteólisis.
Un procedimiento para distinguir entre la glutamina formada por cataplerosis o proteólisis en un sujeto,
que comprende someter a ensayo una muestra corporal del sujeto para glutamina deuteradaen donde la muestra corporal procede de un sujeto al que se le ha administrado agua deuterada (2H2O) y que hasido tratado con un agente que promueve la excreción de glutamina del sujeto; y
en donde las contribuciones catapleróticas y proteolíticas a la formación de glutamina se cuantifican analizando elenriquecimiento en 2H de la glutamina, indicando así las proporciones de glutamina en la muestra corporal formada apartir de la cataplerosis y de la proteólisis.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/001282.
Solicitante: Biocant - Associação De Transferência De Tecnologia.
Nacionalidad solicitante: Portugal.
Dirección: Centro de Inovacao em Biotecnologia Biocant Park Parque Tecnologia de Cantanhede Nucleo 04., Lote 3 Cantanhede 3060-197 PORTUGAL.
Inventor/es: JONES,John Griffith.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/68 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen proteínas, péptidos o aminoácidos.
PDF original: ES-2384603_T3.pdf
Fragmento de la descripción:
Procedimientos para distinguir entre la glutamina formada por cataplerosis o formada por proteólisis [0001] La presente invención se refiere a un ensayo para distinguir entre los orígenes de la glutamina en el cuerpo de un ser humano o de un animal. El ensayo es particularmente adecuado para distinguir entre fuentes catapleróticas y proteolíticas de glutamina hepática.
La glutamina es un abundante aminoácido no esencial que está muy involucrado en la transferencia de carbono y nitrógeno entre diferentes órganos y tejidos. El músculo esquelético es la fuente principal de producción de glutamina en todo el cuerpo, lo que supone el 50 – 70 % de la tasa de aparición (Ra) de la glutamina. El esqueleto carbonado de la glutamina es utilizado por el intestino como fuente de energía y por el hígado como precursor gluconeogénico. Termodinámicamente, la glutamina es un potente aminoácido gluconeogénico puesto que su conversión a los azúcares-fosfato va acompañada por una ganancia neta de ATP y equivalentes de reducción. Existen evidencias de que la glutamina procedente de tejidos periféricos es una importante fuente de carbono para la gluconeogénesis hepática. Por tanto, alteraciones en la producción de glutamina en todo el cuerpo pueden tener un efecto significativo sobre la actividad gluconeogénica y el metabolismo de la glucosa hepática.
La glutamina puede proceder tanto de fuentes metabólicas como proteolíticas puesto que su Ra puede verse influenciada por cambios en la actividad metabólica periférica o en la cinética de proteínas en todo el cuerpo.Éstas podrían incluir el equilibrio entre el anabolismo y catabolismo de las proteínas de todo el cuerpo así como las actividades intermedias de flujo metabólico de diversos tejidos periféricos.
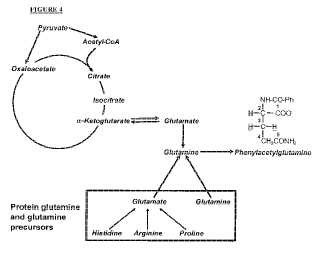
El músculo esquelético presenta un reservorio de glutamina libre relativamente grande que se encuentra en rápida renovación y procede tanto de actividades metabólicas como proteolíticas. El contenido en glutamina de las proteínas musculares solubles en bases es del 4 % aproximadamente, por lo que la degradación de proteínas supone una fuente directa de glutamina. Además, la glutamina se puede sintetizar a partir de otros aminoácidos que se liberan durante la proteólisis, incluyendo prolina, histidina, asparagina y glutamato. De estos precursores, el glutamato es cuantitativamente el más importante puesto que su abundancia en las proteínas del músculo esquelético es ѝ 4 veces superior a la de la glutamina. En consecuencia, cada equivalente de glutamina que se libera directamente por la proteólisis de músculo esquelético va acompañada por cuatro glutamatos que potencialmente se pueden convertir en glutamina. La glutamina también se puede obtener a partir del reservorio de metabolitos del ciclo de Krebs a través del a-cetoglutarato y glutamato. La producción neta de glutamina a partir de esta fuente requiere que el a-cetoglutarato que se pierde en el ciclo de Krebs se compense con la introducción anaplerótica en el ciclo. En el músculo esquelético, las actividades de la piruvato carboxilasa y la enzima málica permiten la utilización anaplerótica del piruvato. Se ha informado de la presencia de niveles significativos de flujo anaplerótico en el músculo esquelético de rata mediante marcadores 13C.
Desde hace mucho tiempo existe la necesidad médica de que un facultativo sea capaz de identificar las fuentes de los carbonos de la glutamina en todo el cuerpo para la actividad gluconeogénica hepática. Una enfermedad crítica se caracteriza por una pérdida de masa corporal magra (deterioro muscular) por lo que existe potencial para el aumento en la generación de glutamina a partir de la degradación de proteínas. Este escenario también se caracteriza por hiperlipidemia y tasas elevadas de gluconeogénesis hepática. Dado que la glutamina puede ser un contribuyente importante en la gluconeogénesis hepática en sujetos sanos, el aumento de la disponibilidad de glutamina hepática durante la enfermedad podría contribuir a elevar los flujos gluconeogénicos hepáticos. No obstante, hasta la fecha, no ha sido posible detectar en qué grado contribuyen la degradación de proteínas en todo el cuerpo y los flujos catapleróticos al reservorio de glutamina hepática. Los procedimientos actuales pueden estimar la contribución de glutamina liberada directamente por la degradación de proteínas a la Ra de la glutamina en todo el cuerpo. No obstante, en la medida en que se sintetice la glutamina a partir de otros aminoácidos liberados durante la degradación de proteínas (principalmente el glutamato) , los procedimientos de la técnica anterior sustancialmente subestiman la contribución total de la degradación de proteínas al reservorio de glutamina hepática y no son útiles para la detección temprana del deterioro muscular.
Por tanto, es un objeto de la presente invención evitar las desventajas asociadas a la técnica anterior y proporcionar los procedimientos mejorados para distinguir entre los orígenes de los esqueletos carbonados de la glutamina hepática.
Según un primer aspecto de la presente invención se proporciona un procedimiento para distinguir entre la glutamina formada por cataplerosis o proteólisis en un sujeto que comprende someter a ensayo una muestra corporal procedente de un sujeto para glutamina deuterada;
en donde la muestra corporal procede de un sujeto al que se le ha administrado agua deuterada (2H2O) y que ha sido tratado con un agente que promueve la excreción de glutamina del sujeto; y en donde las contribuciones catapleróticas y proteolíticas a la formación de glutamina se cuantifican analizando el enriquecimiento en 2H de la glutamina, indicando así las proporciones en la muestra corporal de glutamina formada a partir de la cataplerosis y de la proteólisis.
Kuhn y col., 1999 (Am. J. Clin. Nut 70 (4) : 484 – 489) se propusieron medir la glutamina en proteína muscular. Usaron datos compilados procedentes de estudios previos para recalcular las contribuciones de la proteólisis y la síntesis de novo a la producción endógena de glutamina en especímenes de músculo (biopsias abiertas) procedentes de seres humanos, ratas, vacas y cerdos.
Hankard y col., 2000 (Am. J. Phys. End. Met 279 (3) : E608 – E613) investigaron el papel de la glucosa en la regulación del metabolismo de la glutamina en sujetos sanos y con diabetes de tipo 1 dependiente de insulina usando una infusión continua elaborada de D-[U-14C]glucosa, L-[5, 55-2H3]leucina y L-[3, 4-13C]glutamina y controlando la glucosa plasmática.
Chapa y col., 2000 (Neurochem. Int. 37 (2 – 3) : 217 – 228) utilizaron espectroscopía de RMN [13C, 2H] ex vivo para estimar los tamaños relativos de los reservorios de glutamato neuronales y gliales y las contribuciones relativas de (1-13C) glucosa y (2-13C, 2-2H3) acetato a los ciclos de los ácidos tricarboxílicos neuronales y gliales en cerebro de adulto. Las ratas se infundieron durante 60 minutos en la vena yugular derecha con disoluciones que contienen (2-13C, 2-2H3) acetato y (1-13C) glucosa o (2-13C, 2-2H3) acetato solo. Al final de la infusión los cerebros se congelaron in situ y se prepararon extractos con ácido perclórico y se analizaron mediante espectroscopía de RMN13C de alta resolución (90, 5 MHz) .
Jones y col., 2001 (Am. J. Phys. End. Met 281 (4) : E848 – 856) usaron un estudio de gluconeogénesis con RMN 2H y 13C integrada y el flujo del ciclo de los TCA en seres humanos. Se midió la síntesis de glucosa hepática procedente de glucógeno, glicerol y del ciclo del ácido tricarboxílico (TCA) en cinco sujetos mantenidos en ayunas durante toda la noche mediante análisis de RMN 1H, 2H y 13C de glucosa en sangre, acetaminofen glucurónido en orina y fenilacetilglutamina en orina después de la administración de [1, 6-13C2] glucosa, 2H2O, y [U13C3] propionato.
Perdigoto y col., 2001 (NMR in Biomed. 16 (4) : 189 – 198) examinaron el metabolismo de la glucosa en cinco sujetos sanos mantenidos en ayunas durante 16 horas, medidos con una combinación de [U-13C3] glucosa y marcadores de 2H2O. La producción de glucosa se cuantificó por análisis de RMN 13C del derivado de monoacetona de glucosa plasmática.
Kadrofske y col., 2006 (Am. J. Phys. End. Met 290 (4) : E622 – E630) examinaron el efecto de aminoácidos intravenosos sobre las cinéticas de la glutamina y de proteínas en recién nacidos prematuros con bajo peso. Se determinaron las cinéticas de la síntesis de novo de glutamina, leucina N, fenilalanina y urea utilizando marcadores isotópicos... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para distinguir entre la glutamina formada por cataplerosis o proteólisis en un sujeto, que comprende someter a ensayo una muestra corporal del sujeto para glutamina deuterada en donde la muestra corporal procede de un sujeto al que se le ha administrado agua deuterada (2H2O) y que ha sido tratado con un agente que promueve la excreción de glutamina del sujeto; y en donde las contribuciones catapleróticas y proteolíticas a la formación de glutamina se cuantifican analizando el enriquecimiento en 2H de la glutamina, indicando así las proporciones de glutamina en la muestra corporal formada a partir de la cataplerosis y de la proteólisis.
2. El procedimiento según la reivindicación 1, en donde el sujeto es un ser humano.
3. El procedimiento según la reivindicación 1 o 2 en donde la muestra corporal es una muestra de orina.
4. El procedimiento según la reivindicación 3, en donde el agente promueve la excreción de glutamina en orina.
5. El procedimiento según la reivindicación 4, en donde el agente incluye una fracción fenilacetilo.
6. El procedimiento según la reivindicación 5, en donde el agente es uno comprendido entre: aspartamo, fenilacetato sódico o fenilbutirato sódico.
7. El procedimiento según las reivindicaciones 4 o 5 en donde el agente y la glutamina se combinan para formar una fenilacetilglutamina (PAGN) .
8. El procedimiento según la reivindicación 7, en donde la muestra de orina se procesa adicionalmente para liberar glutamina o glutamato.
9. El procedimiento según una cualquiera de las reivindicaciones precedentes en donde la muestra se somete a ensayo llevando a cabo resonancia magnética nuclear de 2H para identificar la glutamina deuterada o uno de sus derivados deuterados.
10. El uso de un procedimiento según una cualquiera de las reivindicaciones 1 – 9 para evaluar el estado de salud de un sujeto.
11. El uso según la reivindicación 10, en donde el sujeto es sospechoso de padecer una enfermedad crítica que está al menos parcialmente caracterizada por una proteólisis incrementada.
12. El uso según la reivindicación 10, donde el sujeto presenta, o es sospechoso de desarrollar, deterioro muscular.
13. El uso según la reivindicación 10, en donde el sujeto es sospechoso de padecer una enfermedad crítica que está al menos parcialmente caracterizada por una cataplerosis anormal.
14. Un procedimiento de selección de un compuesto para establecer si el compuesto es proteolítico o anabólico que comprende someter a ensayo una muestra corporal procedente de un sujeto para glutamina deuterada;
en donde la muestra corporal procede de un sujeto al que se le ha administrado agua deuterada (2H2O) , ha sido tratado con un agente que promueve la excreción de glutamina del sujeto, y ha sido tratado con el compuesto; y en donde, cuando se compara con un control, un incremento en la proporción de glutamina deuterada indica que el compuesto es anabólico o reduce la proteólisis y una reducción en la proporción de glutamina deuterada indica que el compuesto promueve la proteólisis.
15. El procedimiento según la reivindicación 14, en donde el compuesto es un candidato a producto farmacéutico.
Patentes similares o relacionadas:
Inmunomoduladores, del 29 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de la fórmula (I) **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de **(Ver fórmula)** en donde: […]
Métodos y composiciones para el diagnóstico y pronóstico de lesión renal e insuficiencia renal, del 29 de Julio de 2020, de Astute Medical, Inc: Un método para evaluar el estado renal en un sujeto, que comprende: realizar una pluralidad de ensayos configurados para detectar una […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Método para llevar a cabo el seguimiento de la enfermedad de Gaucher, del 15 de Julio de 2020, de Centogene GmbH: Un método para determinar la evolución de la enfermedad de Gaucher en un sujeto, que comprende la etapa de determinar en varios puntos en el […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Biomarcadores de pronóstico y predictivos y aplicaciones biológicas de los mismos, del 1 de Julio de 2020, de INSTITUT GUSTAVE ROUSSY: Un método para evaluar la sensibilidad o la resistencia de un tumor frente a un agente antitumoral, que comprende evaluar la cantidad de complejo eiF4E-eiF4G (complejo Cap-ON) […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]